Углеводы – источник питания
Содержание.
Введение……………………………………………………….
Глава 1
Классификация углеводов и нахождение их в природе….…стр.
Глава 2
История открытия углеводов…………………………….……стр.
Глава 3
Углеводы – источник питания………………………………..стр.
Заключение……………………………………………………
Используемая литература…………………………………….стр.
Приложение
Введение.
Предмет исследования: углеводы растительного происхождения, характеристика их строения, свойств и пищевая ценность.
Задачи:
- Выявление строения молекул углеводов, их свойства.
- Изменения
углеводов в процессе технологической
обработки пищи.

Цель
работы: изучить теоретические воззрения
по вопросу исследования строения углеводов
и их свойств, прогнозировать пищевую
ценность.
Углеводы – обширный класс органических соединений. В клетках живых организмов углеводы являются источниками и аккумуляторами энергии. В растениях (где на долю углеводов приходится 90% сухого вещества) и некоторых животных они выполняют роль опорного материала, входят в состав многих важнейших природных соединений, выступают в роли регуляторов важнейших биохимических реакций. Соединяясь с белками и липидами, углеводы образуют сложные высокомолекулярные комплексы, составляющие основу субклеточных структур, а следовательно основу живой материи.
Углеводы занимают исключительно важное место в питании. Их доля по калорийности в продуктах питания составляет от 50-80%.
Название
«углеводы» предложил в 1884 году русский
химик К.Г.Шмидт, исходя из того, что
эти вещества по составу формально
соответствуют соединению углерода с
водой общей формулой Сm(Н2О)m . В дальнейшем стало известно много углеводов,
не отвечающих этому условию, однако название
«углеводы» прочно укоренилось в химии,
биологии, медицине и других смежных науках.
В дальнейшем стало известно много углеводов,
не отвечающих этому условию, однако название
«углеводы» прочно укоренилось в химии,
биологии, медицине и других смежных науках.
Углеводы содержатся преимущественно в продуктах растительного происхождения. Образование углеводов в природе начинается со сложнейших биохимических реакций в процессе фотосинтеза растений из диоксида углерода и воды, который происходит в зеленых частях растений при участии хлорофилла. Этот процесс сопровождается поглощением тепловой энергии. Суммарный процесс фотосинтеза можно изобразить следующей схемой:
nCO2 +nH2O→ Cn
Методом
меченых атомов показано, что в
процессе фотосинтеза кислород воды
выделяется в атмосферу. В процессе ассимиляции
углекислого газа растения ежегодно синтезируют
до 1000 млрд. тонн биомассы, связывая до
150 млрд. тонн углерода и 25 млрд. тонн воды.
При этом в атмосферу поступает до 400 млрд.
тонн кислорода.
тонн воды.
При этом в атмосферу поступает до 400 млрд.
тонн кислорода.
С углеводами мы встречаемся в домашнем быту буквально на каждом шагу. Во-первых, они содержатся в больших количествах в муке, крупах, картофеле, фруктах и ягодах. Во-вторых, применяется в кулинарии и в чистом виде: крахмал используется для приготовления киселей, сахар – для сладких блюд.
К углеводам относятся простые сахара (глюкоза – виноградный сахар, фруктоза – фруктовый сахар), а также сложные сахара, или дисахариды (свекловичный, молочный, солодовый, грибной) и полисахариды (крахмалы, клетчатка).
Углеводы – один из важнейших пищевых веществ. Они являются в нашем питании наряду с жирами основными поставщиками энергии. Каждый грамм углеводов дает 3,75 – 4 ккал, общая потребность в них для взрослого человека составляет 400 – 500 грамм в сутки с синтетическими заменителями.
Глава 1.
Классификация
углеводов и нахождение их в природе.
Углеводы широко распространены
в природе и играют большую роль в биологических
процессах живых организмов и человека.
В зависимости от их строения можно подразделить
на моносахариды, дисахариды и полисахариды.
Углеводы
↓
Моносахариды
↓ ↓ ↓ ↓ ↓ ↓ ↓
Глюкоза Фруктоза
Рибоза Сахароза Мальтоза
Крахмал Целлюлоза
Моносахариды. Молекулы моносахаридов построены из
неразветвленных углерод-углеродных целей,
содержащих различное число атомов углерода.
В состав растений и животных входят главным
образом монозы с 5, 4, 6 углеродными атомами
– пентозы и гексозы. У атомов углерода
расположены гидроксильные группы, а один
из них окислен до альдегидной (альдозы)
или кетонной (кетозы) группы.
Мы порой и не подозреваем, какие важные превращения претерпевают некоторые моносахариды, например глюкоза.
При изучении состава глюкозы выяснили, что ее простейшая формула СН2О, а молярная масса 180г/моль. Отсюда можно сделать вывод, что молекулярная формула глюкозы С
6Н12О6. Для
установления структурной формулы
молекулы глюкозы необходимо знать
ее химические свойства. Экспериментально
доказали. Что один моль глюкозы реагирует
с пятью молями уксусной кислоты с образованием
сложного эфира. Это означает, что в молекуле
глюкозы имеется пять гидроксильных групп.
Так как глюкоза с аммиачным раствором
оксида серебра дает реакцию «серебряного
зеркала», то в ее молекуле должна быть
альдегидная группа. Опытным путем также
доказали, что глюкоза имеет неразветвленную
углеродную.
На
основании этих данных строение молекулы
глюкозы можно выразить следующей
формулой:
Н Н Н ОН Н
Н – С – С – С – С – С – С
ОН ОН ОН Н
ОН
Как
видно из структурной формулы, глюкоза
является одновременно многоатомным спиртом
и альдегидом, т. е. альдегидоспиртом. Так
как в молекуле глюкозы С6Н12О6 шесть атомов углерода, то она является
представителем гексоз.
е. альдегидоспиртом. Так
как в молекуле глюкозы С6Н12О6 шесть атомов углерода, то она является
представителем гексоз.
Дальнейшие
исследования показали, что кроме
молекул с открытой цепью для
глюкозы характерны молекулы циклического
строения. Это объясняется тем, что молекулы
глюкозы вследствие вращения атомов углерода
вокруг связей могут принимать изогнутую
форму и гидроксильная группа пятого атома
углерода может приблизиться к альдегидной
группе. В последней под воздействием
гидроксильной группы разрывается П –
связь. К свободной связи присоединяется
атом водорода, и образуется шестичленное
кольцо, в котором альдегидная группа
отсутствует. Доказано, что в водном растворе
существуют обе формы молекул глюкозы
– альдегидная и циклическая, между которыми
устанавливается химическое равновесие:
В
молекулах глюкозы с открытой
цепью альдегидная группа может
свободно вращаться вокруг —
связи, которая находится между первым
и вторым атомами углерода. В молекулах
циклической формы такое вращение невозможно.
По этой причине циклическая форма молекул
глюкозы может иметь различное пространственное
строение:
В молекулах
циклической формы такое вращение невозможно.
По этой причине циклическая форма молекул
глюкозы может иметь различное пространственное
строение:
А) — форма глюкозы – гидроксильные группы при первом и втором углеродных атомах расположены по одну сторону кольца молекулы
Б)
— форма глюкозы – гидроксильные
группы находятся по разные стороны
кольца молекулы:
Глюкоза
– бесцветное кристаллическое вещество
со сладким вкусом, хорошо растворимое
в воде. Из водного раствора она
выделяется в виде кристаллогидрата
С6Н12О6Н2О. По сравнению
со свекловичным сахаром она менее сладкая.
О том, что моносахарид глюкоза – необходимый
компонент пищи, один из главных участников
обмена веществ в организме, сейчас знает
каждый. Прежде всего при ее окислении
выделяется больше трети используемой
в организме энергии. Есть и другой важный
энергетический ресурс – жиры, но роль
глюкозы и жиров в энергетике разных органов
различна. Сердце, например, использует
в качестве топлива жирные кислоты – продукт
распада жиров.
Сердце, например, использует
в качестве топлива жирные кислоты – продукт
распада жиров.
Фруктоза (фруктовый сахар) – находится в плодах, ягодах, овощах, меде. Она очень гигроскопична. Сладость ее в 2,2 раза выше сладости глюкозы.
Галактоза – составная часть молочного сахара. Она обладает незначительной сладостью, в свободном виде в природе не встречается.
Манноза
– содержится во фруктах.
Дисахариды (С12Н22О11)n. Особое
значение имеют дисахариды, молекулы которых
построены из двух одинаковых или разных
моноз. Одна из молекул моноз всегда участвует
в построении молекулы дисахарида свом
полуацетальным гидроксилом, другая –
полуацетальным или одним из спиртовых
гидроксилов. Если в образовании молекулы
дисахарида монозы участвуют своими полуацетальными
гидроксилами, образуется невосстанавливающий
дисахарид. В восстанавливающем дисахариде
циклическая форма одного остатка не является
закрепленной, и оставшийся свободным
полуацетальный гидроксил может перейти
таутомерную альдегидную форму.
К дисахаридам относят сахарозу, мальтозу, лактозу, трегалозу. Это белые кристаллические вещества хорошо растворимые в воде, сладкие на вкус. Однако сладость без лишних сахаров не одинакова. Если сладость сахарозы принять за 100, то при одинаковой температуре сладость остальных сахаров составляет: фруктозы – 173, глюкозы – 74, мальтозы и галактозы – 32, лактозы – 16.
Под
действием ферментов  На этом явлении основано
использование в кулинарии «жженки» для
подкрашивания соусов и желе. Сахароза
– это наиболее известный и широко применяемый
в питании и пищевой промышленности сахар.
Содержится в листьях, стеблях, семенах,
плодах, клубнях растений. В сахарной свекле
от 15-22% сахарозы, в сахарном тростнике
12-15%, это основные источники ее получения.
Отсюда же возникли и ее названия – тростниковый
или свекловичный сахар. В картофеле 0,65
сахарозы, луке 6,5%, моркови 3,5%, дыне 5,9%,
абрикосах и персиках 6,0%, апельсинах 3,5%,
винограде 0,5%. Ее содержится сравнительно
много в кленовом соке и кукурузе 1,4-1,8%.
Сахароза кристаллизуется без воды в виде
больших моноклинных кристаллов. Подобно
моносахаридам, ее водные растворы также
способны вращать плоскость поляризации
проходящего через нее плоскополяризованного
луча света. Гидролиз сахарозы сопровождается
образованием глюкозы и фрактозы. Последняя
обладает более сильным вращением (-92*),
чем глюкоза правым (+52,5*), поэтому при гидролизе
сахарозы угол вращения изменяется.
На этом явлении основано
использование в кулинарии «жженки» для
подкрашивания соусов и желе. Сахароза
– это наиболее известный и широко применяемый
в питании и пищевой промышленности сахар.
Содержится в листьях, стеблях, семенах,
плодах, клубнях растений. В сахарной свекле
от 15-22% сахарозы, в сахарном тростнике
12-15%, это основные источники ее получения.
Отсюда же возникли и ее названия – тростниковый
или свекловичный сахар. В картофеле 0,65
сахарозы, луке 6,5%, моркови 3,5%, дыне 5,9%,
абрикосах и персиках 6,0%, апельсинах 3,5%,
винограде 0,5%. Ее содержится сравнительно
много в кленовом соке и кукурузе 1,4-1,8%.
Сахароза кристаллизуется без воды в виде
больших моноклинных кристаллов. Подобно
моносахаридам, ее водные растворы также
способны вращать плоскость поляризации
проходящего через нее плоскополяризованного
луча света. Гидролиз сахарозы сопровождается
образованием глюкозы и фрактозы. Последняя
обладает более сильным вращением (-92*),
чем глюкоза правым (+52,5*), поэтому при гидролизе
сахарозы угол вращения изменяется. Гидролиз
сахарозы получил название «инверсия»,
а смесь образующихся равных количеств
глюкозы и фрактозы – «инвертный сахар»,
или «искусственный мед». Природным инвертным
сахаром является мед, состоящий в основном
из глюкозы и фруктозы. Сахароза после
гидролиза сбраживается дрожжами, а при
нагревании выше температуры плавления
(160-186 С) карамелизуется, т. е. превращается
в смесь сложных продуктов: карамелана,
карамелена и других, теряя при этом воду.
Процесс карамелизации можно выразить
следующей схемой:
Гидролиз
сахарозы получил название «инверсия»,
а смесь образующихся равных количеств
глюкозы и фрактозы – «инвертный сахар»,
или «искусственный мед». Природным инвертным
сахаром является мед, состоящий в основном
из глюкозы и фруктозы. Сахароза после
гидролиза сбраживается дрожжами, а при
нагревании выше температуры плавления
(160-186 С) карамелизуется, т. е. превращается
в смесь сложных продуктов: карамелана,
карамелена и других, теряя при этом воду.
Процесс карамелизации можно выразить
следующей схемой:
С12Н22О11 → С6Н12О6 + Н2О
Все
эти продукты темно – бурого цвета
под названием «колер»
Открытие углеводов — Справочник химика 21
Для открытия углеводов в биологическом материале иногда пользуются их способностью образовывать с концентрированной серной кислотой фурфурол, дающий фиолето- [c. 19]
19]Область применения. Пентозы, гексозы и их ангидриды при действии концентрированной серной кис юты образуют фурфурол или его производные. Эти альдегиды дают окрашенные продукты конденсации с а-нафтолом. Предел идентификации 10—50 у. Реакция часто используется для открытия углеводов. [c.395]
Когда было сделано открытие о способности микроорганизмов усваивать углеводы нефти и когда микробиологическая промышленность стала самостоятельной отраслью народного хозяйства [c.285]
Углеводы состоят всего из трех элементов — углерода, водорода и кислорода. В течение всей жизни в человеческом организме постоянно происходит превращение углеводов в СОз и Н2О, сопровождающееся выделением энергии. Например, глюкоза — основной поставщик энергии человеческого организма — имеет формулу С Н,20 . Сначала, когда это вещество было только открыто, его формулу записывали так С (Н20) , т. е. в виде комбинации углерода и воды. Отсюда и происхождение названия углевод . Хотя теперь мы знаем, что на самом деле никаких молекул воды в углеводах нет, название сохранилось. [c.244]
е. в виде комбинации углерода и воды. Отсюда и происхождение названия углевод . Хотя теперь мы знаем, что на самом деле никаких молекул воды в углеводах нет, название сохранилось. [c.244]
Гликоген. Этот углевод, открытый Клодом Бернаром (1857) в печени, является резервным питательным веществом организма животных. Особенно богата им печень высших и низших животных ( печеночный крахмал ), но он широко распространен также в мускульной ткани и во многих других клетках. Во время работы мышц содержание в них гликогена уменьшается углевод при этом разрушается до молочной кислоты. [c.456]
К. Бауэр. Анализ органических соединений. Издатинлит, 1953, (488 стр.), В книге содержится описание методов открытия, идентификации и количественного определения важнейших классов и отдельных представителей органических соединений углеводородов, галогенопроизводных, спиртов, фенолов, эфиров, нитропроизводных, аминов, альдегидов, кетонов, кислот, углеводов, жиров, алкалоидов и др. По каждому классу дан обзор общих групповых реакций и описаны специфические методы открытия и количественного определения главных представителей класса. Каждая глава снабжена списком литературы. [c.492]
По каждому классу дан обзор общих групповых реакций и описаны специфические методы открытия и количественного определения главных представителей класса. Каждая глава снабжена списком литературы. [c.492]
Такое объяснение опыта Велера удерживалось в науке еще около 30 лет, но в течение этого периода оно постепенно подтачивалось открытием все новых и новых возможностей перехода от минеральных веществ к органическим . Окончательный удар витализму был нанесен искусственным получением жиров (Бертло, 1854 г.) и углеводов (А. М. Бутлеров, 1861 г.), т. е. веществ, которые уже ни с какой натяжкой нельзя было отнести к разряду мертвых отбросов живых организмов. Можно ручаться эа возможность синтетического получения каждого органического вещества ,— писал А. М. Бутлеров в 1864 г. [c.543]
В литературе, посвященной углеводам, можно встретить утверждения, что наука, быть может, находится на пороге углеводного бума , когда в этой области будут сделаны открытия, не уступающие по своей значимости открытиям 50-х годов, связанным с выяснением биохимической роли нуклеиновых кислот. [c.305]
[c.305]
Указанные ранее сопряженные, последовательные и параллельные химические реакции также протекают в открытых системах, но особенно типичными для них являются многоступенчатые изменения, происходящие в виде циклов биохимических реакций, как, например, цикла трикарбоновых кислот при обмене углеводов и жиров или цикла Кребса при синтезе мочевины и др. При обмене веществ протекают процессы линейного, разветвленного и циклического характера, которые принципиально отличны по химической кинетике от простых цепных реакций. Нужно учитывать, что в отличие от постоянного повторения однотипного процесса, наблюдающегося в цепных реакциях, в биологических процессах почти каждая молекула может быть вовлечена в несколько различных реакций. Выбор пути химических превращений, по которому пойдет каждая молекула, в значительной степени является случайным. [c.94]
Циклическая структура глюкозы. Хотя для обозначения простых углеводов часто удобно пользоваться формулами с открытыми цепями, более корректно изображать структуры пентоз и гексоз в виде циклов, где карбонильная функция превращается в полуацетальную (разд. 7.1.4,А) в результате соединения с одной из гидроксильных групп в той же молекуле. Обычно таким путем образуются только пяти- и шестичленные циклы, называемые фуранозной и пиранозной структурами в соответствии с названиями родоначальных гетероциклических соединений — фурана и пирана. [c.265]
Хотя для обозначения простых углеводов часто удобно пользоваться формулами с открытыми цепями, более корректно изображать структуры пентоз и гексоз в виде циклов, где карбонильная функция превращается в полуацетальную (разд. 7.1.4,А) в результате соединения с одной из гидроксильных групп в той же молекуле. Обычно таким путем образуются только пяти- и шестичленные циклы, называемые фуранозной и пиранозной структурами в соответствии с названиями родоначальных гетероциклических соединений — фурана и пирана. [c.265]
Фенилозазоны. — Успешное развитие химии сахаров тормозилось трудностью получения кристаллических производных углеводов, так как сахара, особенно не очень чистые, имеют тенденцию образовывать некристаллизующиеся сиропы. Одним из выдающихся вкладов Э. Фишера в химию углеводов было внедрение в 1884 г. в лабораторную практику фенилгидразина, который реагирует со многими карбонильными соединениями, даная малорастворимые и хорошо кристаллизующиеся производные.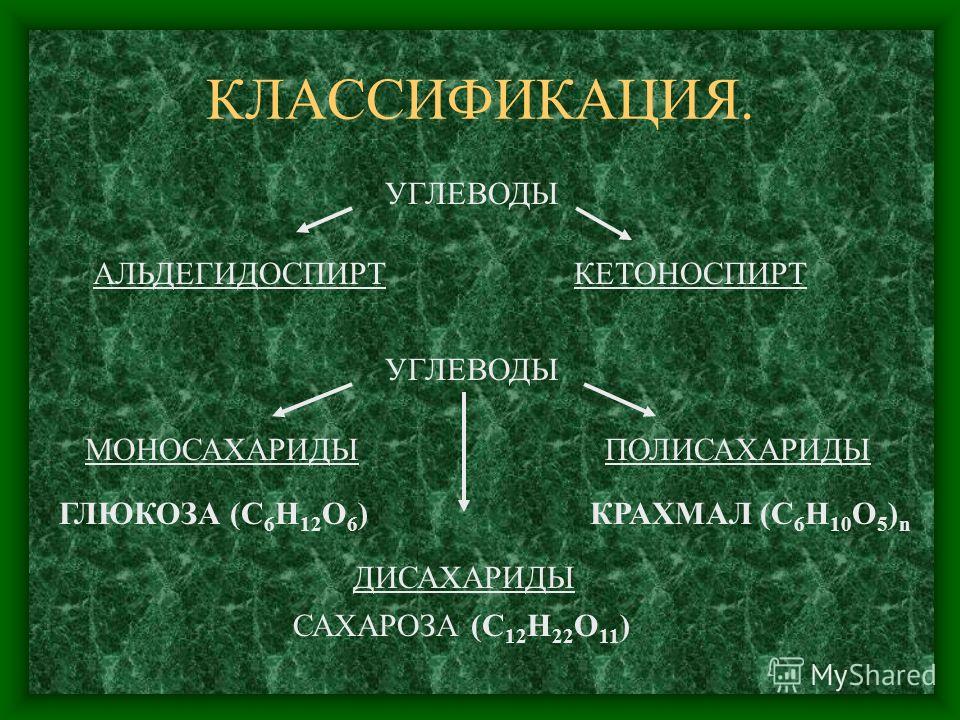 В докторской диссертации Э. Фишера, выполненной десятью годами ранее в Страсбурге под руководством Байера, было описано открытие, синтез и применение фенилгидразина. [c.534]
В докторской диссертации Э. Фишера, выполненной десятью годами ранее в Страсбурге под руководством Байера, было описано открытие, синтез и применение фенилгидразина. [c.534]
I Построение и запись проекционных формул Фишера можно выполнить еще и по-другому. Прежде всего за счет вращения вокруг простых связей С—С молекуле углевода придают заслоненную конформацию в виде буквы С . Открытый конец этой клешни ориентируют так, чтобы он был удален от наблюдателя, и видимую [c.232]
Сахара в морской воде представлены в основном полисахаридами, содержание которых в водах шельфовой зоны часто превосходит 500 мкг С/л. На долю моносахаридов (глюкозы и фруктозы) приходится 10-30 % общего содержания углеводов. Их концентрации в водах открытого океана находятся на уровне 5-10 мкг С/л. [c.30]
Углеводы представляют большой класс сложных органических соединений, СОСТОЯШ.ИХ, как правило, из углерода, водорода и кислорода. Название углеводы было дано им потому, что большинство из них отвечает составу Сп(Н20) ,и в то время, когда были выделены первые представители этого класса, они рассматривались как соединения углерода и воды, так как структурной теории тогда еще не существовало. Это историческое название сохранилось и до наших дней. Углеводы как химически индивидуальные вещества известны с глубокой древности. Один из важнейших углеводов — тростниковый сахар (сахароза) хорошо знали в древней Индии, Китае и Египте. Тростниковый сахар является, по-видимому, первым органическим веществом, полученным человеком в чистом виде. Выращивание сахарного тростника и выделение из него сахара относятся к числу самых древних сельскохозяйственных процессов. Значительно позднее были выделены другие представители углеводов. Так, фруктоза была получена из меда Ловицем в 1792 г., глюкоза — Пру в 1802 г. В 1811 г. Кирхгоф впервые осуществил гидролиз крахмала, открыв тем самым класс полисахаридов. Это открытие позднее послужило основой важнейшего процесса, ставшего краеугольным камнем современной гидролизной промышленности. [c.7]
Это историческое название сохранилось и до наших дней. Углеводы как химически индивидуальные вещества известны с глубокой древности. Один из важнейших углеводов — тростниковый сахар (сахароза) хорошо знали в древней Индии, Китае и Египте. Тростниковый сахар является, по-видимому, первым органическим веществом, полученным человеком в чистом виде. Выращивание сахарного тростника и выделение из него сахара относятся к числу самых древних сельскохозяйственных процессов. Значительно позднее были выделены другие представители углеводов. Так, фруктоза была получена из меда Ловицем в 1792 г., глюкоза — Пру в 1802 г. В 1811 г. Кирхгоф впервые осуществил гидролиз крахмала, открыв тем самым класс полисахаридов. Это открытие позднее послужило основой важнейшего процесса, ставшего краеугольным камнем современной гидролизной промышленности. [c.7]
Предположения о циклической полуацетальной формуле моносахаридов и о таутомерии между открытой и циклической формами удовлетворительно объяснили все факты химии углеводов и были вскоре приняты. Однако совершенно невыясненным оставался вопрос о размере окисного кольца, которое Толленс из общих соображений об устойчивости пятичленных циклов принял за -окисное. В действительности альдегидная группа моносахарида может реагировать с любой из имеющихся пяти гидроксильных групп с образованием полуацеталя. В этом случае структура моносахарида на примере альдогексоз изображается одной из формул (III—VII). [c.32]
Однако совершенно невыясненным оставался вопрос о размере окисного кольца, которое Толленс из общих соображений об устойчивости пятичленных циклов принял за -окисное. В действительности альдегидная группа моносахарида может реагировать с любой из имеющихся пяти гидроксильных групп с образованием полуацеталя. В этом случае структура моносахарида на примере альдогексоз изображается одной из формул (III—VII). [c.32]
Конформационные изомеры, которые могут быть приняты в расчет при рассмотрении структуры углеводов, относятся, очевидно, только к пиранозам. Для фуранозных структур, имеющих жесткий пятичленный цикл, существование заметно отличающихся конформаций невозможно. С другой стороны, открытые альдегидные формы моносахаридов могут существовать в виде большого числа конформационных изомеров, мало отличающихся один от другого энергетически, и анализ реакционной способности отдельных связей теряет в этом случае смысл. [c.50]
В молекуле ДНК углевод представлен дезоксирибозой, а в молекуле РНК-рибозой, отсюда их названия дезоксирибонуклеиновая (ДНК) и рибонуклеиновая (РНК) кислоты.
 Кроме того, они содержат фосфорную кислоту, по два пуриновых и по два пиримидиновых основания различия только в пиримидиновых основаниях в ДНК содержится тимин, а в РНК -урацил. В составе ДНК и РНК открыты так называемые минорные [c.97]
Кроме того, они содержат фосфорную кислоту, по два пуриновых и по два пиримидиновых основания различия только в пиримидиновых основаниях в ДНК содержится тимин, а в РНК -урацил. В составе ДНК и РНК открыты так называемые минорные [c.97]Открытие углеводов (моно- и дисахаридов). Углеводы бесцветны, хорошо растворимы в воде, нейтральны. Их легко открывают по присутствию альдегидной, кетонной и гидроксильной групп. Эти группы открывают вышеописанными реакциями. Кроме того, углеводы оптически активные соединения угол вращения можно измерить с помощью поляриметра. [c.126]
Сравнительно недавно были сформулированы Н. А. Васюниной А. А. Баландиным и Р. Л. Слуцкиным положения о системе катализаторов, действующих при гидрогенолизе углеводов и много атомных спиртов [52, 53], — о гомогенном катализаторе разрыва связи С—С (крекирующем агенте) и гетерогенном катализатор гидрогенизации. В то же время было открыто каталитическое дей ствие в этой реакции растворимых соединений металлов, наприме сульфата железа, хелатного комплекса железа с сахарными кисло тами, сульфата цинка и др. , названных гомогенными сокатализа торами гидрогеиолиза [54, 55]. Механизм их действия рассмотре в гл. 3 добавление гомогенных сокатализаторов ускоряет гидроге нолиз в 2—3 раза с получением гидрогенизата примерно таког( же состава, как и без их применения. [c.122]
, названных гомогенными сокатализа торами гидрогеиолиза [54, 55]. Механизм их действия рассмотре в гл. 3 добавление гомогенных сокатализаторов ускоряет гидроге нолиз в 2—3 раза с получением гидрогенизата примерно таког( же состава, как и без их применения. [c.122]
Н. Д. Зелинский назвал открытый им процесс избирательным катализом , поскольку алканы, а также цикланы, кроме гексагидроаромати-ческих, нанример нятичленные, в этих условиях дегидрогенизации не подвергаются. Как было показано Н. Д. Зелинским и его школой на многочисленных примерах, даже сложные углеводороды, если они содержат в молекуле гексагидроароматическое кольцо, претерпевают дегидрогенизацию в образованием соответственного углевод(5рода с ароматическим ядром. [c.501]
В первой стадии процесса брожения, так называемой затравке , большую роль играет открытый Гарденом и Юнгом зимофосфат . Этот эфир Гардена — Юнга представляет собой 1,6-дифосфат фрукто-фуранозы (относительно названий см. главу об углеводах). Его предшественниками, вероятно, являются два монофосфорных эфира так называемый эфир Робинсона (6-фосфат глюкопираыозы) и эфир Ней-берга (6-фосфат фруктофуранозы). Кроме того, присутствует также 6-фоефат маннозы. [c.120]
главу об углеводах). Его предшественниками, вероятно, являются два монофосфорных эфира так называемый эфир Робинсона (6-фосфат глюкопираыозы) и эфир Ней-берга (6-фосфат фруктофуранозы). Кроме того, присутствует также 6-фоефат маннозы. [c.120]
В 1888 г. Фаворский синтезировал метилвинилэтиловый эфир 17],, и этим открытием было положено начало развития химии виниловых соединений. Классическая реакция Фаворского основана на взаимодействии спиртов с ацетиленом в присутствии едкого калия. В 1940 г. Фаворский и Шостаковский [8] теоретически обосновали и экспериментально доказали целесообразность работы с ацетиленом под давлением и три повышенных температурах. Ацетилен хорошо растворяется в виниловых эфирах, а благодаря большей коицен-трации ацетилена ускоряется винилирование. Установлено, что реакция протекает успешно при 140—160 . Берут 5—10% КОН от исходного спирта, начальное давление ацетилена 14—15 атм. Выход алкилвиниловых эфиров достигает 95%. Винилирование распространилось на спирты, гликоли, глицерин, фенолы, циклические спирты, аминоспирты, углеводы, оксикислоты и другие соединения. [c.21]
[c.21]
Конфигурация асимметрического центра не являе-гся абсолютно жесткой. Многие оптические изомеры, предоставленные сами себе, постепенно претерпевают ауторацемизацию, превращаясь в смесь оптических антиподов. Особенно склонны к реакции рацемизации углеводы. Здесь она осложнена влиянием других асимметрических центров молекулы, поэтому состояние равновесия обычно не достигает соотношения 1 1. Если динамическая стереоизомерия затрагивает первый углеродный атом молекулы углевода, то говорят об йномеризации, которая протекает через открытую аль-форму [c.112]
За свою более чем полуторавековую историю структурная химия достигла поистине поразительных результатов. Уст 1-новлено строение и открыты пути синтеза сложнейших природных соединений — терпенов, углеводов, пептидов п белков, нуклеиновых мислот, стероидов, антибиотиков, витаминов и коферментов, алкалоидов. Созданы научные основы препаративного органического синтеза самых разнообразных соединений. И, конечно, все эти успехи вовсе не означают того, что структурная химия достигла потолка. Нет, дальнейшие перспективы ее развития безграничны. Они состоят в поисках новых зависимостей между валентностью (реакционной способностью) свободных атомов и структурой образуемых из них частиц, новых корреляций между различными видами химических связей в результате более эффективных методов количественного обсчета многоэлектронных систем, в установлении новых форм химических соединений типа ферроцена, бульвалена, В севоэмож)Ных элементоорганических соединений, в частности фто-руглеродов и их производных. [c.100]
И, конечно, все эти успехи вовсе не означают того, что структурная химия достигла потолка. Нет, дальнейшие перспективы ее развития безграничны. Они состоят в поисках новых зависимостей между валентностью (реакционной способностью) свободных атомов и структурой образуемых из них частиц, новых корреляций между различными видами химических связей в результате более эффективных методов количественного обсчета многоэлектронных систем, в установлении новых форм химических соединений типа ферроцена, бульвалена, В севоэмож)Ных элементоорганических соединений, в частности фто-руглеродов и их производных. [c.100]
Перегруппировка открыта К. Фрисом в 1908. ФРУКТОЗА (плодовый, нли фруктовый, сахар левулоза), моносахарид сладкого вкуса (слаще сахарозы в 1,5 раза). В природе распростр. В-Ф. для ее (3-аномера (ф-ла I) illл 102—104 °С, 1а]п —132°, равновесное [а]п —93°. Содержится в спелых фруктах, меде структурный фрагмент олигоса-харидов (напр., сахарозы и раффинозы), полисахаридов (напр.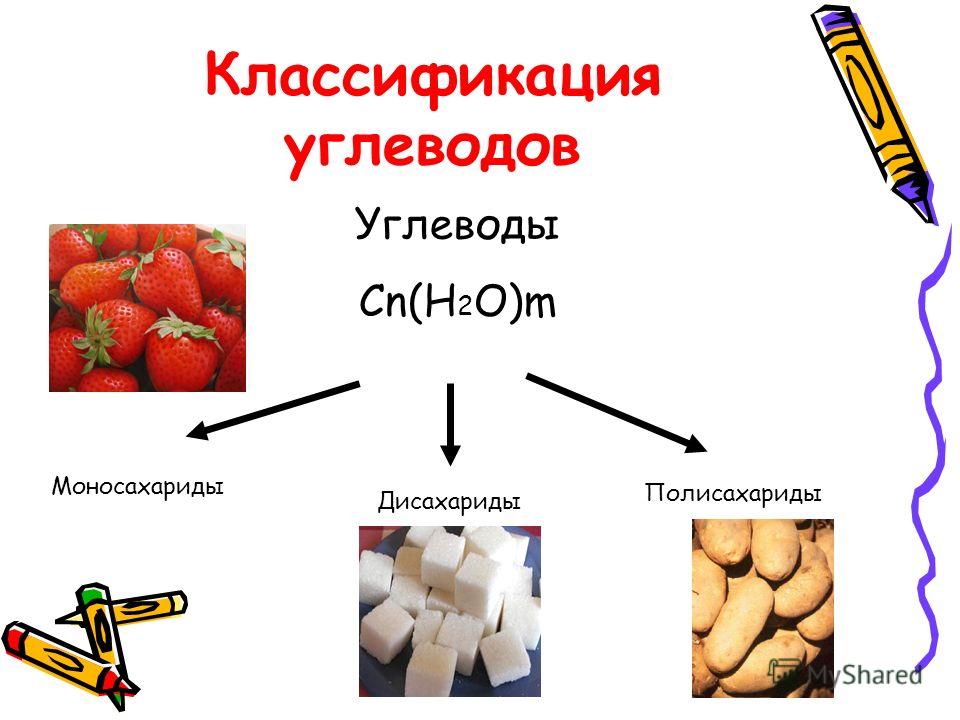 , инулина). Фосфаты Ф. — промежут. соед. в энергетич. обмене углеводов. Получ. мягким кислотным или ферментативным гидролизом сахарозы или фрук-танов. Усиаивается больными диабетом лучше, чем глюкоза. [c.635]
, инулина). Фосфаты Ф. — промежут. соед. в энергетич. обмене углеводов. Получ. мягким кислотным или ферментативным гидролизом сахарозы или фрук-танов. Усиаивается больными диабетом лучше, чем глюкоза. [c.635]
В модификациях B. . в качестве алкилирующих агентов применяют диалкилсульфаты, что особенно удобно для алкилирования реакционноспособных спиртов (напр., бензилового, аллилового, коричного), углеводов и фенолов. Из др. алкилирующих агентов используют эфиры муравьиной к-ты, ортоэфиры и эфиры арил- и алкилсульфокислот, соли триалкилоксония. Для алкилирования гидроксикислот применяют алкилиодиды в присут. AgjO или ВаО. Удобный метод синтеза PhOR-алкилирование фенолов в р-ре ацетона в присут. поташа (этот синтез наз. р-цией Клайзена). Р-ция открыта А. Вильямсоном в 1851. [c.368]
Работами Дж. Гиббса, Вант-Гоффа, В. Нернста и др. создается химическая термодинамика. Исследования электропроводности р-ров и электролиза привели к открытию электролитич. диссоциации (С. Аррениус, 1887). В это же году Оствалвд и Вант-Гофф основали первый журнал, посвященный физической химии, и она оформилась как самостоятельная дисциплина. К сер. 19 в. принято относить зарождение агрохимии и биохимии, особенно в связи с пионерскими работами Либиха (1840-е гг.) по изучению ферментов, белков и углеводов. [c.259]
диссоциации (С. Аррениус, 1887). В это же году Оствалвд и Вант-Гофф основали первый журнал, посвященный физической химии, и она оформилась как самостоятельная дисциплина. К сер. 19 в. принято относить зарождение агрохимии и биохимии, особенно в связи с пионерскими работами Либиха (1840-е гг.) по изучению ферментов, белков и углеводов. [c.259]
Вклад в развитие конформаиноиного анализа и его применение в органической химии Открытие роли нуклеотидов в биоснитезе углеводов [c.776]
Но позднее были открыты и такие сахара, которые оказались исключением из правила. Так, явный представитель углеводов рамиоза (она тоже дает реакцию Молиша) имеет формулу СбН)205. И хотя неточность в названии целого класса соединений была очевидной, термин «углеводы» стал уже настолько привычным, что его не стали менять. Впрочем, в наши дни многие химики предпочитают иное название — «сахара». [c.58]
Весь изложенный выше материал по химии моносахаридов основывался на предложенных Э. Фишером оксикарбонильных формулах моносахаридов с открытой цепью углеродных атомов. Несмотря на то, что значительное число реакций моносахаридов удовлетворительно объясняется этими формулами, имелись противоречащие им факты, которые уже в период работ Фишера ждали объяснения, и поэтому одновременно с оксикар бонильными формулами для моносахаридов были предложены другие формулы (Колли, Толленс). Следующие экспериментальные данные не согласовывались с фишеровскими формулами углеводов. [c.30]
Фишером оксикарбонильных формулах моносахаридов с открытой цепью углеродных атомов. Несмотря на то, что значительное число реакций моносахаридов удовлетворительно объясняется этими формулами, имелись противоречащие им факты, которые уже в период работ Фишера ждали объяснения, и поэтому одновременно с оксикар бонильными формулами для моносахаридов были предложены другие формулы (Колли, Толленс). Следующие экспериментальные данные не согласовывались с фишеровскими формулами углеводов. [c.30]
Однако последнее, а именно, доказательство открытой формы гликозиламина, по некоторым данным недостаточно убедительно. Оказалось, что полные ацетаты альдегидных форм моносахаридов ( XLI) при взаимодействии с ароматическими аминами в присутствии спирта (т. е. в условиях, соответствующих образованию N- гликозидов, поскольку углевод, имеющий свободные гидроксильные группы, сам играет роль спирта) образуют не истинные шиффовы основания, а соединения типа (XLII). [c.133]
До сих шор вое эти реакции шли с хорошими выходами, но далее начались осложнения. Окислением диена (III) четырехокисью осмия он получил тетраол (IV) с выходом 10—13%, но уже с нужной конфигурацией. Далее он действовал йодной кислотой, и так же как при синтезе по Суворову (стр. 359), подобрал такие условия, что отщеплялся только один углеродный атом. Таким образом, было получено соединение (V) с боковой цепью, но на первый взгляд не той, которая нужна. Здесь Рейхштейн использовал известную перегруп1шровку глицеринового альдегида в диоксиацетон, которая была открыта в 90-х годах прошлого столетия Лобри де Брюином в ряду углеводов Действительно, при нагревании в пиридине соединение (V) было превращено в вещество S (IV) с выходом 30%. Общий выход вещества S, считая на дегидроэпиандростерон, составил 1,8%, что даже в лабораторных условиях неприемлемо. [c.361]
Окислением диена (III) четырехокисью осмия он получил тетраол (IV) с выходом 10—13%, но уже с нужной конфигурацией. Далее он действовал йодной кислотой, и так же как при синтезе по Суворову (стр. 359), подобрал такие условия, что отщеплялся только один углеродный атом. Таким образом, было получено соединение (V) с боковой цепью, но на первый взгляд не той, которая нужна. Здесь Рейхштейн использовал известную перегруп1шровку глицеринового альдегида в диоксиацетон, которая была открыта в 90-х годах прошлого столетия Лобри де Брюином в ряду углеводов Действительно, при нагревании в пиридине соединение (V) было превращено в вещество S (IV) с выходом 30%. Общий выход вещества S, считая на дегидроэпиандростерон, составил 1,8%, что даже в лабораторных условиях неприемлемо. [c.361]
Подобно другим соединениям, содержащим две или более групп ОН или =0 при соседних атомах углерода, углеводы подвергаются окислительному расщеплению йодной кислотой (разд. 28.6). Эта реакция, открытая в 1928 г. Л. Малапраде (университет в Нанси, Франция), является одним из наиболее важных методов в современных исследованиях структуры углеводов. [c.937]
Л. Малапраде (университет в Нанси, Франция), является одним из наиболее важных методов в современных исследованиях структуры углеводов. [c.937]
С середины XVIII в. начинается период открытия и вьщеления большого числа новых органических веществ растительного и животного происхождения. Крупным событием второй половины XVIII в. стали исследования Л. Спалланцани по физиологии пищеварения, которые положили начало изучению ферментов пищеварительных соков. Русский химик К.С. Кирхгоф в 1814 г. описал ферментативный процесс осахаривания крахмала под влиянием вытяжки из проросших семян ячменя. К середине XIX в. были найдены и другие ферменты амилаза слюны, пепсин желудочного сока, трипсин сока поджелудочной железы. Й. Берцелиус ввел в химию понятие о катализе и катализаторах, к числу последних были отнесены все известные в то время ферменты. В 1839 г. Ю. Либих выяснил, что в состав пищи входят белки, жиры и углеводы, являющиеся главными составными частями животных и растительных организмов. [c.16]
[c.16]
Пуклеопротеины состоят из белков и нуклеиновых кислот. Последние рассматриваются как простетические группы. В природе обнаружено 2 типа нуклеопротеинов, отличающихся друг от друга по составу, размерам и физико-химическим свойствам,— дезоксирибонуклеопротеины (ДНП) и рибонуклеопротеины (РНН). Названия нуклеопротеинов отражают только природу углеводного компонента (пентозы), входящего в состав нуклеиновых кислот. У РНП углевод представлен рибозой, у ДНП—дезоксирибозой. Термин пуклеопротеины связан с названием ядра клетки, однако ДНП и РНП содержатся и в других субклеточных структурах. Следовательно, речь идет о химически индивидуальном классе органических веществ, имеющих своеобразные состав, структуру и функции независимо от локализации в клетке. Доказано, что ДНП преимущественно локализованы в ядре, а РНП —в цитоплазме. В то же время ДНП открыты в митохондриях, а в ядрах и ядрышках обнаружены также высокомолекулярные РНП. [c.86]
Открытие пути прямого окисления углеводов, или, как его называют, пентозофосфатного цикла, принадлежит О. Варбургу, Ф. Липману, Ф. Дикенсу и В.А. Энгельгарду. Расхождение путей окисления углеводов—классического (цикл трикарбоновых кислот, или цикл Кребса) и пентозофосфатного—начинается со стадии образования гексозомонофосфата. Если глюкозо-6-фосфат изомеризуется во фруктозо-6-фосфат, который фосфорилируется второй раз и превращается во фруктозо-1,6-бисфосфат, то в этом случае дальнейший распад углеводов происходит по обычному гликолитическому пути с образованием пировиноградной кислоты, которая, окисляясь до ацетил-КоА, затем сгорает в цикле Кребса. [c.353]
Варбургу, Ф. Липману, Ф. Дикенсу и В.А. Энгельгарду. Расхождение путей окисления углеводов—классического (цикл трикарбоновых кислот, или цикл Кребса) и пентозофосфатного—начинается со стадии образования гексозомонофосфата. Если глюкозо-6-фосфат изомеризуется во фруктозо-6-фосфат, который фосфорилируется второй раз и превращается во фруктозо-1,6-бисфосфат, то в этом случае дальнейший распад углеводов происходит по обычному гликолитическому пути с образованием пировиноградной кислоты, которая, окисляясь до ацетил-КоА, затем сгорает в цикле Кребса. [c.353]
Углеводы. История открытия углеводов. Полисахариды. Сложные эфиры целлюлозы
Конечно, организм получает не все 49,5 кДж, а только 30,6 кДж. Но и это не мало.
Второе
соединение с высокоэнергетической связью — фосфоенолпируват. В его молекуле
неустойчива связь между фосфатной и гидроксильной группами. При гидролизе этой
связи на один моль фосфоенолпирувата выделяется 62,1 кДж (14,8 ккал) свободной
энергии. Она используется для синтеза ещё одного моля АТФ.
Она используется для синтеза ещё одного моля АТФ.
Займёмся теперь математикой; из каждой молекулы глюкозы получаются две молекулы 1,3-дифосфоглицериновой кислоты и потом две молекулы фосфоенолпирувата. Каждая из получившихся молекул даёт одну молекулу АТФ. Значит, при расщеплении одной молекулы глюкозы образуется четыре молекулы АТФ. Но это не «чистый» выход АТФ. Дело в том, что на некоторых стадиях гликолиза клетке требуется энергия, и, чтобы её получить, она вынуждена расщеп
В основе фосфоенолпирувата — молекула пировиноградной кислоты. В ней —
три углеродных атома. Атом с номером 1 входит в карбоксильную группу, атом с
номером 2 — в карбонильную группу, атом с номером 3 — в метильную. В центре
молекулы расположена карбонильная группа, которая связана как с метильной, так
и с карбоксильной. Карбоксильная группа легко теряет ион водорода. В результате
образуется отрицательно заряженный ион, который называется пируватом. Он может
существовать и в другой форме. Между вторым и третьим атомами углерода
возникает двойная связь, а на месте карбонильной группы появляется атом
углерода, связанный с гидроксильной группой. Такая молекула получила название
енолпируват. Наконец, соединение, в котором гидроксильная группа связана с
фосфатной группой, — это фосфоенолпируват.
Он может
существовать и в другой форме. Между вторым и третьим атомами углерода
возникает двойная связь, а на месте карбонильной группы появляется атом
углерода, связанный с гидроксильной группой. Такая молекула получила название
енолпируват. Наконец, соединение, в котором гидроксильная группа связана с
фосфатной группой, — это фосфоенолпируват.
В
основе молекулы 1,3-дифосфоглицериновой кислоты лежит глицерин, у которого
имеются три атома углерода. Каждый из них связан с гилроксильной группой. Если
окислить одну из СН2ОН-групп, получится карбоксильная группа —СООН.
Такое соединение называется глицериновой кислотой. У неё одна карбоксильная и
две гидроксильные группы, а атомов углерода, как и у глицерина, три. Они
нумеруются, начиная с того атома углерода, который входит в состав
карбоксильной группы. Он получает номер 1, а атомы, связанные с гидроксильными
группами — номера 2 и 3. Карбоксильная и гидроксильная группы могут
образовывать эфирную связь (через атом кислорода) с фосфатными группами. Так и
происходит в
1,3-дифосфоглицериновой кислоте. В этой молекуле — две фосфатные группы. Одна
связана с карбоксильной группой, а другая — с гидроксильной при атоме углерода
с номером 3. Отсюда и цифры в названии кислоты — 1,3.
Так и
происходит в
1,3-дифосфоглицериновой кислоте. В этой молекуле — две фосфатные группы. Одна
связана с карбоксильной группой, а другая — с гидроксильной при атоме углерода
с номером 3. Отсюда и цифры в названии кислоты — 1,3.
526
ЧТО ТАКОЕ НАД
Молекула НАД состоит из двух нуклеотидов. Один из них содержит основание аденин, присутствующее в нуклеотидах ДНК, а другой — положительно заряженное соединение никотинамид, который и определяет способность НАД быть аккумулятором электронов. Никотинамид может приобретать два электрона в некоторых окислительно-восстановительных реакциях, которые протекают в организме. Условно можно представить, что НАД реагирует с двумя атомами водорода. Каждый такой атом имеет по одному электрону. Один атом водорода никотинамид забирает к себе полностью, а другой отпускает, предварительно отобрав у него электрон. В итоге никотинамид получает два электрона:
НАД++2Н®НАД•Н+Н+.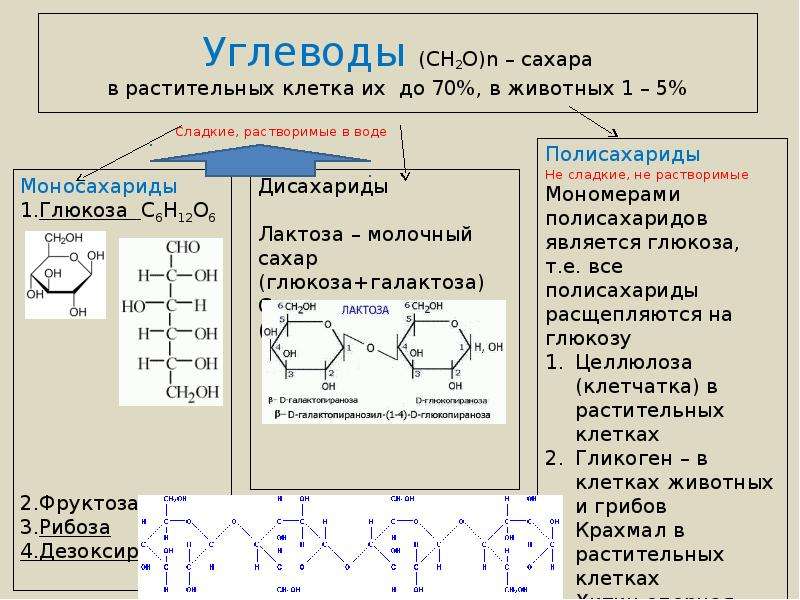
На самом деле, НАД, конечно же, вступает в реакцию не с атомами водорода. Вот как, например, протекает реакция окисления альдегидной группы до карбоксильной:
В этой реакции атом водорода, который присоединяется к НАД, поступает из альдегидной группы, а ион водорода — из воды.
В других реакциях НАД•Н, наоборот, отдаёт пару электронов. Например, при восстановлении карбонильной группыдо группы НАД•Н теряет атом водорода, а из окружающей среды поглощается ион водорода:
лять АТФ. Для превращения одной молекулы глюкозы нужна энергия двух молекул АТФ. Получается, что «чистый» выход АТФ в результате гликолиза равен двум
История
При открытии Московского университета в 1755 году к числу предметов, изучаемых на факультете, была добавлена «химия с применением химии аптекарской». Половина других предметов университетского курса определилось на много лет вперед – химия была отдана на службу медицине». Студентов обучали «физической особливо, химии аптекарской и приложениям химии к медицине».
Студентов обучали «физической особливо, химии аптекарской и приложениям химии к медицине».
На медицинском факультете предусматривалась должность доктора и профессора химии. Устанавливалось, что профессором химии должен быть доктор медицины, т.к. это было во всех университетах Европы в то время.
Первым профессором химии в Московском университете (1758-1770 гг.) был доктор медицины и магистр философии И.Х. Карстенс. При И.Х. Карстенсе в университете была устроена первая химическая лаборатория (1760 г). В период с 1770 по 1804 год кафедрой химии и практической медициной заведовали П.П. Вениаминов (1770-1775), С.Г. Зебелин (1775-1802) и С.Г. Политковский (1802-1804).
В начале XIX века кафедра химии была передана в административное подчинение факультета физических и математических наук.
В 1804 г. кафедру возглавил доктор медицины Фердинанд-Фридрих Рейсс, который не ограничивал свою деятельность учебными и административными обязанностями, уделяя большое внимание систематической научно-исследовательской работе.
Ф.Ф. Рейсс известен открытием в 1808 г. явления электрофореза. Ему принадлежит оригинальная по тому времени мысль получения искусственных минеральных вод.
Несомненной заслугой Ф.Ф. Рейсс является постройка химической лаборатории после пожара Москвы в 1812г. Постройка лаборатории была закончена в 1823 г.
Будучи членом и, с 1822 года, председателем физико-медицинского общества Рейсс поместил в его «Актах» («Commentationes») целый ряд статей и исследований; из них наиболее крупные: в I томе:«Описание химических действий гальванического электричества», «Theoremata de miasmatum contagiosorum origine, natura, proprietatibus et agendi modo»; во II томе: «Опыты, относящиеся к фармации», «Наблюдения над различными лекарствами», «Физико-химические опыты над животным магнетизмом», «О водогонной силе гальванического электричества, открытой Рейссом и об участии её в различных явлениях природы», «Анатомо-физиологическое исследование сил, движущих кровь, которыми доказывается, что главная из них есть водогонная сила электричества», «О действии различных средств, особенно растения Scutellaria laterifolia против водобоязни». В издаваемых тем же обществом «Bulletin de la Société Physico-Médical» (1830) были помещены следующие статьи Рейсса: «Замечания относительно того, что врачам следовало бы к своим метеорологическим наблюдениям присоединять и геологические», «Наблюдения над средством Cadet de Vaux против ломоты и ревматизма», «Замечания об изумительном действии сернокислой меди в крупе» и «Замечания о болезни: asthma acutum periodicum Millari». Отдельно были изданы: «Nouvelle analyse du principe febrifuge du quinquina» (M., 1810; перепечатано в «Записках Физико-Медицинского Общества» во II томе), «Наставление как употреблять средство, предохраняющее от моровой язвы и других заразительных болезней» (1807; «De incendiis spontaneis eorumque legibus et causis oratio» (1808), «De stadiorum Academicorum rectius instituendorum, prosperius celebrandorum et felicius absolvendorum ratione» (1809), «Memoria coronationis et sacrae unctionis Imperatoris ac domini nostri Nicolai primi» (1827) и «Об употреблении хлора для предохранения от холеры» (1830).
В издаваемых тем же обществом «Bulletin de la Société Physico-Médical» (1830) были помещены следующие статьи Рейсса: «Замечания относительно того, что врачам следовало бы к своим метеорологическим наблюдениям присоединять и геологические», «Наблюдения над средством Cadet de Vaux против ломоты и ревматизма», «Замечания об изумительном действии сернокислой меди в крупе» и «Замечания о болезни: asthma acutum periodicum Millari». Отдельно были изданы: «Nouvelle analyse du principe febrifuge du quinquina» (M., 1810; перепечатано в «Записках Физико-Медицинского Общества» во II томе), «Наставление как употреблять средство, предохраняющее от моровой язвы и других заразительных болезней» (1807; «De incendiis spontaneis eorumque legibus et causis oratio» (1808), «De stadiorum Academicorum rectius instituendorum, prosperius celebrandorum et felicius absolvendorum ratione» (1809), «Memoria coronationis et sacrae unctionis Imperatoris ac domini nostri Nicolai primi» (1827) и «Об употреблении хлора для предохранения от холеры» (1830).
В последующие годы кафедрой заведовал Р.Г. Гейман (1832-1854), назначенный 17 сентября 1832 года преподавателем химии в Московском университете на место профессора Рейсса; 28 марта 1833 года утверждён ординарным профессором при университете, а 18 июля того же года — и при академии. Добился в 1834 году постройки, по разработанному им плану, нового здания химической лаборатории Московского университета, считавшейся в то время одной из лучших в Европе.
Ввёл в научный оборот термин «техническая химия» и в период 1836—1854 годов читал составленный им публичный курс московским фабрикантам.
В 1841 году, путешествуя по Германии, Франции, Швейцарии, Тиролю, Бельгии и Англии, осматривал различные учебные заведения, особенно химические лаборатории, заводы и фабрики, знакомился с различными фабричными производствами. Вернувшись в Россию, осматривал фабрики и заводы в России — Шуи и Иваново-Вознесенска, Санкт-Петербурга. Результатом стал обзор русских химических заводов с различными предложениями относительно возможного их улучшения.
Результатом стал обзор русских химических заводов с различными предложениями относительно возможного их улучшения.
В 1842 году был награждён орденом Св. Станислава 2-й степени; 13 июня 1849 года — орденом Св. Анны 2-й степени. В 1852 году назначен членом московского отделения Мануфактурного совета, утверждён членом комитета по устройству Московской мануфактурной выставки 1853 года.
Состоял действительным членом Московского общества сельского хозяйства (с 1826), членом геологического общества во Франции (с 1841) и членом германского медицинского общества в Берлине (с 1844). Был инициатором разработки месторождений торфа под Москвой.
С 1854 года — действительный статский советник и Заслуженный профессор Московского университета.
Следующим заведующим стал Н.Э. Лясковский
(1854-1871). В 1843 году Н.Э. Лясковский принял предложение занять в Московском университете кафедру ветеринарии и был отправлен за границу для изучения «скотоврачебной науки». При этом, в феврале 1844 года, он получил через попечителя Московского учебного округа графа Строганова разрешение заниматься и любимыми науками — фармацией и химией, сначала в Берлине у Генриха Розе и Мичерлиха, а потом в Гиссене под руководством Либиха и в Париже у Дюма и Араго. В Гиссене он впервые представил формулу маргарина, и Либих предлагал ему остаться работать в Германии.
При этом, в феврале 1844 года, он получил через попечителя Московского учебного округа графа Строганова разрешение заниматься и любимыми науками — фармацией и химией, сначала в Берлине у Генриха Розе и Мичерлиха, а потом в Гиссене под руководством Либиха и в Париже у Дюма и Араго. В Гиссене он впервые представил формулу маргарина, и Либих предлагал ему остаться работать в Германии.
В 1846 году, по возвращении в Россию, он был определен на должность «учёного аптекаря» при Московском университете, где читал курс фармакогнозии и фармации, а с начала 1847 года стал читать публичный курс органической химии. В том же году он сделался действительным членом Московского Общества испытателей природы, а в следующем году членом Медицинской конторы по фармацевтической части в качестве визитатора аптек.
В 1849 году Лясковский защитил диссертацию на латинском языке «De cholere epidemici nonnullis causis atmosphericis» («О некоторых атмосферных причинах холерной эпидемии») и получил степень доктора медицины. В 1850 году он был избран в действительные члены Московского физико-медицинского общества, а в 1852 году в действительные члены Московского Общества сельского хозяйства. Несмотря на всё это, он оставался в должности учёного аптекаря с ничтожным жалованьем. Наконец, с отставкой профессора Геймана в 1854 году, после многих хлопот, он был утверждён, сначала исправляющим должность адъюнкта, а затем, в 1858 году, — экстраординарным профессором химии и занял кафедру чистой химии до конца своей жизни. В 1859 году он был назначен ординарным профессором химии в Московский университет.
В 1850 году он был избран в действительные члены Московского физико-медицинского общества, а в 1852 году в действительные члены Московского Общества сельского хозяйства. Несмотря на всё это, он оставался в должности учёного аптекаря с ничтожным жалованьем. Наконец, с отставкой профессора Геймана в 1854 году, после многих хлопот, он был утверждён, сначала исправляющим должность адъюнкта, а затем, в 1858 году, — экстраординарным профессором химии и занял кафедру чистой химии до конца своей жизни. В 1859 году он был назначен ординарным профессором химии в Московский университет.
По воспоминаниям одного из его учеников, профессор Н. Э. Лясковский «никогда не упускал случая теоретические воззрения на один и тот же вопрос сопоставлять в их исторической последовательности с указанием влияния того или другого воззрения на ход и развитие современной ему науки».
В 1873 году Московский университет впервые пригласил на должность заведующего кафедрой профессионального химика профессора В. В. Марковникова.
В. Марковникова.
В 1864 году В.В. Марковников защитил магистерскую диссертацию «Об изомерии органических соединений». Её тема была связана с проблемой существования изомерии среди жирных (насыщенных) кислот; Марковников доказал, что такая изомерия существует. После защиты, в 1865 году он был на два года отправлен за границу: работал в Берлине, Мюнхене и Лейпциге, — в лабораториях А. Байера, Э. Эрленмейера и А. В. Г. Кольбе.
В феврале 1867 году он был избран в число приват-доцентов по кафедре химии и, после возвращения в Россию, в сентябре того же года начал преподавательскую деятельность. Весной 1869 года он защитил докторскую диссертацию по теме «Материалы по вопросу о взаимном влиянии атомов в химических соединениях» и стал экстраординарным профессором кафедры химии; с 1870 года — ординарный профессор Казанского университета.
В 1871 году оставил университет вместе с группой учёных в знак протеста против увольнения профессора П. Ф. Лесгафта и был избран ординарным профессором Новороссийского университета в Одессе, где успел прочитать только один курс органической химии. В 1872 году он был избран профессором Московского университета и переехав в Москву, возглавил химическую лабораторию университета; в следующем году был утверждён в должности ординарного профессора.
Ф. Лесгафта и был избран ординарным профессором Новороссийского университета в Одессе, где успел прочитать только один курс органической химии. В 1872 году он был избран профессором Московского университета и переехав в Москву, возглавил химическую лабораторию университета; в следующем году был утверждён в должности ординарного профессора.
В 1875 году В.В.Морковников организовал кафедру органической химии.
В 1877 году был командирован в действующую армию и непосредственно руководил дезинфекционными работами в госпиталях. В 1880-х годах исследовал соляные озёра в Астраханской губернии и на Кавказе, минеральные воды Нарзана. С 1880 года исследовал состав нефти.
В 1892 году ему было присвоено звание заслуженного профессора Московского университета. Почётный член Московского университета (1901). Почётный член ОЛЕАЭ (1887). Несмотря на достижение 25-летней выслуги лет, его оставили на службе ещё на пять лет. В 1893 году он передал заведование лабораторией профессору Н. Д. Зелинскому, но продолжал читать лекции на физико-математическом факультете Московского университета.
В 1893 году он передал заведование лабораторией профессору Н. Д. Зелинскому, но продолжал читать лекции на физико-математическом факультете Московского университета.
В 1901 году по инициативе В. В. Марковникова был издан «Ломоносовский сборник», посвящённый истории химии в России.
В последующие годы кафедрой химии заведовали знаменитые профессоры:
А.П. Сабонеев (1877-1901), научные исследования которого, охватывают несколько областей химии. С 1870 года он исследовал производные, главным образов галоидные, ацетилена. Впервые получил и описал (1873) трибромэтилен и дийодэтилен. Детально изучил (1873) действие брома на ацетилен, азотистые производные ацетилена, действие цинковой пыли на галогенпроизводные алканов. Разработал (1881) метод получения дибромацетилена и смешанных галогенпроизводных ацетилена. Одним из первых исследовал изомерию производных гидразина, гидроксиламина и подобных неорганических соединений. Первым применил (1889—1893) и в дальнейшем широко использовал криоскопический метод определения молекулярных масс соединений в коллоидных растворах, в частности кремниевой кислоты и соединений белковой природы (альбумина, альбумозы, пептона и др. ). Открыл (1889) реакцию димеризации ацетилена в присутствии брома с образованием гексабромциклобутана, являющуюся одним из наиболее важных способов синтеза малых циклов.
). Открыл (1889) реакцию димеризации ацетилена в присутствии брома с образованием гексабромциклобутана, являющуюся одним из наиболее важных способов синтеза малых циклов.
И.А. Каблуков (1901-1912) и (1917-1923), который не только занимался теоретическими исследованиями, но и изучал природные богатства России (позднее — СССР). Участвовал в организации российского производства минеральных удобрений. В 1905 году он был назначен представителем Главного управления землеустройства и земледелия в Междуведомственную комиссию по вопросу получения окислов азота при Главном артиллерийском управлении. В 1908 году он вошёл в состав комиссии МСХИ по исследованию фосфоритов в России, чья работа положила начало производству удобрений из российского сырья. В 1909 году по предложению Департамента земледелия в МСХИ была создана комиссия по добыванию азотных туков из воздуха, получению известковой селитры и цианистого кальция. В состав комиссии вошли И. А. Каблуков, Н. Я. Демьянов и Д. Н. Прянишников. Через два года, в 1911 году, И. А. Каблуков стал председателем комиссии по вопросу о добывании окислов азота из воздуха. В 1911 году И. А. Каблуков и его отец А. С. Каблуков посетили соляные промыслы Крыма и исследовали собранные ими образцы рапы соляных озёр Крыма на предмет получения калийных солей и брома из маточных растворов, остающихся после извлечения поваренной соли. Опубликовал результаты исследования в виде монографии, которая позволила организовать в Крыму бромный завод и получать калийные соли из морской воды.
Н. Прянишников. Через два года, в 1911 году, И. А. Каблуков стал председателем комиссии по вопросу о добывании окислов азота из воздуха. В 1911 году И. А. Каблуков и его отец А. С. Каблуков посетили соляные промыслы Крыма и исследовали собранные ими образцы рапы соляных озёр Крыма на предмет получения калийных солей и брома из маточных растворов, остающихся после извлечения поваренной соли. Опубликовал результаты исследования в виде монографии, которая позволила организовать в Крыму бромный завод и получать калийные соли из морской воды.
И.С. Плотников (1912-1917) им была основана фотохимическая лаборатория Московского университета (первоначально состоявшую из 2-х отделений: оптического и фотохимического; позднее создано фотоэлектрическое; оборудовал лабораторию на уровне мировых стандартов: большую часть приборов пожертвовал сам Плотников. В 1914 году возглавил объединённую лабораторию неорганической, физической химии и фотохимии.
Большое внимание уделял технике фотохимического эксперимента, конструировал новые приборы, обучал этому своих учеников. В стенах фотохимической лаборатории Московского университета создал новые модификации светового термостата, светофильтры для УФ-области, триболюминескоп и др. В зарубежный период своей деятельности также создал несколько аппаратов для фотохимических и термоэлектрических измерений (термофотометр, фотохимический аппарат с «вращательной» экспозицией и др.), а также специальное оборудование для применения в медицине и биологии. Фотохимические аппараты Плотникова выставлены в немецком музее истории науки, как важнейшие изобретения техники фотохимического эксперимента в XX веке.
В стенах фотохимической лаборатории Московского университета создал новые модификации светового термостата, светофильтры для УФ-области, триболюминескоп и др. В зарубежный период своей деятельности также создал несколько аппаратов для фотохимических и термоэлектрических измерений (термофотометр, фотохимический аппарат с «вращательной» экспозицией и др.), а также специальное оборудование для применения в медицине и биологии. Фотохимические аппараты Плотникова выставлены в немецком музее истории науки, как важнейшие изобретения техники фотохимического эксперимента в XX веке.
Кафедру органической химии, основанную в 1922 г., возглавил профессор Александр Васильевич Степанов — специалист в области судебной химии, автор первого учебника по органической химии, профилированного для студентов медицинского профиля. Со дня основания кафедры в центре ее деятельности всегда были научные исследования в соприкасающихся с медициной областях.
В 1923 г. на медицинском факультете была учреждена новая кафедра неорганической, аналитической, физической и коллоидной химии.
Ее возглавил профессор Ярослав Степанович Пржеборовский (1923-1930), в последствие — первый заведующий кафедрой 1 -го Московского медицинского института (1930-1960 ГГ.).
Профессором Я.С Пржеборовским был введен для студентов медицинского факультета был впервые организован курс физической и коллоидной химии, пересмотрены учебные планы и программы, организована лаборатория для проведения практических занятий, был создан новый курс лекций, сопровождающийся интересно подобранными экспериментами.
Значительный период развития кафедры органической химии (1943-79 гг.) связан с именем профессора, доктора биологических наук Бориса Николаевича Степаненко – крупного ученого в области химии и биохимии углеводов, автора открытия нового полисахарида, лауреата премии имени А.Н. Баха. Б.Н. Степаненко всемерно стремился содействовать прогрессу в области химии и биохимии углеводов и утверждал значимость исследований в области химии углеводов для теоретической и клинической медицины.
Большой научный интерес имеют работы Б.Н. Степаненко и его учеников по изучению гликозилирования лекарственных веществ с гидрокси- и аминогруппами: был синтезирован ряд новых гликозидов, изучена кинетика их гидролиза, установлены закономерности, характеризующие влияние строения агликона и углеводного компонента на устойчивость гликозидных связей. Осуществлен синтез ряда новых арил N-гликозидов, постулирован механизм их гидролиза; показана возможность разделения аномерных гликозиламинов с помощью газожидкостной хроматографии; предложен новый способ определения конфигурации аномерного центра N-гликозидов методом гамма-резонансной спектроскопии, получены новые биологически активные соединения (21 авторское свидетельство). Выявлено, что синтезированные фруктозаминокислоты и фруктозопептиды оказывают специфическое действие на ряд микроорганизмов и на родоначальные кроветворные клетки костного мозга.
Широкие исследования были проведены в области нуклеозидов: синтезированы аналоги природных пиримидиновых нуклеозидов, обладающие противовирусной активностью. В 1974-79 гг. были выполнены исследования по синтезу кремнийсодержащих производных углеводов, обладающих противогипоксическим действием.
В 1974-79 гг. были выполнены исследования по синтезу кремнийсодержащих производных углеводов, обладающих противогипоксическим действием.
Результаты работы сотрудников кафедры и лаборатории углеводов Института биохимии им. А.Н. Баха представлены в 20 кандидатских и одной докторской диссертациях, а также обобщены в монографиях «Углеводы. Успехи в изучении строения и метаболизма» (1968), «Химия и биохимия углеводов (моносахариды, полисахариды)» (1977-78). Научные результаты докладывались на международных конгрессах по биохимии и химии природных соединений в США, Японии, Англии, Бельгии, Швеции, Венгрии.
В 1960 г. на базе кафедры неорганической, аналитической, физической и коллоидной химии образовались две самостоятельные кафедры: кафедра физической и коллоидной химии и кафедра неорганической химии. Кафедру физической и коллоидной химии, на которой занимались студенты лечебного, санитарно-гигиенического и фармацевтического факультетов 1 ММИ возглавил ученик Я. С. Пржеборовского, доцент, кандидат химических наук, Василий Порфирьевич Мишин, который заведовал кафедрой до 1982 года.
С. Пржеборовского, доцент, кандидат химических наук, Василий Порфирьевич Мишин, который заведовал кафедрой до 1982 года.
В.П.Мишин в 1937 г в МГУ защитил диссертацию на соискание ученой степени кандидата химических наук, в 1939 утвержден ВАК СССР в ученом звании доцента. 7 июля 1941 г. он ушел добровольцем в составе Фрунзеновской дивизии народного ополчения, а 16 октября 1941 г при выходе из Вяземского окружения раненым и контуженным попал в плен, из которого был освобожден 16 апреля 1945 г. 26 ноября 1945 г. он приступил к работе в должности доцента кафедры физической и коллоидной химии I ММИ им. Сеченова.
В.П.Мишин сформулировал новое понятие о конденсационной устойчивости дисперсных систем в 1968 г. в соавторстве с В.А. Попковым. Работы, выполненные сами В.П.Мишиным и его учениками привели к формированию научной школы основы термических методов исследования биологически-активных веществ и лекарственных соединений.
Он был талантливым лектором и методистом, принимал активное участие в координации методической работы химических кафедр медицинских вузов, являясь председателем центральной проблемной учебно-методической комиссии по химическим дисциплинам ГУУЗа МЗ СССР, а также членом центральной методической комиссии по химии МВССО СССР. Длительное время работал ученым секретарём редакционного отдела по химии и биохимии в большой и малой медицинской энциклопедиях СССР. С сентября 1958 по февраль 1973 являлся ученым секретарем ред.отдела «Биохимия БМ СССР», а с февраля 1973 являлся заместителем главного редактора ред.отдела «Биохимия». Участвовал в работе по аттестации медицинских и фармацевтических институтов страны.
Длительное время работал ученым секретарём редакционного отдела по химии и биохимии в большой и малой медицинской энциклопедиях СССР. С сентября 1958 по февраль 1973 являлся ученым секретарем ред.отдела «Биохимия БМ СССР», а с февраля 1973 являлся заместителем главного редактора ред.отдела «Биохимия». Участвовал в работе по аттестации медицинских и фармацевтических институтов страны.
Автор более 100 научных статей, учебников и учебно-методических пособий. Он обладал широчайшим кругозором, владел английским, немецким и французским языками. Им опубликовано свыше 100 научно-популярных работ.
В.П.Мишин награжден Почетной грамотой Верховного Совета РСПСР за «…успехи в развитии медицинской науки и подготовки медицинских кадров…», награжден Орденом «Знак почета» (10.12.1961), медалью «За Победу над Германией в Великой отечественной войне 1941-45 гг.», медалью «50 лет вооруженных сил СССР» (5 мая 1969 г.), медалью «За доблестный труд». В ознаменование 100-летия со дня рождения В. И. Ленина» 1.04.1970 г., медалью «В память 800-летия Москвы» 7.11.1948 и памятным значком «Отличник здравоохранения» 28.04.1955
И. Ленина» 1.04.1970 г., медалью «В память 800-летия Москвы» 7.11.1948 и памятным значком «Отличник здравоохранения» 28.04.1955
В 1982 г. в связи с изменением учебного плана кафедра физической и коллоидной химии была переименована в кафедру общей химии.
С 1982 г., после ухода В.П.Мишина на пенсию до 2018 года, кафедру общей химии возглавил его ученик — профессор, доктор фармацевтических наук — Владимир Андреевич Попков, который уделял большое внимание совершенствованию педагогического процесса преподавания химии студентам медикам. В 2002 году защитил диссертацию на соискание ученой степени доктор педагогических наук. Он продолжал работу по координации методической работы химических кафедр медицинских вузов, являясь председателем центральной проблемной учебно-методической комиссии по химическим дисциплинам ГУУЗа МЗ СССР, а также членом центральной методической комиссии по химии МВССО СССР. 17.03.1993 В. А. Попков избран член-корреспондентом РАО, а 14. 04.1999 — действительным членом РАО. Под руководством В.А. Попкова защищено 10 докторских и более 25 кандидатских диссертаций. Автор более 300 научных статей, учебников и учебно-методических пособий по химии и педагогике.
04.1999 — действительным членом РАО. Под руководством В.А. Попкова защищено 10 докторских и более 25 кандидатских диссертаций. Автор более 300 научных статей, учебников и учебно-методических пособий по химии и педагогике.
Награждён медалью ордена «За заслуги перед Отечеством» (II ст. – 1998), Лауреат премии Президента РФ в области образования (1998), Заслуженный деятель науки РФ (1996), Почётный работник высшего профессионального образования РФ (2003), Награждён медалью ордена «За заслуги перед Отечеством» (I ст. – 2018), медаль К.Д. Ушинского (2000), золотая медаль РАО «За достижения в науке», медаль Преподобного Сергия Радонежского (2001), памятная медаль 1020-летия Крещения Руси (2008), Орден Святитель Макария Митрополита Московского (2010) «За вклад в развитие духовного просвещения» и др.
В 1982 г. в связи с изменением учебного плана кафедра физической и коллоидной химии была переименована в кафедру общей химии.
Примерно в этот период в 1979-2007 гг. кафедру биоорганической химии возглавляла Заслуженный деятель науки РФ, профессор, доктор химических наук Нонна Арсеньевна Тюкавкина. Н.А. Тюкавкина крупный специалист в области химии природных соединений, Член Международной Ассоциации ученых «Группа полифенолов»; член редакций ряда научных журналов. Под руководством профессора Н.А. Тюкавкиной в тесном взаимодействии с другими научными учреждениями создан новый отечественный препарат «Диквертин» антиоксидантного и капилляропротекторного действия. Актуальность и важность ведущихся исследований отражены в Актовой речи Н.А. Тюкавкиной на Ученом Совете академии «Биофлавоноиды: химия, пища, лекарства, здоровье» (2002 г.). Н.А. Тюкавкина большое внимание уделяла совершенствованию и профилизации фундаментального химического образования в медицинских и фармацевтических учебных заведениях. Она является соавтором и редактором учебных программ и основных видов учебной литературы для студентов медицинских и фармацевтических вузов, в частности, учебников «Биоорганическая химия», «Органическая химия» (для фармацевтических и медицинских училищ), «Органическая химия.
кафедру биоорганической химии возглавляла Заслуженный деятель науки РФ, профессор, доктор химических наук Нонна Арсеньевна Тюкавкина. Н.А. Тюкавкина крупный специалист в области химии природных соединений, Член Международной Ассоциации ученых «Группа полифенолов»; член редакций ряда научных журналов. Под руководством профессора Н.А. Тюкавкиной в тесном взаимодействии с другими научными учреждениями создан новый отечественный препарат «Диквертин» антиоксидантного и капилляропротекторного действия. Актуальность и важность ведущихся исследований отражены в Актовой речи Н.А. Тюкавкиной на Ученом Совете академии «Биофлавоноиды: химия, пища, лекарства, здоровье» (2002 г.). Н.А. Тюкавкина большое внимание уделяла совершенствованию и профилизации фундаментального химического образования в медицинских и фармацевтических учебных заведениях. Она является соавтором и редактором учебных программ и основных видов учебной литературы для студентов медицинских и фармацевтических вузов, в частности, учебников «Биоорганическая химия», «Органическая химия» (для фармацевтических и медицинских училищ), «Органическая химия. Основной курс», книга 1 и Органическая химия. книга 2», практикумов «Руководство к лабораторным занятиям по биоорганической химии», «Руководство к лабораторным занятиям по органической химии», многократно переиздававшихся и пользующихся большим успехом у студентов.
Основной курс», книга 1 и Органическая химия. книга 2», практикумов «Руководство к лабораторным занятиям по биоорганической химии», «Руководство к лабораторным занятиям по органической химии», многократно переиздававшихся и пользующихся большим успехом у студентов.
С 2008 г по по 2018 г. кафедрой органической химии руководил Заслуженный работник высшей школы РФ, профессор, доктор фармацевтических наук Белобородов Владимир Леонидович. На кафедре развивается направление по исследованию фармакокинетики и метаболизма кардиологических средств и ряда фитохимических лекарственных препаратов, стандартизации лекарственных средств синтетической и растительной природы, а также стоматологических материалов с средств гигиены. Это научное направление лежит в пограничной области между химией, медициной и фармацией. С использованием современной аппаратуры, разработаны аналитические методики для определения лекарственных средств и их метаболитов в биологических жидкостях, компонентного состава растительных экстрактов и фитохимических препаратов и чистоты стандартных образцов.
В 2018 году кафедры общей химии и органической химии были объединены в кафедру химии. Объединенную кафедру химии возглавила доктор фармацевтических наук, профессор, Заслуженный работник здравоохранения РФ – Нестерова Ольга Владимировна, автор 18 патентов РФ, более 100 научных трудов, учебников и учебных пособий по химии и стоматологическому материаловедению.
На кафедре воспитана школа учеников, занимающихся вопросами фармации и медицины с позиций молекулярного подхода, подготовлено около 50 кандидатов и 15 докторов наук. Оригинальность и новизна проводимых исследований подтверждена 35 патентами РФ.
Огромную работу коллектив кафедры проводит в сотрудничестве с деканатом довузовского образования. Читаются лекции и проводятся показательные лабораторно-практические занятия с учителями-химиками школ г.Москвы, сотрудничающих с Сеченовским Университетом. Преподаватели кафедры ведут занятия по химии в РЦ Московский Сеченовский Предуниверсарий. Авторским коллективом кафедры разрабатываются задания Всероссийской Сеченовской Олимпиады по химии, а также критерии оценки проектно-исследовательских работ, представленных на ежегодных конференциях «Старт в медицину» и других конференциях, проводимых Сеченовским Университетом и Правительством г. Москвы.
Авторским коллективом кафедры разрабатываются задания Всероссийской Сеченовской Олимпиады по химии, а также критерии оценки проектно-исследовательских работ, представленных на ежегодных конференциях «Старт в медицину» и других конференциях, проводимых Сеченовским Университетом и Правительством г. Москвы.
Конспект урока и презентация по химии на тему «Углеводы»
МИНОБРНАУКИ РОССИИ
Федеральное государственное бюджетное образовательное
учреждение высшего профессионального образования
«Астраханский государственный университет»
кафедра органической, неорганической
и фармацевтической химии
Разработка урока по теме:
«Углеводы»
(10 класс)
Выполнила:
студентка группы МДЗХ-25
Пикулина Н. Ю.
Ю.
Астрахань — 2016г.
Урок по теме «УГЛЕВОДЫ».
Тема: Углеводы. Их классификация: моносахариды (глюкоза, фруктоза), дисахариды (сахароза), полисахариды (крахмал и целлюлоза). Значение углеводов в живой природе и жизни человека. Химические свойства глюкозы и сахарозы. Понятие о реакциях поликонденсации и гидролиза на примере взаимопревращений: глюкоза —— полисахарид.
Тип занятия: комбинированный.
Цель занятия: Расширение знаний об углеводах, их роли в организме человека.
Задачи занятия:
Обучающая: Закрепить знания обучающихся об углеводах, их роли в жизни человека, а также умения обобщать и систематизировать, углублять и конкретизировать теоретические знания, (классификация, строение, свойства, получение и биологическая роль, значение), закрепить теоретические знания, (зависимость свойств веществ от их строения — наличия функциональных групп) и практические умения;.
Воспитательная: Показать практическую значимость изучаемого материала, поддерживать интерес к изучаемому предмету, воспитывать потребность в знаниях о тех веществах, с которыми мы соприкасаемся в жизни. Воспитывать отрицательное отношение к вредным привычкам, бережное отношения к своему здоровью, окружающей среде.
Развивающая: Развитие навыков исследовательской работы — умение использовать химическую терминологию, проводить, наблюдать и описывать химический эксперимент, развитие творческого мышления студентов — прогнозирование свойств веществ на основе их строения;
Реактивы и оборудование:
реактивы – растворы глюкозы, аммиака, сульфата меди, щелочи натрия, азотнокислого серебра;
оборудование – штатив, пробирки, спиртовка, спички, держатель, таблицы.
Методы обучения:
беседа, постановка и решение учебных проблем, демонстрация натуральных объектов (моносахариды, сахароза, поли-сахариды) и таблиц, химический эксперимент, объяснение, рассказ. Демонстрация презентации.
Демонстрация презентации.
Средства обучения:
внутри и межпредметные связи, таблицы, оборудование и реактивы для опытов, натуральные объекты.
Информационно-справочное оснащение:
Основная литература:
1. Учебник: Химия 10 класс, учебник для общеобразовательных учреждений, автор О. С. Габриелян, М., «Дрофа», 2010г.
Дополнительная литература:
1. Естествознание. Часть II Химия. Биология. Т.А.Боровских, В.С. Рохлов М.; Издательский центр «Академия»,2005.
Интернет-ресурсы:
1. Научно-информационный журнал Биофайл
http://biofile.ru/bio/20915.html
http://biofile.ru/bio/20914.html
2. Сайт о химии. Химик
http://www.xumuk.ru/bse/2796.html
http://www. xumuk.ru/bse/973.html
xumuk.ru/bse/973.html
Междисциплинарные связи: химия, биология.
Ход урока.
Организационный момент. (5-3мин)
(Написать вопросы для дом.задания )
Домашнее задание и
задание для самостоятельной работы студентов: (3мин)
1.«Углеводы в жизни человека». «Азотсодержащие соединения». Презентации.
2.Строение, свойства и получение глюкозы, сахарозы, целлюлозы и крахмала. Распространение и роль углеводов в природе, области их применения?
3.Сравните химические свойства глюкозы, сахарозы, крахмала и целлюлозы.
2. Актуализация знаний:
Какое значение имеют углеводы для нашего организма? Биохимические функции углеводов в живом организме.
Глюкоза аккумулирует энергию Солнца, которая таким образом становится доступной живым организмам.
Ежегодно в результате фотосинтеза образуется около 20 тонн органического вещества на каждого жителя Земли.
Какой % составляют углеводы при сбалансированном рационе питания? (до 70% )
Каково строение молекулы глюкозы и какие химические свойства глюкозы можно прогнозировать, исходя из ее строения?
Показать генетическую связь неорганических соединений с органическими при получении глюкозы (биохимический процесс образования углеводов – фотосинтез). (5 мин)
3. Изучение нового материала (15-20 мин):
Демонстрация презентации. (5 – 10 мин)
4. Вопросы и тест для закрепления материала (15мин):
почему глюкозу называют бифункциональным соединением?
как доказать бифункциональность глюкозы?
5. Подведение итогов проведенного занятия (3мин).
6.Домашнее задание и задание для самостоятельной работы учеников: (5мин)
1.«Углеводы в жизни человека». Презентация.
2.Получение глюкозы, сахарозы, целлюлозы и крахмала. Распространение и роль углеводов в природе, области их применения?
3.Сравните химические свойства глюкозы, сахарозы, крахмала и целлюлозы.
4. Задача: картофель содержит 25% крахмала. Какую массу глюкозы можно получить при полном гидролизе крахмала, содержащего в 504кг такого картофеля?
Источники дополнительной информации по вопросуАвтор и наименование
Страницы
(форма доступа для Интернет-ресурсов)
Основная литература
Химия 10 Габриелян О.С. Дрофа,2010г.
Стр. 104
Дополнительная литература
Естествознание. Часть II Химия. Биология. Т.А.Боровских, В.С. Рохлов
Часть II Химия. Биология. Т.А.Боровских, В.С. Рохлов
§ 13.2§§§§§§§§§¨¨§13.1,
Интернет ресурсы
Биофайл. Научно-информационный журнал
http://biofile.ru/bio/20915.html
Химик. Сайт о химии
http://www.xumuk.ru/bse/2796.html
Тест по теме «Углеводы».
1.Какие продукты образуются в результате окисления глюкозы аммиачным раствором оксида серебра?
а) Глюконовая кислота и вода;
б) многоатомный спирт и вода;
в) глюконовая кислота и серебро;
г) сложный эфир пентанитроглюкозы и вода.
2.Какое вещество образуется при спиртовом брожении глюкозы?
а) Этиловый спирт;
б) метиловый спирт;
в) молочная кислота;
г) глюконовая кислота.
3. Какие группы веществ дают реакцию «серебряного зеркала»?
а) Глюкоза, глицерин, этиленгликоль;
б) этаналь, глюкоза, муравьиная кислота;
в) глюкоза, молочная кислота, фруктоза.
4. Глюкоза является ———————- (выберите ответ):
а) экологически вредным веществом, т.к. отравляет растительные и животные организмы;
б) ценным для организма веществом, т.к. необходима для образования ферментов;
в) ценным для организма веществом, т.к. легко окис-ляется и поэтому является источником энергии;
г) безвредным, но ненужным для организма вещест-вом.
5. Назовите конечный продукт полного гидролиза целлюлозы:
а) Cахароза;
б) фруктоза;
в) а-глюкоза;
г) в-глюкоза.
6. Дополните фразу: «Крахмал используют» ———— (выберите правильный ответ):
а) не используют, т.к. это экологически вредное вещесво;
б) для накрахмаливания белья и некоторых видов одежды;
в) в пищу для приготовления киселей, выпечки и кондитерских изделий;
г) в пищу для приготовления жаркого;
д) для получения глюкоза;
е) для изготовления искусственных волокон.
7. « Целлюлозу применяют —————- (выберите ответ):
а) не применяют, т.к. это вещество получено искусственным путем, дорогое и экологически вредное;
б) для получения глюкозы, из которой потом получат гидролизный этанол;
в) для получения искусственных волокон (ацетатного
волокна, медноаммиачного шелка, вискозы)
г) в строительстве (в смеси с другими соединениями для изготовления различных строительных конструкций, а также при изготовлении мебели, скульптур и т. д.).
д.).
8. Составы каких веществ способствуют общей формуле Cn(H2O)m, но не относятся к классу углеводов?
а) H-C-H ; б) C6H12O6; в) C5H10O5; г) CH3COOH.
O
9.Какое из веществ не подергается гидролизу?
а) крахмал, б) сахароза, в) глюкоза, г) целлюлоза.
10.Какой тип брожения углеводов существует?
а) Маслянокислое, б) молочнокислое, в) спиртовое,
г) все предыдущие ответы вместе.
11. Найдите синоним термину « целлюлоза»:
а) сахароза, б) вискоза, в) клетчатка, г) пироксилин.
12. Исключите лишнее понятие:
а) рибоза, б) заноза, в) глюкоза, г) галактоза.
13. Какой сахар нельзя употреблять в пищу?
а) Тростниковый,
б) свинцовый,
в) виноградный,
г) свекловичный.
Краткая история открытия и получения углеродных наноструктур
Выжимка из моего реферата, написанного для экзамена по истории и философии науки.
Кто хочет полную версию (там страниц 25) — пишите.
Углерод занимает особое положение среди химических элементов, хотя не принадлежит к самым распространенным в природе (в земной коре — всего 0,15555555 % по массе, правда, в нашей галактике, согласно недавним оценкам, углерод 4й сразу после водорода, гелия и кислорода). Однако углерод является основой строения всего животного и растительного мира, входя в состав белков, жиров и углеводов. Углерод в природе встречается в кристаллической форме в виде алмаза, лонсдейлита, графита, в форме аморфных образований входит в состав углей и шунгитов. Углерод обнаружен в атмосфере Солнца, планет в парообразном состоянии и в виде соединений с азотом и водородом, в твердом состоянии найден в каменных и железных метеоритах.
Углерод – один из самых необычных элементов. Ни один другой элемент не обладает тем разнообразием свойств, иногда прямо противоположных, которое присуще углероду. Это эталон прозрачности и абсолютно черное тело; диа- и парамагнетик; диэлектрик и металл; полупроводник и полуметалл; сверхтвердый и сверхмягкий материал; теплоизолятор и один из лучших проводников тепла.
Ни один другой элемент не обладает тем разнообразием свойств, иногда прямо противоположных, которое присуще углероду. Это эталон прозрачности и абсолютно черное тело; диа- и парамагнетик; диэлектрик и металл; полупроводник и полуметалл; сверхтвердый и сверхмягкий материал; теплоизолятор и один из лучших проводников тепла.
В 1972 г. П. Уокер назвал углерод «старым, но всегда новым материалом», подчеркнув, что «прогресс в разработке новых углеродных материалов будет продолжаться — как глава всеобщей истории материаловедения». Справедливость этого утверждения многократно подтверждалась в минувшие годы.
В 1985 году группа исследователей — Роберт Кёрл, Харольд Крото, Ричард Смолли, Хис и О’Брайен — исследовали масс-спектры паров графита, полученных при лазерном облучении твёрдого образца, и обнаружили пики с максимальной амплитудой, соответствующие кластерам, состоящим из 60 и 70 атомов углерода. Они предположили, что данные пики отвечают молекулам С60 и С70 и выдвинули гипотезу, что молекула С60 имеет форму усечённого икосаэдра. Такие полиэдрические кластеры углерода получили название фуллеренов. За открытие фуллеренов Крото, Смолли и Кёрлу в 1996 году была присуждена Нобелевская премия по химии. Однако возможность их существования была предсказана ещё в 1971 году в Японии и теоретически обоснована в 1973 году в СССР.
Такие полиэдрические кластеры углерода получили название фуллеренов. За открытие фуллеренов Крото, Смолли и Кёрлу в 1996 году была присуждена Нобелевская премия по химии. Однако возможность их существования была предсказана ещё в 1971 году в Японии и теоретически обоснована в 1973 году в СССР.
Что касается углеродных нанотрубок, то здесь нельзя назвать точную дату их открытия. Хотя общеизвестным является факт наблюдения структуры многостенных нанотрубок Иидзимой в 1991 г., существуют более ранние свидетельства открытия углеродных нанотрубок. Так, например, группа ученых Института катализа СО АН СССР в 1977 году при изучении зауглероживания железохромовых катализаторов дегидрирования зарегистрировали образование «пустотелых углеродных дендритов», при этом был предложен механизм образования и описано строение стенок.
Теоретическое исследование графена началось задолго до получения реальных образцов материала. Химик Бенджамин Броуди первым, ещё в 1859 году испытал действие сильных кислот на графите, получил суспензию кристаллов оксида графена. Первые графеновые слои, выращенные на металлических подложках Ru, Rb, Ni, были получены ещё в 1970 году Грантом и Блэкли. Но только в 2004 году простой метод получения образцов графена, предложенный Андреем Геймом и Константином Новосёловым позволил сотням лабораторий по всему миру включиться в исследования уникальных свойств графена. За исследования свойств графена Андрей Гейм и Константин Новосёлов получили Нобелевскую премию по физике за 2010 год.
Первые графеновые слои, выращенные на металлических подложках Ru, Rb, Ni, были получены ещё в 1970 году Грантом и Блэкли. Но только в 2004 году простой метод получения образцов графена, предложенный Андреем Геймом и Константином Новосёловым позволил сотням лабораторий по всему миру включиться в исследования уникальных свойств графена. За исследования свойств графена Андрей Гейм и Константин Новосёлов получили Нобелевскую премию по физике за 2010 год.
Таким образом, когда речь идет об углеродных наноструктурах, момент открытия нового материала зачастую не совпадает с моментом его получения. Фуллерены были «открыты» как интерпретация масс-спектра, уже после их получения, а об углеродных нанотрубках и графене говорили ещё задолго до бума углеродных наноструктур на рубеже ХХ-ХХI веков.
Сэр Гарольд Крото, Роберт Кёрл и Ричард Смолли — Нобелевская премия по химии (1996) «За открытие фуллеренов»
Первые «официально» открытые углеродные наноструктуры были получены 30 лет, в 1985 году Крото, Смолли и Кёрлом. Это были фуллерены, замкнутые молекулы, представляющие из себя выпуклые замкнутые многогранники из 20 и более атомов. При этом гипотезы об их существовании выдвигались гораздо раньше, ещё в 1970х годах независимо Джонсом и Осавой. Примерно тогда же советские физики Д. А. Бочвар и Е. Г. Галперн рассчитали электронную структуру таких замкнутых молекул углерода и установили, что они являются химически стабильными. Тогда на эти работы особого внимания не обратили. В середине 80х годов Крото, Смолли и Кёрл, моделируя процессы, происходящие в атмосфере гигантских красных углеродных звёзд, получили пики масс-спектра, соответствующие шестидесяти атомам углерода. Что интересно, полученный ими масс-спектр совершенно не похож на углеродные масс-спектры различных «космических» структур (комет и т. д), полученные около 5-6 лет назад.
Это были фуллерены, замкнутые молекулы, представляющие из себя выпуклые замкнутые многогранники из 20 и более атомов. При этом гипотезы об их существовании выдвигались гораздо раньше, ещё в 1970х годах независимо Джонсом и Осавой. Примерно тогда же советские физики Д. А. Бочвар и Е. Г. Галперн рассчитали электронную структуру таких замкнутых молекул углерода и установили, что они являются химически стабильными. Тогда на эти работы особого внимания не обратили. В середине 80х годов Крото, Смолли и Кёрл, моделируя процессы, происходящие в атмосфере гигантских красных углеродных звёзд, получили пики масс-спектра, соответствующие шестидесяти атомам углерода. Что интересно, полученный ими масс-спектр совершенно не похож на углеродные масс-спектры различных «космических» структур (комет и т. д), полученные около 5-6 лет назад.
Не зная ничего о теоретических догадках предшественников, они попытались интерпретировать свой масс-спектр, предложив для молекулы С60 структуру усеченного икосаэдра. Икосаэдр — правильный выпуклый двадцатигранник[1], одно из Платоновых тел, соответствует (по Платону) воде. Было предложено и название молекулы — бакминстерфуллерен, в честь американского архитектора Р. Бакминстера Фуллера, автора концепции геодезических куполов — сразивших мир зданий-многогранников. Напрямую подтвердить или опровергнуть гипотезу о бакминстерфуллерене могло бы только применение структурно-чувствительных методов исследования, например, спектроскопии ЯМР. Гипотеза подтвердилась только спустя 5 лет, благодаря разработке Крёчмером и Хафманом простого и производительного способа получения макроскопических количеств С60 и его более крупных собратьев по семейству фуллеренов. Можно говорить, что фуллерены сначала были получены, и только потом – открыты, а о возможности их существования рассуждали ещё за несколько лет до этого.
Икосаэдр — правильный выпуклый двадцатигранник[1], одно из Платоновых тел, соответствует (по Платону) воде. Было предложено и название молекулы — бакминстерфуллерен, в честь американского архитектора Р. Бакминстера Фуллера, автора концепции геодезических куполов — сразивших мир зданий-многогранников. Напрямую подтвердить или опровергнуть гипотезу о бакминстерфуллерене могло бы только применение структурно-чувствительных методов исследования, например, спектроскопии ЯМР. Гипотеза подтвердилась только спустя 5 лет, благодаря разработке Крёчмером и Хафманом простого и производительного способа получения макроскопических количеств С60 и его более крупных собратьев по семейству фуллеренов. Можно говорить, что фуллерены сначала были получены, и только потом – открыты, а о возможности их существования рассуждали ещё за несколько лет до этого.
За открытие фуллеренов им в 1996 году была присуждена Нобелевская премия по химии. Получение фуллеренов инициировало продолжающийся до сих пор «бум» углеродных наноструктур: практически одновременно были получены и углеродные нанотрубки.
Слева — фрагмент статьи Сумио Иджимы с электронномикроскопическими изображениями высокого разрешения двух-, пяти- и семистенных нанотрубок, в центре — Фрагмент статьи Л. В. Радушкевича и В. М. Лукъяновича с электронномикроскопическими изображениями многостенных углеродных нанотрубок (по современной терминологии)
Впервые структура многостенной нанотрубки была экспериментально продемонстрирована в 1991 г. Иджимой. Но однозначно отдавать Иджиме приоритет в окрытии нанотрубок нельзя, так как о наблюдении многостенных нанотрубок (без прямого разрешения и понимания их многостенной структуры) сообщалось в нескольких статьях, появившихся в печати до работы Иджимы. первое электронно-микроскопическое изображение похожих структур нанотрубками, было опубликовано в 1952 г. российскими учёными Л. В. Рабушкевичем и В. М. Лукъяновичем. В 1982 в статье А. М. Нестеренко и др. были продемонстрированы не только электронно-микроскопические снимки «многостенных трубчатых углеродных кристаллов», но и впервые предложена модель образования структуры углеродных нанотрубок как свёрнутой в цилиндр графеновой плоскости. То есть в СССР то, что мы сегодня называем «углеродные нанотрубки», получили задолго до Иджимы. Добавлю, что уже в 1976 группа Моринобу Эндо опубликовала электронно-микроскопический снимок углеродной структуры, напоминающей одностенную трубку. Вероятно, никто из перечисленных ученых в своё время ещё не подозревал об этом, да и разрешение электронных микроскопов просто не позволяло более детально исследовать полученные структуры. Возможно, именно поэтому углеродные нанотрубки – единственная из трех «основных» углеродных наноструктур, за которую не дали Нобелевскую Премию.
То есть в СССР то, что мы сегодня называем «углеродные нанотрубки», получили задолго до Иджимы. Добавлю, что уже в 1976 группа Моринобу Эндо опубликовала электронно-микроскопический снимок углеродной структуры, напоминающей одностенную трубку. Вероятно, никто из перечисленных ученых в своё время ещё не подозревал об этом, да и разрешение электронных микроскопов просто не позволяло более детально исследовать полученные структуры. Возможно, именно поэтому углеродные нанотрубки – единственная из трех «основных» углеродных наноструктур, за которую не дали Нобелевскую Премию.
Графен, двумерная структура из атомов углерода толщиной в один атом, слой, из которого составлен издавна известный человечеству графит, в свободном виде была получена всего 10 лет назад. Хотя изначально считалось, что такая структура не может существовать в принципе — в середине 1930-х гг. теория выдающихся физиков Л. Ландау и Р. Пайерса утверждала, что двумерные кристаллы, подобные графену, неустойчивы и легко разрушаются. При этом химики получали различные близкие к графену структуры в ХIX- начале XX века, но просто не имели методов, необходимых для подробного анализа таких структур. Английский химик Броуди в 1859 году испытал действие сильных кислот на графите и получил суспензию кристаллов оксида графена. Доказательство малой толщины этих кристаллов были получены только в 1948 году после эксперимента Дж. Руесса и Ф. Фогта, которые использовали просвечивающий электронный микроскоп. Хотя эти кристаллы были не чистым графеном и их толщина составляла несколько нанометров, в последующих работах Хоффмана и Бёма было показано, что при восстановлении оксида графита попадаются также фрагменты графита атомарной толщины. Первые графеновые слои, выращенные на металлических подложках Ru, Rb, Ni, были получены в 1970 году Грантом и Блэкли. Однако «графеновый бум» начался только после 2004 года и статью Андрея Гейма и Константина Новоселова о получении с помощью механического расслоения (с помощью скотча) графита. За исследования свойств графена Андрей Гейм и Константин Новосёлов получили Нобелевскую премию по физике за 2010 год и стала ещё одной премией, связанной с исследованием углеродных наноструктур.
При этом химики получали различные близкие к графену структуры в ХIX- начале XX века, но просто не имели методов, необходимых для подробного анализа таких структур. Английский химик Броуди в 1859 году испытал действие сильных кислот на графите и получил суспензию кристаллов оксида графена. Доказательство малой толщины этих кристаллов были получены только в 1948 году после эксперимента Дж. Руесса и Ф. Фогта, которые использовали просвечивающий электронный микроскоп. Хотя эти кристаллы были не чистым графеном и их толщина составляла несколько нанометров, в последующих работах Хоффмана и Бёма было показано, что при восстановлении оксида графита попадаются также фрагменты графита атомарной толщины. Первые графеновые слои, выращенные на металлических подложках Ru, Rb, Ni, были получены в 1970 году Грантом и Блэкли. Однако «графеновый бум» начался только после 2004 года и статью Андрея Гейма и Константина Новоселова о получении с помощью механического расслоения (с помощью скотча) графита. За исследования свойств графена Андрей Гейм и Константин Новосёлов получили Нобелевскую премию по физике за 2010 год и стала ещё одной премией, связанной с исследованием углеродных наноструктур. В 2013 году Михаил Кацнельсон, соавтор Гейма и Новоселова, награждён премией Спинозы за разработку базовой концепции и понятий, которыми оперирует наука в области графена. Необходимо отметить, премия была дана не только «за открытие» графена. Не менее, а возможно, что и более важная часть исследования Гейма и Новоселова – это исследование различных свойств графена, в первую очередь, электронных.
В 2013 году Михаил Кацнельсон, соавтор Гейма и Новоселова, награждён премией Спинозы за разработку базовой концепции и понятий, которыми оперирует наука в области графена. Необходимо отметить, премия была дана не только «за открытие» графена. Не менее, а возможно, что и более важная часть исследования Гейма и Новоселова – это исследование различных свойств графена, в первую очередь, электронных.
Андрей Гейм, Константин Новоселов — Нобелевская премия по физике (2010) «За новаторские эксперименты по исследованию двумерного материала графена»
Наноуглеродная наука носит междисциплинарный характер. Физика, химия, математика, астрономия и медицина представляют неполный перечень дисциплин, связанных с исследованием фуллеренов, нанотрубок, наноалмазов и графена. Например, изучение фуллеренов открывает пути для построения новых материалов с заданными свойствами на атомарном уровне. Мировая углеродная «наногонка» стала одним из центральных эпизодов в развитии НТ. По мнению Осавы, если бы не было открытия фуллеренов в 1985 г. и углеродных нанотрубок в 1991 году, то появление нанотехнологии могло быть отсрочено, по крайней мере, на несколько десятилетий. В 2004 году к ним присоединился графен. На данный момент предложено множество различных применений углеродных наноструктур — электроника (гибкие электронные устройства, высокочастотные транзисторы, логические транзисторы), фотоника (фотодетекторы, оптические модуляторы, лазеры с синхронизацией мод, THz генераторы и оптические поляризаторы), композитные материалы, краски и покрытия, приложения для хранения и генерации энергии, сенсоры и приложения для метрологии, биоприложения и многое, многое другое. Однако, несмотря на многообразие применений существует множество проблем, связанных с развитием этих технологий. И главной проблемой, как ни странно, остается проблема синтеза высококачественных углеродных наноструктур в макроскопических масштабах. До сих пор ученые спорят, каков именно механизм образования фуллерена С60, до сих пор выдвигаются различные модели образования и методы получения графена и углеродных нанотрубок.
и углеродных нанотрубок в 1991 году, то появление нанотехнологии могло быть отсрочено, по крайней мере, на несколько десятилетий. В 2004 году к ним присоединился графен. На данный момент предложено множество различных применений углеродных наноструктур — электроника (гибкие электронные устройства, высокочастотные транзисторы, логические транзисторы), фотоника (фотодетекторы, оптические модуляторы, лазеры с синхронизацией мод, THz генераторы и оптические поляризаторы), композитные материалы, краски и покрытия, приложения для хранения и генерации энергии, сенсоры и приложения для метрологии, биоприложения и многое, многое другое. Однако, несмотря на многообразие применений существует множество проблем, связанных с развитием этих технологий. И главной проблемой, как ни странно, остается проблема синтеза высококачественных углеродных наноструктур в макроскопических масштабах. До сих пор ученые спорят, каков именно механизм образования фуллерена С60, до сих пор выдвигаются различные модели образования и методы получения графена и углеродных нанотрубок.
Сам К. Новоселов с коллегами отмечает, что на текущем рынке существует «Четкая иерархия между тем, как скоро появляется идея о каком-либо приложении и тем, когда оно становится доступным пользователю или потребителю. Те приложения, которые используют «низкий сорт» графена (самый дешевый и самый доступный материал) можно ожидать на рынке в течение нескольких лет, однако, тем приложениям, которым требуется «высший сорт» (высокая электронная проводимость или биосовместимость), требуются десятилетия, чтобы развиться». Данные заявления выглядят скорее как некоторые оправдания перед мировой общественностью за поднятый «бум» вокруг графена. Поэтому, несмотря на, в принципе, позитивный прогноз («всё-всё будет – просто позже»), после прочтения появляется легкое чувство грусти. Но можно надеяться, что за 10-15 лет все действительно изменится.
[Список литературы]1.С. Н. Колокольцев. Углеродные материалы: свойства, технологии, применения. Долгопрудный: Издательский Дом «Интеллект», 2012.
2. Е. А. Кац. Фуллерены, углеродные нанотрубки и нанокластеры: Родословная форм и идей. Изд. 2-е. М.: Книжный дом «Либроком», 2009.
3. А. В. Елецкий., Б.М. Смирнов. Фуллерены. УФН, Том 163, №2, февраль 1993.
4. А. В. Елецкий. Углеродные нанотрубки. УФН, Том 167, №9, сентябрь 1997.
5. A. K. Geim, K. S. Novoselov. The Rise of Graphene. Nature Materials 6, 183 – 191, 2007.
5. История открытия углерода. http://www.alhimikov.net/otkritie_elementov/C.html
6. Углерод, Carboneum, С (6). http://www.chem.msu.su/rus/history/element/C.html
7. УГЛЕРОД. Рождающий жизнь. http://xn--e1aaqamqrh.xn--p1ai/rozhdayushchij-zhizn.html
8. УГЛЕРОД. Энциклопедия Кругосвет. http://www.krugosvet.ru/enc/nauka_i_tehnika/himiya/UGLEROD.html
9. Р.Б.Хайманн, С.Е.Евсюков. Аллотропия углерода. Природа, №8, 2003. http://vivovoco.astronet.ru/VV/JOURNAL/NATURE/08_03/ALLO.HTM
10. David Bradley. The Chemical History of Graphene. http://www.materialstoday.com/carbon/comment/chemical-history-of-graphene/
ИСТОРИЯ ОТКРЫТИЯ ВИТАМИНОВ — блог Планета Здоровья
Практически во всех сколько-нибудь развитых цивилизациях авторитетные врачи и ученые утверждали, что существует прямая связь между состоянием здоровья человека и его рационом. Древние уже каким-то образом догадывались о существовании веществ, необходимых не только для нормального функционирования организма, но и для профилактики болезней и даже для лечения болезней. Открытие витаминов позволило практически полностью победить такие заболевания, как цинга, бери-бери, пеллагра или рахит. Но когда же все-таки были открыты витамины?
Древние уже каким-то образом догадывались о существовании веществ, необходимых не только для нормального функционирования организма, но и для профилактики болезней и даже для лечения болезней. Открытие витаминов позволило практически полностью победить такие заболевания, как цинга, бери-бери, пеллагра или рахит. Но когда же все-таки были открыты витамины?ПЕРВЫЕ ДОГАДКИ
В Древнем мире и в Средние века интерес к невидимым или искусственно созданным веществам, способным исцелить человека, был традиционно высок: алхимия стремилась найти панацею — лекарство от всех болезней, шумеры, египтяне, славяне, греки и римляне лечились травами.
В древних трудах описано множество человеческих недомоганий, которые, как мы знаем сегодня, возникают от недостатка витаминов. Военные походы всех времен были омрачены не только ужасами боев, но и жестоким действием цинги. Она была зловещим спутником морских путешественников: моряки при достаточных запасах продовольствия были долгое время лишены свежих фруктов, овощей и свежего мяса (оно обычно заменялось солониной).
Лишь в середине XVIII века шотландец Джеймс Линд выяснил, что, изменив корабельный рацион, можно победить цингу, — и только в 1795 году лимоны и лаймы стали стандартной добавкой в меню британских мореходов. Жители Древнего Египта страдали от так называемой «куриной слепоты» — они боролись с ней, поедая печень (источник витамина A).
С нарушением поступления витаминов в организм связаны 3 принципиальных патологических состояния: отсутствие витамина — авитаминоз, недостаток витамина — гиповитаминоз,
избыток витамина — гипервитаминоз.
Вероятно, именно от египетских знахарей великий Гиппократ получил эти знания, советуя своим пациентам пару раз в неделю питаться сырой печенью в меду. В 1330 году в Пекине китайский врач Ху Сыхуэй опубликовал трехтомный труд «Важные принципы пищи и напитков», систематизировавший знания о терапевтической роли питания и утверждавший необходимость разнообразить рацион для поддержания здоровья.
ОТКРЫТИЕ
Научные факты, свидетельствующие о существовании группы веществ, необходимых для человеческого организма, накапливались учеными постепенно. В своей докторской диссертации 1880 года русский педиатр Николай Иванович Лунин утверждал, что для нормального функционирования живого организма помимо белков, жиров, углеводов и воды необходимы некие дополнительные вещества. Он писал: «Обнаружить эти вещества и изучить их значение в питании было бы исследованием, представляющим большой интерес». В 1906 году англичанин Фредерик Хопкинс также предположил, что помимо белков, жиров и углеводов пища содержит еще какие-то вещества, необходимые для человеческого организма. Хопкинс назвал их «accessory food factors».
В своей докторской диссертации 1880 года русский педиатр Николай Иванович Лунин утверждал, что для нормального функционирования живого организма помимо белков, жиров, углеводов и воды необходимы некие дополнительные вещества. Он писал: «Обнаружить эти вещества и изучить их значение в питании было бы исследованием, представляющим большой интерес». В 1906 году англичанин Фредерик Хопкинс также предположил, что помимо белков, жиров и углеводов пища содержит еще какие-то вещества, необходимые для человеческого организма. Хопкинс назвал их «accessory food factors».
Сам же термин «vitamine» был введен польско-американским биохимиком Казимежем Функом в 1912 году — именно он выделил, наконец, кристаллический препарат, небольшое количество которого излечивало болезнь бери-бери (авитаминоз B1). Этому предшествовало важнейшее наблюдение голландского врача Христиана Эйкмана. В 1889 году он обнаружил, что куры при питании вареным белым рисом заболевают бери-бери, а при добавлении в пищу рисовых отрубей — излечиваются.
Христиан Эйкман и Фредерик Хопкинс в 1929 году стали лауреатами Нобелевской премии по медицине — награда Хопкинса вручалась с формулировкой «За открытие витаминов, стимулирующих процессы роста», Эйкман получил премию «За вклад в открытие витаминов». Роль Николая Лунина и Казимежа Функа, таким образом, оценена не была. В 1940-х годах было расшифровано химическое строение витаминов — и в фармакологии началась новая эра.
Были ли углеводы пищей для мозга наших древних предков? : Соль: NPR
Группа британских исследователей догадывалась , что, когда древние люди научились готовить, крахмалистые продукты, такие как корнеплоды или травы, могли дать им калорийность, подпитывающую эволюцию человеческого мозга. Скотт Шерилл-Микс / Flickr скрыть подпись
переключить подпись Скотт Шерилл-Микс / Flickr Группа британских исследователей предположила , что, когда древние люди научились готовить, крахмалистые продукты, такие как корнеплоды или травы, могли дать им калорийность, подпитывающую эволюцию человеческого мозга.
Углеводы — богатый источник энергии. Именно поэтому некоторые из нас могут чувствовать себя немного противоречивыми по поводу них, поскольку несколько недавних исследований и диет показали, что мы должны сокращать их, чтобы похудеть. (Последнее исследование пришло к выводу, что общее количество калорий имеет наибольшее значение, если вы хотите похудеть.)
Однако наши древние предки жадно собирали углеводы для получения энергии. И, глядя на прошлые работы по эволюции человека, группа британских исследователей догадывалась , что когда древние люди научились готовить, крахмалистые продукты, такие как корнеплоды или травы, могли дать им калорийность, которая подпитывала эволюцию человеческого мозга. .
Исследователи, изучающие палеолитические диеты, ранее предполагали, что ранний человеческий мозг начал увеличиваться по крайней мере 2,5 миллиона лет назад после того, как первые люди научились разделывать и обрабатывать мясо каменными орудиями. «Но я не думаю, что это вся история», — говорит Марк Томас, эволюционный генетик из Университетского колледжа Лондона. «Около 800 000 лет назад размер мозга действительно увеличился».
«Но я не думаю, что это вся история», — говорит Марк Томас, эволюционный генетик из Университетского колледжа Лондона. «Около 800 000 лет назад размер мозга действительно увеличился».
В новой статье в The Quarterly Review of Biology Томас и его коллеги утверждают, что мозг внезапно начал развиваться быстрее, потому что наши предки обнаружили еще лучшую пищу для мозга.«В этот момент мы развиваем использование огня и начинаем употреблять больше продуктов, богатых углеводами», — говорит Томас. «[Это] было критически важно для расширения мозга».
Углеводы, особенно длинные цепочки простых сахаров, глюкозы или крахмалов, являются идеальной пищей для питания мозга, — говорит Томас. «Мозгу абсолютно необходима глюкоза», — говорит он. А с пищей, богатой углеводами, организму не нужно тратить дополнительную энергию на преобразование других питательных веществ, таких как те, которые содержатся в мясе, в глюкозу для питания мозга.
Когда люди начали готовить овощи, ферменты, переваривающие крахмал в их кишечнике, называемые амилазами, могли работать намного эффективнее, чем с сырыми овощами. «Например, в картофеле вы могли бы переваривать крахмал примерно в 20 раз быстрее, если бы он [он] был приготовлен, а не сырым», — говорит Томас. «И самые ранние свидетельства пожара также относятся к периоду от 500 до 800 000 лет». Приготовление пищи превратило углеводы в основной источник энергии, в то время как наш мозг начал всерьез расширяться, говорится в статье.
Чтобы выяснить, действительно ли люди ели больше крахмала в это время, команда исследовала гены, которые производят амилазу. Томас говорит, что генетический анализ предполагает, что эти гены начали размножаться примерно в то же время, когда люди начали готовить, а это означает, что наша слюна эволюционировала, чтобы нести более высокие концентрации фермента. «Для переваривания требуется больше крахмала, и поэтому увеличение количества генов амилазы в слюне является преимуществом», — говорит он. Это означало бы, что первые люди могли получать больше глюкозы из картофеля, давая больше энергии для роста голодного мозга.
Это означало бы, что первые люди могли получать больше глюкозы из картофеля, давая больше энергии для роста голодного мозга.
Но другие исследователи не согласны с этой гипотезой. «Имеет смысл, что если вы едите больше крахмала, у вас будет больше амилазы, и это прекрасное предположение. Но факт в том, что данные еще не подтверждают это», — говорит Ричард Рэнгхэм, биологический антрополог из Гарвардского университета.
Чтобы подтвердить свою гипотезу, Томас и его коллеги процитировали работу антропологов из Университета штата Аризона, согласно которой у определенных групп людей с диетой с высоким содержанием крахмала было больше амилазы в слюне, а у людей с диетой с низким содержанием крахмала — меньше.
Wrangham говорит, что исследование неправильно проанализировало рацион каждой популяции. «Основываясь на данных, которые я нашел, казалось, что у них получилось прямо противоположное. Их популяции с высоким содержанием крахмала потребляли меньше крахмала, чем любая из популяций с низким содержанием крахмала». По словам Рэнгема, это означает, что нет никаких доказательств того, что употребление большего количества углеводов заставит слюну эволюционировать, чтобы лучше переваривать крахмал. (Томас также признает, что исследование ошибочно.)
По словам Рэнгема, это означает, что нет никаких доказательств того, что употребление большего количества углеводов заставит слюну эволюционировать, чтобы лучше переваривать крахмал. (Томас также признает, что исследование ошибочно.)
Другие критики говорят, что временная шкала в версии эволюции мозга Томаса не совсем совпадает друг с другом, что, как признает Томас, также верно.Когда начали размножаться гены амилазы, неясно. «По сути, это когда-то в течение последнего миллиона лет, но мы не знаем когда», — говорит он. «Мы хотим иметь больше, гораздо больше доказательств того, когда [это] начало расти».
И когда именно люди начали готовить, также остается предметом споров. «Лучшее свидетельство пожара, которое у нас есть 700, 800 000 лет назад», — говорит Шара Бейли, биологический антрополог из Нью-Йоркского университета. «Если они утверждают, что приготовление крахмала было необходимо для большого мозга, что ж, ничего страшного», — говорит она.«Но к тому времени, когда у нас есть веские доказательства для приготовления пищи, у нас уже сформировался большой мозг».
Какая именно пища привела к появлению современного человеческого мозга, может быть спорным вопросом. «Приготовление пищи облегчает употребление пищи, и способность готовить вообще, вероятно, важнее, чем то, что готовили первые люди», — говорит Сюзана Херкулан-Хузель, нейроанатом из Федерального университета в Рио-де-Жанейро, Бразилия.
«Мне нравится думать, что наши предки начали жарить все, что они могли придумать, чтобы положить им в рот, — и тогда вы получите много белка, углеводов и жира, потому что, черт возьми, жареный жир восхитителен», — говорит она.В конце концов, нам нужно много разных питательных веществ для работы нашего тела и мозга, и приготовление множества разных продуктов — единственный способ легко получить их все.
углеводов | Encyclopedia.com
КОНЦЕПЦИЯ
Углеводы — это питательные вещества, наряду с белками и другими типами химических соединений, но это гораздо больше. Помимо сахаров, разновидностей которых намного больше, чем обычная сахароза или столовый сахар, углеводы появляются в виде крахмалов и целлюлозы. По сути, они являются конструкционными материалами, из которых сделаны растения. Углеводы производятся одним из самых сложных, жизненно важных и удивительных процессов в физическом мире: фотосинтезом. Поскольку они являются неотъемлемой частью жизни растений, неудивительно, что углеводы содержатся в большинстве фруктов и овощей. И хотя они не являются диетической потребностью в отличие от витаминов или незаменимых аминокислот, их трудно есть, не потребляя углеводов, которые являются отличными источниками быстро сжигаемой энергии.Однако не все углеводы имеют одинаковую питательную ценность: в целом те, которые созданы природой, полезны для организма, в то время как углеводы, произведенные человеческим вмешательством, — некоторые формы макарон и большинство сортов хлеба, белого риса, крекеров, печенья и т. Д. и так далее — гораздо менее полезны.
По сути, они являются конструкционными материалами, из которых сделаны растения. Углеводы производятся одним из самых сложных, жизненно важных и удивительных процессов в физическом мире: фотосинтезом. Поскольку они являются неотъемлемой частью жизни растений, неудивительно, что углеводы содержатся в большинстве фруктов и овощей. И хотя они не являются диетической потребностью в отличие от витаминов или незаменимых аминокислот, их трудно есть, не потребляя углеводов, которые являются отличными источниками быстро сжигаемой энергии.Однако не все углеводы имеют одинаковую питательную ценность: в целом те, которые созданы природой, полезны для организма, в то время как углеводы, произведенные человеческим вмешательством, — некоторые формы макарон и большинство сортов хлеба, белого риса, крекеров, печенья и т. Д. и так далее — гораздо менее полезны.
КАК ЭТО РАБОТАЕТ
Что такое углеводы
Углеводы — это природные соединения, состоящие из углерода, водорода и кислорода, которые вырабатываются зелеными растениями в процессе фотосинтеза. Проще говоря, фотосинтез — это биологическое преобразование световой энергии (то есть электромагнитной энергии) Солнца в химическую энергию растений. Это чрезвычайно сложный процесс, и его тщательное рассмотрение требует большого количества технической терминологии. Хотя мы обсудим основы фотосинтеза позже в этом эссе, мы сделаем это лишь очень поверхностно.
Проще говоря, фотосинтез — это биологическое преобразование световой энергии (то есть электромагнитной энергии) Солнца в химическую энергию растений. Это чрезвычайно сложный процесс, и его тщательное рассмотрение требует большого количества технической терминологии. Хотя мы обсудим основы фотосинтеза позже в этом эссе, мы сделаем это лишь очень поверхностно.
Фотосинтез включает превращение углекислого газа и воды в сахара, которые, наряду с крахмалом и целлюлозой, являются одними из наиболее известных разновидностей углеводов.Сахар можно определить как любое из ряда водорастворимых соединений различной сладости. (То, что мы считаем сахаром, то есть столовым сахаром, на самом деле является сахарозой, о чем будет сказано ниже.) Крахмалы — это сложные углеводы без вкуса и запаха, которые в физической форме являются гранулированными или порошкообразными. Целлюлоза — это полисахарид, состоящий из единиц глюкозы, который составляет основную часть клеточных стенок растений и естественным образом содержится в волокнистых материалах, таких как хлопок. В коммерческом отношении это сырье для таких промышленных товаров, как бумага, целлофан и вискоза.
В коммерческом отношении это сырье для таких промышленных товаров, как бумага, целлофан и вискоза.
МОНОСАХАРИДЫ.
Предыдущие определения содержат несколько слов, которые также должны быть определены. Углеводы состоят из строительных блоков, называемых моносахаридами, самого простого типа углеводов. Содержащиеся в винограде и других фруктах, а также в меде, они могут быть химически расщеплены на составляющие их элементы, но нет углеводов более простых в химическом отношении, чем моносахариды. Следовательно, они также известны как простые сахара или простые углеводы.
Примеры простых сахаров включают глюкозу, которая является сладкой, бесцветной и водорастворимой, широко распространенной в природе.Глюкоза, также известная как декстроза, виноградный сахар и кукурузный сахар, является основной формой, в которой углеводы усваиваются или поглощаются животными. Другие моносахариды
включают фруктозу или фруктовый сахар и галактозу, которая менее растворима и сладка, чем глюкоза, и обычно появляется в сочетании с другими простыми сахарами, а не сама по себе. Глюкоза, фруктоза и галактоза являются изомерами, что означает, что они имеют одинаковую химическую формулу (C 6 H 12 O 6 ), но разные химические структуры и, следовательно, разные химические свойства.
Глюкоза, фруктоза и галактоза являются изомерами, что означает, что они имеют одинаковую химическую формулу (C 6 H 12 O 6 ), но разные химические структуры и, следовательно, разные химические свойства.
ОТКАЗЫВАЕТСЯ.
Когда две молекулы моносахарида химически связываются друг с другом, в результате получается один из трех основных типов сложного сахара: дисахарид, олигосахарид или полисахарид. Дисахариды или двойные сахара состоят из двух моносахаридов. Безусловно, наиболее известным примером дисахарида является сахароза или столовый сахар, который образуется в результате связывания молекулы глюкозы с молекулой фруктозы. Сахарная свекла и тростниковый сахар являются основными естественными источниками сахарозы, с которой средний американец, скорее всего, столкнется в очищенной форме, такой как белый, коричневый или сахарная пудра.
Другой дисахарид — это лактоза или молочный сахар, единственный тип сахара, который производится из животных (т. Е. Из млекопитающих), а не из растительных источников. Мальтоза, сбраживаемый сахар, обычно образующийся из крахмала под действием фермента амилазы, также является дисахаридом. Сахароза, лактоза и мальтоза являются изомерами с формулой C 12 H 22 O 11 .
ОЛИГОСАХАРИДЫ И ПОЛИСАХАРИДЫ.
Определения олигосахарида и полисахарида настолько близки, что могут ввести в заблуждение.Олигосахарид иногда определяется как углевод, содержащий известное небольшое количество моносахаридных единиц, в то время как полисахарид представляет собой углевод, состоящий из двух или более моносахаридов. Теоретически это означает практически то же самое, но на практике олигосахарид содержит 3-6 моносахаридных единиц, тогда как полисахарид состоит из более чем шести.
Олигосахариды редко встречаются в природе, хотя было обнаружено несколько форм растений. Гораздо более распространены полисахариды («многие сахара»), которые составляют подавляющее большинство типов углеводов, встречающихся в природе.(См. Раздел «Где узнать больше о номенклатуре углеводов» на веб-сайте химического факультета Колледжа королевы Марии Лондонского университета. Взгляд на этот сайт позволит кое-что узнать о многих, многих разновидностях углеводов.)
Полисахариды может быть очень большим, состоящим из 10000 моносахаридных единиц, соединенных вместе. Учитывая такой широкий диапазон размеров, неудивительно, что существуют сотни типов полисахаридов, которые отличаются друг от друга размером, сложностью и химическим составом.Сама целлюлоза представляет собой полисахарид, наиболее распространенную из известных разновидностей, состоящий из многочисленных единиц глюкозы, соединенных друг с другом. Крахмал и гликоген также являются полисахаридами глюкозы. Первый из этих полисахаридов содержится в основном в стеблях, корнях и семенах растений. Что касается гликогена, это наиболее распространенная форма, в которой углеводы хранятся в тканях животных, особенно в тканях мышц и печени.
Фотосинтез
Фотосинтез, как мы отметили ранее, представляет собой биологическое преобразование света или электромагнитной энергии Солнца в химическую энергию.Встречается в зеленых растениях, водорослях и некоторых типах бактерий. и требует ряда биохимических реакций. У высших растений есть структуры, называемые хлоропластами, которые содержат темно-зеленый или сине-черный химикат, известный как хлорофилл. Поглощение света хлорофиллом катализирует или ускоряет процесс фотосинтеза. (Катализатор — это вещество, которое ускоряет химическую реакцию, не участвуя в ней.)
При фотосинтезе углекислый газ и вода реагируют друг с другом в присутствии света и хлорофилла с образованием простых углеводов и кислорода.Это одно из тех утверждений в области науки, которые на первый взгляд кажутся немного сухими и скучными, но на самом деле заключают в себе одну из величайших загадок жизни — концепцию, гораздо более увлекательную, чем любое количество воображаемых, фантастических или псевдонаучных идей. можно было придумать. Фотосинтез — один из важнейших процессов поддержания жизни, который делает возможным питание всех вещей и дыхание животных и других организмов, дышащих кислородом.
При фотосинтезе растения поглощают продукты жизнедеятельности человека и животных и в результате ряда химических реакций производят как пищу, так и кислород.Пища питает растение, которое, в отличие от животного, способно производить собственное питание из собственного тела с помощью только солнечного света и нескольких химических соединений. Позже, когда растение будет съедено животным или когда оно умрет и будет съедено бактериями и другими разрушителями, оно передаст свои углеводы другим существам. (См. «Пищевые сети», чтобы узнать больше о растениях как автотрофах и взаимоотношениях между первичными продуцентами, потребителями и деструкторами.)
Углеводы — не единственный полезный продукт фотосинтетической реакции.В результате реакции образуется чрезвычайно важный побочный продукт — отходы, то есть с точки зрения предприятия, которому кислород не нужен. Тем не менее, кислород, который он генерирует в процессе фотосинтеза, делает возможной жизнь животных и многих одноклеточных форм жизни, дыхание которых зависит от кислорода.
УРАВНЕНИЕ ФОТОСИНТЕЗА.
Реакцию фотосинтеза можно представить в виде химического уравнения:
Обратите внимание, что стрелка указывает на то, что химическая реакция произошла с помощью света и хлорофилла.Таким же образом может потребоваться тепло от горелки Бунзена для инициирования какой-либо другой химической реакции, которая фактически не является частью реагентов слева от стрелки. В данном уравнении ни добавленная энергия, ни катализатор не отображаются слева, потому что они не являются физическими участниками, потребляемыми в реакции, как диоксид углерода и вода. Катализатор не участвует в реакции, тогда как энергия, потребляемая в реакции, не является материальным или физическим участником, то есть это энергия, а не материя.
Можно также задаться вопросом, почему уравнение показывает шесть молекул углекислого газа и шесть молекул воды. Почему не по одному для простоты? Чтобы составить сбалансированное химическое уравнение, в котором одинаковое количество атомов появляется по обе стороны стрелки, необходимо показать шесть молекул углекислого газа, вступающих в реакцию с шестью молекулами воды с образованием шести молекул кислорода и одной молекулы глюкозы. Таким образом, обе стороны содержат шесть атомов углерода, 12 атомов водорода и 18 атомов кислорода.
Уравнение создает впечатление, что фотосинтез — это простой одноэтапный процесс, но ничто не может быть дальше от истины.Фактически, процесс происходит по одному маленькому шагу за раз. Он также включает в себя множество тонкостей и аспектов, требующих введения множества новых терминов и идей. Такое обсуждение выходит за рамки настоящего эссе, и поэтому читателю рекомендуется обратиться к надежному учебнику для получения дополнительной информации о деталях фотосинтеза.
ПРИМЕНЕНИЕ В РЕАЛЬНОМ ЖИЗНИ
Фрукты и овощи
Один из основных способов, которыми люди получают углеводы из своего рациона, — это фрукты и овощи.Различия между ними основаны не на науке, а на обычае. Традиционно овощи — это растительные ткани (которые могут быть сладкими, но обычно не сладкими), которые едят как существенную часть основного блюда. Напротив, фрукты почти всегда сладкие и их едят как десерты или закуски. Бывает также, что люди гораздо чаще готовят овощи, чем фрукты, хотя овощи лучше всего питаются, когда их едят в сыром виде.
Фрукты и овощи содержат большое количество углеводов в виде пищевых сахаров и крахмалов, а также несъедобной целлюлозы, роль которой в рационе питания будет рассмотрена позже.В свежем овоще, например, вода может составлять около 70% объема, а белки, жиры, витамины и минералы могут составлять немногим более 5%, причем почти 25% приходится либо на съедобные сахара и крахмалы, либо на несъедобные целлюлозные волокна. .
ПРИМЕР АРТИШОКА.
Каждый фрукт или овощ, который можно было бы съесть — а их сотни — содержат как съедобные углеводы, которые являются хорошим источником энергии, так и несъедобные, которые содержат клетчатку. Прекрасным примером этой съедобно-несъедобной смеси является земной шар или французский артишок — Cynara scolymus, член семейства сложноцветных, в которое входит подсолнечник.Шаровидный артишок (не путать с топинамбуром или Helianthus tuberosus ) появляется в виде соцветия или грозди цветов. Этот овощ обычно готовят на пару, а прицветники или листья обмакивают в сливочном масле или другом соусе.
Однако не все прицветники съедобны; Чтобы съесть крахмалистое «мясо» артишока, которое имеет характерный ореховый вкус, нужно протянуть листья между зубцами. Таким образом, большая часть лучших частей артишока скрыта, а лучшая часть всего — нежное и полностью съедобное «сердце» — заключено под устрашающим щитом из тонкого чертополоха.Тот, кто первым открыл, что артишок можно есть, должен был быть действительно храбрым человеком, и тот, кто выяснил, , как его есть, был мудр. Благодаря этим душам, любящим приключения, кухня мира стала незабываемым деликатесом.
СОДЕРЖАНИЕ УГЛЕВОДОВ В ОВОЩАХ.
По содержанию пищевых углеводов артишок имеет низкий процент. Некоторые овощи содержат меньший процент углеводов, в то время как другие имеют гораздо более высокий процент, как показывает приведенный здесь список.В целом кажется, что содержание углеводов в овощах (и в каждом из этих случаев мы говорим о съедобных углеводах, , а не целлюлозе) находится в диапазоне примерно 5-10%, примерно 20% или очень высоком уровне. 60-80%. Кажется, что в этих диапазонах нет большого разброса.
Содержание воды, белка и углеводов в отобранных овощах:
- Артишок: 85% воды, 2,9% белка, 10,6% углеводов
- Свекла красная: 87,3% воды, 1.6% белка, 9,9% углеводов
- Сельдерей: 94,1% воды, 0,9% белка, 3,9% углеводов
- Кукуруза: 13,8% воды, 8,9% белка, 72,2% углеводов
- Лима: 10,3% воды, 20,4% белка, 64% углеводов
- Картофель: 79,8% воды, 2,1% белка, 17,1% углеводов
- Красный перец: 74,3% воды, 3,7% белка, 18,8% углеводов
- Летние кабачки: 94% воды, 1,1% белка, 4,2% углеводов
Крахмалы
Не все углеводы в этих овощах одинаковы.Некоторые углеводы представлены в виде сахара, а другие — в виде несъедобной целлюлозы, что обсуждается в следующем разделе. Кроме того, некоторые овощи содержат много крахмала. Как мы отмечали ранее, крахмал белый и гранулированный, и, в отличие от сахаров, крахмал не может быть растворен в холодной воде, спирте или других жидкостях, которые обычно действуют как растворители.
Крахмал, производимый из листьев растений, является продуктом избытка глюкозы, образующейся во время фотосинтеза, и обеспечивает растение запасом продовольствия в хлоропластах на случай чрезвычайной ситуации.Овощи с высоким содержанием крахмала — это продукты растений, содержащие крахмал в тех порциях, которые мы едим. Например, клубень или подземная луковица картофеля, а также семена кукурузы, пшеницы и риса. Таким образом, все эти овощи и продукты, полученные из них, содержат много углеводов в форме крахмала.
Помимо своей роли в рационе человека, кукурузный, пшеничный, тапиоковый и картофельный крахмалы находят множество коммерческих применений. Из-за его способности загущать жидкости и твердеть твердые вещества, крахмал применяется в продуктах (например,g., кукурузный крахмал), которые действуют как загустители как для пищевых, так и для непищевых продуктов. Крахмал также широко используется на различных этапах производства одежды и в производстве одежды для придания жесткости тканям. При производстве бумаги крахмал используется для увеличения прочности бумаги. Он также используется в производстве картонных и бумажных пакетов.
Целлюлоза
Одним из аспектов фруктов и овощей, о котором мы упоминали несколько раз, является высокое содержание несъедобного материала или целлюлозы.(На самом деле, это съедобно, но не усваивается.) Целлюлоза, содержащаяся в клеточных стенках растений, химически похожа на крахмал, но еще более жесткая, и это свойство делает ее отличным веществом для придания силы растительным телам. У животных нет жестких клеток с стенками, но у растений они есть. Высокое содержание целлюлозы в клеточных стенках растений придает им прямостоячую жесткую форму; другими словами, без целлюлозы растения могут быть вялыми и частично бесформенными. Как и человеческая кость, стенки растительных клеток состоят из фибрилл (мелких нитей или волокон), которые включают многочисленные полисахариды и белки.Одним из этих полисахаридов в клеточных стенках является пектин, вещество, которое при нагревании образует гель и используется поварами для приготовления желе и джемов. У некоторых деревьев есть вторичная клеточная стенка над первичной, содержащая еще один полисахарид, называемый лигнином . Лигнин делает дерево еще более жестким, проницаемым только острыми топорами.
ЦЕЛЛЮЛОЗА В ПИЩЕВАРЕНИИ.
Как мы уже отмечали, целлюлоза богата фруктами и овощами, но людям не хватает фермента, необходимого для ее переваривания.Термиты, коровы, коалы и лошади переваривают целлюлозу, но даже эти животные а у насекомых нет фермента, который переваривает этот материал. Вместо этого они скрывают в своем кишечнике микробы, которые могут за них переваривать пищу. (Это пример симбиотического мутуализма, взаимовыгодных отношений между организмами, обсуждаемых в «Симбиозе».)
Коровы — жвачные животные, или животные, которые жуют свою жвачку, то есть пищу, которую отрыгивают, чтобы ее снова пережевывать. У жвачных животных есть несколько желудков или несколько отделов желудка, которые расщепляют растительный материал с помощью ферментов и бактерий.Затем частично переваренный материал срыгивает в рот, где его пережевывают, чтобы еще больше разложить материал. (Если вы когда-либо наблюдали за коровами на пастбище, вы, вероятно, наблюдали, как они спокойно жуют жвачку.) Переваривание клетчатки бактериями в желудках жвачных животных является анаэробным, то есть для этого процесса не требуется кислород. Одним из побочных продуктов этого анаэробного процесса является метан, который имеет неприятный запах, легко воспламеняется и токсичен. Жвачные животные ежедневно выделяют большое количество метана, что обеспокоило некоторых экологов, поскольку метан, переносимый коровами, может вносить свой вклад. к разрушению озона высоко в стратосфере Земли.
Целлюлоза Alhough неперевариваема человеком, она является важным диетическим компонентом, так как способствует пищеварению. Целлюлоза, которую иногда называют клетчаткой или грубыми кормами, помогает придать пище объемный вес при ее прохождении через пищеварительную систему и помогает организму вытеснять пищу и отходы. Это особенно важно, поскольку помогает сделать возможной регулярную дефекацию, тем самым избавляя организм от шлаков и снижая риск рака толстой кишки. (См. Пищеварение для получения дополнительной информации о пищеварительных и выделительных процессах.)
Общее углеводное питание
Диета с высоким содержанием целлюлозы может быть полезной по причинам, которые мы указали. Точно так же здоровая диета включает питательные углеводы, но только при определенных условиях. Прежде всего, это должно быть поняли, что человеческий организм не имеет необходимой потребности в углеводах сами по себе — другими словами, нет «незаменимых» углеводов, поскольку есть незаменимые аминокислоты или жирные кислоты.
С другой стороны, очень важно есть свежие фрукты и овощи, которые, как мы видели, богаты углеводами.Их значение имеет мало общего с содержанием углеводов в питательных веществах, а скорее с витаминами, минералами, белками и пищевыми волокнами, которые они содержат. Эти полезные углеводы лучше всего есть в максимально естественной форме: например, есть апельсин целиком, а не просто выжать сок и выбросить мякоть. Кроме того, сырой шпинат и другие овощи содержат гораздо больше витаминов и минералов, чем приготовленные.
САХАР ВЫСОКОГО ХРАНЕНИЯ ЖИРА.
Углеводы могут короткий прилив энергии, поэтому спортсмены могут «набрать углеводы» прямо перед соревнованиями. Но если углеводы не сжигаются быстро, они в конечном итоге откладываются в виде жира. Так обстоит дело даже со здоровыми углеводами, но гораздо хуже обстоит дело с углеводами нездоровой пищи, которые содержат только пустые калории, лишенные содержания витаминов и минералов. Одним из примеров является особый бренд шоколадных батончиков, который на протяжении многих лет рекламировался в рекламе как средство получения быстрого прилива энергии.Фактически, эта и все другие леденцы на основе белого сахара дают только быстрый «высокий уровень сахара», за которым почти сразу следует гораздо более низкий «минимум» энергии — и, в конечном итоге, происходит накопление жира.
Жир — единственная форма, в которой организм может хранить углеводы в течение длительного времени, а это означает, что «обезжиренные» наклейки на многих упаковках печенья или пирожных в супермаркете так же бессмысленны, как и сами калории. Потребление углеводов — одна из основных причин, по которой средний американец имеет такой избыточный вес.При активном образе жизни, который типичен для большинства взрослых в современной жизни, все эти картофель фри, печенье, булочки и т. Д. Не имеют места, кроме центров накопления жира в области живота, ягодиц и бедер. Из всех продуктов, содержащих углеводы, наименее жирными, конечно, являются натуральные некрахмалистые продукты, такие как фрукты и овощи (при условии, что они не приготовлены с жиром). Следующим в списке наименее калорийных продуктов являются крахмалистые натуральные продукты, такие как картофель, а наиболее жирными из всех являются обработанные крахмалы, будь то рис, пшеница или картофельные продукты.
ПОЧЕМУ ВЫ МОЖЕТЕ ЕСТЬ БОЛЬШЕ УГЛЕВОДОВ, ЧЕМ БЕЛКОВ.
Одна из самых больших проблем, связанных с крахмалом, заключается в том, что организм может потреблять их так много по сравнению с белками и жирами. Сколько раз вы ели огромную тарелку картофельного или рисового пюре, горы картошки фри или кусок за куском хлеба? Все мы сделали это: углеводы и особенно крахмалы, кажется, никогда не смогут насытиться. Но сколько раз вы ели огромную тарелку только курицы, стейка или яиц? Вероятно, не очень часто, и если вы пытались съесть слишком много этих продуктов с высоким содержанием белка за один раз, вы, скорее всего, начали болеть.
Причина в том, что когда вы едите белок или жир, он вызывает высвобождение гормона под названием холецистокинин (CCK) в тонком кишечнике. По сути, CCK сообщает мозгу о том, что тело получает питание, и, если выделяется достаточное количество CCK, он сигнализирует мозгу о том, что организм получил достаточно пищи. Если человек продолжит потреблять белки или жиры после этого, скорее всего, последует тошнота. Углеводы, с другой стороны, не вызывают высвобождения ХЦК; только когда они попадают в кровоток, они наконец посылают в мозг сигнал о том, что тело удовлетворено.К тому времени большинство из нас накопило больше картофельного пюре, которому суждено занять свое место в организме в качестве жировых отложений.
ГДЕ УЗНАТЬ БОЛЬШЕ
Углеводы. Hardy Research Group, химический факультет Университета Акрона (веб-сайт).
Дей, П. М. и Р. А. Диксон. Биохимия запасных углеводов в зеленых растениях. Орландо, Флорида: Academic Press, 1985.
Carpi, Anthony.«Пищевая химия: углеводы». Visionlearning.com (веб-сайт).
Food Resource, Государственный университет Орегона (веб-сайт).
Кеннеди, Рон. «Углеводы в питании». Медицинская библиотека врачей (веб-сайт).
«Номенклатура углеводов». Колледж Королевы Марии Лондонского университета, факультет химии (веб-сайт).
Снайдер, Карл Х. Необычная химия обычных вещей. New York: John Wiley and Sons, 1998.
Spallholz, Julian E. Nutrition, Chemistry, and Biology. Englewood Cliffs, NJ: Prentice-Hall, 1989.
Wiley, T. S., and Bent Formby. Отключение света: сон, сахар и выживание. New York: Pocket Books, 2000.
КЛЮЧЕВЫЕ ТЕРМИНЫ
УГЛЕВОДЫ:
Кольцевые соединения природного происхождения, состоящие из углерода, водорода и кислорода, основная функция которых в организме — обеспечение энергией.В группу углеводов входят сахара, крахмалы, целлюлоза и различные другие вещества. Большинство углеводов вырабатываются зелеными растениями в процессе фотосинтеза.
КАТАЛИЗАТОР:
Вещество, которое ускоряет химическую реакцию, не участвуя в ней. Таким образом, катализаторы, хорошим примером которых являются ферменты, не расходуются в реакции.
ЦЕЛЛЮЛОЗА:
Полисахарид, состоящий из единиц глюкозы, которая является основным материалом в клеточных стенках растений.Целлюлоза также содержится в натуральных волокнах, таких как хлопок, и используется в качестве сырья при производстве таких продуктов, как бумага.
КОМПЛЕКСНЫЙ УГЛЕВОДНЫЙ:
Дисахарид, полисахарид или олигосахарид. Также называется сложным сахаром .
DEXTROSE:
Другое название глюкозы.
ДИСАХАРИД:
Двойной сахар, состоящий из двух моносахаридов. Примеры дисахаридов включают изомеры сахарозы, мальтозы и лактозы.
ФЕРМЕНТ:
Белковый материал, ускоряющий химические реакции в организме растений и животных.
ФРУКТОЗА:
Фруктовый сахар, моносахарид, являющийся изомером глюкозы.
ГАЛАКТОЗА:
Моносахарид и изомер глюкозы. Менее растворимая и сладкая, чем глюкоза, галактоза обычно появляется в сочетании с другими простыми сахарами, а не сама по себе.
ГЛЮКОЗА:
Моносахарид, который широко встречается в природе и представляет собой форму, в которой животные обычно получают углеводы.Также известен как декстроза, виноградный сахар и кукурузный сахар.
ГЛИКОГЕН:
Белый полисахарид, который является наиболее распространенной формой хранения углеводов в тканях животных, особенно в тканях мышц и печени.
GUT:
Термин, обозначающий весь или часть пищеварительного тракта, по которому пища проходит изо рта в кишечник, а отходы — из кишечника в задний проход. Хотя в повседневной жизни это слово считается несколько грубым, врачи и ученые-биологи, занимающиеся этой частью анатомии, используют его регулярно.
ИЗОМЕРЫ:
Два вещества, которые имеют одинаковую химическую формулу, но различаются по химической структуре и, следовательно, по химическим свойствам.
ЛАКТОЗА:
Молочный сахар. Дисахаридный изомер сахарозы и мальтозы, лактоза является единственным основным типом сахара, который производится из животных (т. Е. Из млекопитающих), а не из растительных источников.
МАЛЬТОЗА:
Ферментируемый сахар, обычно образующийся из крахмала под действием фермента амилазы. Мальтоза представляет собой дисахаридный изомер сахарозы и лактозы.
МОНОСАХАРИД:
Самый простой вид углеводов. Моносахариды, которые не могут быть химически расщеплены на более простые углеводы, также известны как простые сахара. Примеры моносахаридов включают изомеры глюкозы, фруктозы и галактозы.
ОЛИГОСАХАРИД:
Углевод, содержащий известное небольшое количество моносахаридных единиц, обычно от трех до шести. Сравните с полисахаридом .
ФОТОСИНТЕЗ:
Биологическое преобразование световой энергии (то есть электромагнитной энергии) Солнца в химическую энергию в растениях.В этом процессе углекислый газ и вода превращаются в углеводы и кислород.
ПОЛИСАХАРИД:
Углевод, состоящий из более чем шести моносахаридов. Иногда полисахарид определяется как содержащий два или более моносахаридов, но это определение мало чем отличается от олигосахарида .
САХАРИД:
Сахар.
ПРОСТОЙ САХАР:
Моносахарид или простой углевод.
КРАХМАЛЫ:
Сложные углеводы без вкуса и запаха, гранулированные или порошкообразные в физической форме.
СУКРОЗА:
Обычный столовый сахар (C 12 H 22 O 11 ), дисахарид, образованный в результате связывания молекулы глюкозы с молекулой фруктозы. Сахарная свекла и тростниковый сахар являются основными естественными источниками сахарозы, с которой средний американец, скорее всего, столкнется в очищенной форме, такой как белый, коричневый или сахарная пудра.
САХАР:
Один из трех основных типов углеводов, наряду с крахмалом и целлюлозой.Сахар можно определить как любой из различных водорастворимых углеводов различной сладости. То, что мы называем сахаром (то есть столовым сахаром), на самом деле является сахарозой.
Историческая справка и обзор — Основы гликобиологии
В этой главе содержится историческая справка по области гликобиологии и обзор этой книги. Рассмотрены общие термины, встречающиеся в томе, упомянутые общие моносахаридные единицы гликоконъюгатов, а также представлена единообразная номенклатура символов, используемых для структурных изображений.Описаны основные классы гликанов, обсуждаемые в книге, и дан обзор общих путей их биосинтеза. Также рассматриваются топологические вопросы, связанные с биосинтезом и функциями гликоконъюгатов, и отмечается растущая роль этих молекул в медицине, биотехнологии, нанотехнологиях, биоэнергетике и материаловедении.
ЧТО ТАКОЕ ГЛИКОБИОЛОГИЯ?
В самом широком смысле гликобиология — это изучение структуры, биосинтеза, биологии и эволюции сахаридов (также называемых углеводами, сахарными цепями или гликанами), которые широко распространены в природе, и белков, которые их распознают.Как гликобиология вписывается в современные концепции молекулярной биологии? Центральная парадигма исследований в области молекулярной биологии заключалась в том, что биологическая информация перетекает от ДНК к РНК и белку. Сила этой концепции заключается в ее основанной на шаблонах точности, способности манипулировать одним классом молекул на основе знания о другом, а также в моделях гомологии и родства последовательностей, которые предсказывают функцию и выявляют эволюционные отношения. Благодаря продолжающемуся секвенированию многочисленных геномов достигнут впечатляющий прогресс в понимании биологии нуклеиновых кислот и белков.Таким образом, многие ученые предполагают, что изучение именно этих молекул объяснит состав клеток, тканей, органов, физиологических систем и интактных организмов. Фактически, для создания клетки требуется множество низкомолекулярных метаболитов, а также два других основных класса макромолекул — липиды и углеводы, которые служат в качестве промежуточных звеньев в производстве энергии и в качестве сигнальных эффекторов, маркеров распознавания и структурных компонентов. Взятые вместе с тем фактом, что они охватывают некоторые из основных посттрансляционных модификаций белков, липидов и углеводов, помогают объяснить, как относительно небольшое количество генов в типичном геноме может порождать огромные биологические сложности, присущие развитию, росту и функционированию различных организмы.
Биологические роли углеводов особенно заметны в сборке сложных многоклеточных органов и организмов, что требует взаимодействия между клетками и окружающей матрицей. Все без каких-либо известных исключений все клетки и многочисленные макромолекулы в природе несут набор ковалентно связанных сахаров (моносахаридов) или сахарных цепей (олигосахаридов), которые в этой книге обычно называются «гликанами». Иногда гликаны также могут быть автономными объектами.Находясь на внешней поверхности клеточных и секретируемых макромолекул, многие гликаны способны модулировать или опосредовать различные события во взаимодействиях клетка-клетка, клетка-матрица и клетка-молекула, критически важных для развития и функционирования сложного многоклеточного организма. . Они также могут опосредовать взаимодействия между организмами (например, между хозяином и паразитом, патогеном или симбионтом). Кроме того, простые, быстро обновляющиеся гликаны, связанные с белками, широко распространены в ядре и цитоплазме, где они могут служить регуляторными переключателями.Следовательно, более полная парадигма молекулярной биологии должна включать гликаны, часто в ковалентной комбинации с другими макромолекулами (т.е. гликоконъюгатами, такими как гликопротеины и гликолипиды). По аналогии с нынешней ситуацией в космологии, гликаны можно рассматривать как «темную материю» биологической вселенной: главный и критический компонент, который еще не полностью включен в «стандартную модель» биологии.
Химия и метаболизм углеводов вызывали большой интерес в первой половине 20 века.Несмотря на то, что они привлекали большое внимание, они в первую очередь рассматривались как источник энергии или как конструкционные материалы, явно лишенные другой биологической активности. Более того, во время революции в молекулярной биологии 1970-х годов исследования гликанов сильно отставали от исследований других основных классов молекул. Частично это было из-за присущей им структурной сложности, сложности определения их последовательностей и того факта, что их биосинтез нельзя было напрямую предсказать по матрице ДНК.Развитие многих новых технологий для исследования структур и функций гликанов с тех пор открыло новый рубеж молекулярной биологии, получивший название «гликобиология» — слово, впервые появившееся в конце 1980-х годов для обозначения объединения традиционных дисциплин химии углеводов и биохимии. с современным пониманием клеточной и молекулярной биологии гликанов и, в частности, их конъюгатов с белками и липидами. Гликобиология в настоящее время является одной из наиболее быстро развивающихся областей естественных наук, имеющей широкое отношение ко многим областям фундаментальных исследований, биомедицины и биотехнологии.Эта область включает химию углеводов, энзимологию образования и деградации гликанов, распознавание гликанов определенными белками, роль гликанов в сложных биологических системах, а также их анализ или манипулирование различными методами. Таким образом, исследования в области гликобиологии требуют основы не только в области номенклатуры, биосинтеза, структуры, химического синтеза и функций гликанов, но также и в общих дисциплинах молекулярной генетики, химии белков, клеточной биологии, биологии развития, физиологии и медицине.Эта книга представляет собой обзор этой области с относительным акцентом на гликаны животных систем. Предполагается, что читатель имеет базовые знания в области химии, биохимии и клеточной биологии на уровне бакалавриата. Некоторые из основных исследователей, которые повлияли на раннее развитие гликобиологии, показаны здесь, а другие перечислены в онлайн-приложении 1A. Многие другие также внесли значительный вклад, и краткое изложение общих принципов, извлеченных из всех этих исследований, представлено в.
РИСУНОК 1.1.
Нобелевские лауреаты в областях, связанных с историей гликобиологии. Перечислены лауреаты и их оригинальные Нобелевские цитаты: Герман Эмиль Фишер (химия, 1902), «в знак признания выдающихся заслуг, которые он оказал своей работой над (подробнее …)
МОНОСАХАРИДЫ ЯВЛЯЮТСЯ ОСНОВНОЙ СТРУКТУРНОЙ ЕДИНИЦЕЙ GLYCANS
Углеводы определяются как полигидроксиальдегиды, полигидроксикетоны и их простые производные или более крупные соединения, которые можно гидролизовать до таких единиц.Моносахарид — это углевод, который обычно не может быть гидролизован до более простой формы. Он имеет потенциальную карбонильную группу на конце углеродной цепи (альдегидная группа) или у внутреннего углерода (кетонная группа). Поэтому эти два типа моносахаридов называются альдозами и кетозами соответственно (примеры см. Ниже, а более подробную информацию см. В главе 2). Свободные моносахариды могут существовать в форме с открытой цепью или в форме кольца (). Кольцевые формы моносахаридов являются правилом для олигосахаридов, которые представляют собой линейные или разветвленные цепи моносахаридов, связанных друг с другом через гликозидные связи (термин «полисахарид» обычно используется для больших гликанов, состоящих из повторяющихся олигосахаридных мотивов; например, см. Главу 3 ).Кольцевая форма моносахарида генерирует хиральный аномерный центр на C-1 для альдосахаров или на C-2 для кетосахаров (подробности см. В главе 2). Гликозидная связь включает присоединение моносахарида к другому остатку, обычно через гидроксильную группу этого аномерного центра, с образованием α-связей или β-связей, которые определяются на основе отношения гликозидного кислорода к аномерному атому углерода и кольцу (Глава 2). Эти два типа связи придают очень разные структурные свойства и биологические функции последовательностям, которые в остальном идентичны по составу, что классически иллюстрируется различиями между крахмалом и целлюлозой (оба являются гомополимерами глюкозы, первый в значительной степени связан с α1-4, а второй — с β1. -4-связаны повсюду).Гликоконъюгат — это соединение, в котором одна или несколько моносахаридных или олигосахаридных единиц (гликон) ковалентно связаны с неуглеводным фрагментом (агликоном). Олигосахарид, не связанный с агликоном, обладает восстанавливающей способностью альдегида или кетона в его концевом моносахаридном компоненте, за исключением олигосахаридов, в которых сахара связаны вместе своими восстанавливающими концами, как в производных сахарозы или трегалозы. Конец гликана, открывающий альдегидную или кетоновую группу, поэтому называется восстанавливающим концом или восстанавливающим концом, термины, которые обычно используются, даже когда сахарная цепь присоединена к агликону и, таким образом, утратила свою восстанавливающую способность.Соответственно, противоположный конец цепи обычно называют невосстанавливающим концом (обратите внимание на аналогию с амино- и карбоксильными концами белков или 5′- и 3′-концами ДНК и РНК).
РИСУНОК 1.2.
Открытоцепочечные и кольцевые формы глюкозы. Изменения в ориентации гидроксильных групп вокруг определенных атомов углерода генерируют новые молекулы, которые имеют отличную биологию и биохимию (например, галактоза является эпимером C-4 глюкозы). В кольцевой форме глюкоза (подробнее …)
ГЛИКАНЫ МОГУТ СОСТАВЛЯТЬ ОСНОВНУЮ ЧАСТЬ МАССЫ ГЛИКОКОНЬЮГАТА
В встречающихся в природе гликоконъюгатах часть молекулы, включающая гликаны, может сильно различаться по вкладу в ее общий размер. .Во многих случаях гликаны составляют значительную часть массы гликоконъюгатов (для типичного примера см.). По этой причине поверхности всех типов клеток в природе (которые сильно украшены различными видами гликоконъюгатов) эффективно покрыты плотным массивом сахаров, так называемым «гликокаликсом». Эта структура клеточной поверхности была впервые обнаружена много лет назад электронными микроскопистами как полисахаридное покрытие, внешнее по отношению к мембране клеточной поверхности у бактерий, которое могло быть окрашено рутениевым красным, и в клетках животных, где анионные полисахариды на поверхности могли быть украшены поликатионными реагентами, такими как катионизированный ферритин (классические и недавние примеры см.).Плотность гликанов в гликокаликсе может быть очень высокой. Например, было подсчитано, что концентрация сиаловых кислот в гликокаликсе типичного В-лимфоцита человека может быть> 100 мм.
РИСУНОК 1.3.
Схематическое изображение гликопротеина Thy-1, включая три N-гликана ( синий ) и липидный якорь гликозилфосфатидилинозитол (GPI-гликан; зеленый ), ацильные цепи которого ( желтый ) обычно встроены в мембрану двухслойный.Обратите внимание, что полипептид (подробнее …)
РИСУНОК 1.4.
( Верхний левый ) Историческая электронная микрофотография эндотелиальных клеток из кровеносного капилляра в мышце диафрагмы крысы, показывающая клеточную мембрану клеток (обращенных к крови), украшенную частицами катионизированного ферритина ( наконечников стрелок ). Эти (подробнее …)
МОНОСАХАРИДЫ МОГУТ БЫТЬ СВЯЗАНЫ ВМЕСТЕ БОЛЬШЕ, ЧЕМ АМИНОКИСЛОТ ИЛИ НУКЛЕОТИДЫ
Нуклеотиды и белки представляют собой линейные полимеры, каждый из которых может содержать только один базовый тип связи между мономерами.Напротив, каждый моносахарид теоретически может генерировать α- или β-связь с любым одним из нескольких положений на другом моносахариде в цепи или с другим типом молекулы. Таким образом, хотя три разных нуклеотида или аминокислоты могут генерировать только шесть тримеров, три различных гексозы теоретически могут давать (в зависимости от того, какие из их форм рассматриваются) от 1056 до 27 648 уникальных трисахаридов. Эта разница в сложности становится еще больше по мере увеличения количества моносахаридных единиц, обнаруженных в природном гликане (теперь их количество исчисляется сотнями).К счастью для изучающих гликобиологию, встречающиеся в природе биологические макромолекулы данного вида, как правило, содержат относительно мало возможных моносахаридных единиц, и они находятся в ограниченном количестве комбинаций. Конечно, подавляющее большинство гликанов у большинства видов еще не обнаружено и структурно не определено. Таким образом, большая часть возможного разнообразия еще может существовать в природе.
ОБЩИЕ МОНОСАХАРИДНЫЕ ЕДИНИЦЫ ГЛИКОКОНЪЮГАТОВ
Хотя в природе известно несколько сотен различных моносахаридов, лишь небольшая их часть обычно обнаруживается в хорошо изученных гликанах.Примеры распространенных моносахаридов в клетках позвоночных перечислены ниже вместе с их стандартными сокращениями (подробные сведения об их структурах см. В главе 2, а также ссылки на символы в онлайн-приложении 1B).
Пентозы : пятиуглеродные нейтральные сахара — D-ксилоза (Xyl)
Гексозы : шестиуглеродные нейтральные сахара, например, D-глюкоза (Glc)
Hexos : гексозы с аминогруппой в положении 2, которые могут быть свободными или, чаще, N-ацетилированными — например, N -ацетил-D-глюкозамин (GlcNAc)
6-дезоксигексозы : например, L-фукоза (Fuc)
Уроновые кислоты : гексозы с карбоксилатом в положении 6 — например, D-глюкуроновая кислота (GlcA)
- Нонулозоновые кислоты : семейство из девяти -углеродно-кислые сахара, из которых наиболее часто встречается у животных сиаловая кислота N -ацетилнейраминовая кислота (Neu5Ac, также иногда называемая NeuAc или, исторически, NANA) (см. главу 15)
Для простоты символы D- и L- опускаются в полных именах обычных m оносахариды, если не встречается менее распространенный вариант.Этот ограниченный набор моносахаридов доминирует в гликобиологии недавно эволюционировавших (так называемых «высших») животных, но несколько других были обнаружены у «низших» животных (например, тивелоза; главы 25 и 26), бактерий и архей (например, кетодезоксиоктулозоновая кислота, рамноза, L-арабиноза и мурамовая кислота; главы 21 и 22) и растения (например, арабиноза, апиоза и галактуроновая кислота; глава 24). Разнообразные модификации гликанов дополнительно увеличивают их разнообразие в природе и часто служат для опосредования определенных биологических функций.Таким образом, гидроксильные группы различных моносахаридов могут подвергаться модификациям, таким как фосфорилирование, сульфатирование, метилирование, O-ацетилирование или ацилирование жирных кислот. Хотя аминогруппы обычно N-ацетилированы, они могут быть N-сульфатированы или оставаться незамещенными. Карбоксильные группы иногда подвергаются лактонизации до близлежащих гидроксильных групп или даже лактамизации до близлежащих аминогрупп.
Подробности, касающиеся структурного описания моносахаридов, связей и олигосахаридов, обсуждаются в главе 2.Многие рисунки в этом томе используют символическое изображение сахарных цепочек (см. Онлайн-приложение 1B и примеры в). Эта номенклатура символов для гликанов (SNFG) является расширенной из Второго издания и была проверена и принята многими исследователями. Для удобства читателя полная таблица символов воспроизведена на внутренней стороне обложки книги, доступна для просмотра на веб-сайте NCBI Books Online, Приложение 1B, и может быть загружена в графическом и текстовом форматах с этого веб-сайта. Подробные примечания относительно логики, используемой для номенклатуры символов, также можно найти в онлайн-приложении 1B, вместе со встроенными ссылками на онлайн-базы данных, содержащими подробную информацию о каждом моносахариде, а также информацию о настройках цвета для художников, которые хотят использовать систему.
РИСУНОК 1.5.
Примеры символов и условных обозначений для рисования гликановых структур. Набор символов моносахаридов из Второго издания Essentials of Glycobiology остается неизменным, но был расширен для охвата более широкого диапазона моносахаридов, встречающихся в природе. Для (подробнее …)
ОСНОВНЫЕ КЛАССЫ ГЛИКОКОНЪЮГАТОВ И ГЛИКАНОВ
Общие классы гликанов в первую очередь определяются в соответствии с природой связи с агликоном (белком или липидом) (общие примеры эукариот см. В и).Гликопротеин представляет собой гликоконъюгат, в котором белок несет один или несколько гликанов, ковалентно связанных с основной цепью полипептида, обычно через N- или O-связи. N-гликан (N-связанный олигосахарид, N- [Asn] -связанный олигосахарид) представляет собой сахарную цепь, ковалентно связанную с остатком аспарагина полипептидной цепи, обычно включающую остаток GlcNAc в эукариоатах, и консенсусную пептидную последовательность: Asn- X-Ser / Thr. N-гликаны животных также имеют общую пентасахаридную центральную область и могут быть разделены на три основных класса: олигоманнозный (или высокоманнозный) тип, сложный тип и гибридный тип (глава 9).О-гликан (О-связанный олигосахарид) часто связан с полипептидом через N- ацетилгалактозамин (GalNAc) с гидроксильной группой остатка серина или треонина и может быть расширен на различные структурные основные классы (глава 10). Муцин — это большой гликопротеин, несущий множество сгруппированных (близко расположенных) О-гликанов. Также существует несколько других типов O-гликанов (например, O-связанная фукоза, глюкоза или манноза). Протеогликан — это гликоконъюгат, который имеет одну или несколько цепей гликозаминогликанов (GAG) (см. Определение ниже), прикрепленных к «коровому белку» через типичную сердцевинную область, которая имеет на своем восстанавливающем конце остаток ксилозы, связанный с гидроксильной группой остатка серина. .В остальном различие между протеогликаном и гликопротеином является произвольным, поскольку некоторые полипептиды протеогликана могут нести как цепи GAG, так и различные O- и N-гликаны (глава 17). Многие цитоплазматические и ядерные белки имеют один остаток GlcNAc на одном или нескольких остатках серина или треонина (глава 19). предоставляет список известных в природе гликан-белковых связей.
РИСУНОК 1.6.
Общие классы гликанов животных. (Изменено и обновлено из Варки А. 1997. FASEB J 11: 248–255; Fuster M, Esko JD. 2005. Nat Rev Can 7: 526–542, с разрешения Macmillan; и Стэнли П. 2011. Cold Spring Harb Perspect Biol 3: a005199.) (Подробнее …)
РИСУНОК 1.7.
Гликан-белковые связи, обнаруженные в природе. (Обновлено и перерисовано с разрешения Oxford University Press, из Spiro RG. 2002. Glycobiology 12: 43R – 56R.) Схематическое изображение шести различных типов сахарно-пептидных связей, которые (more…)
Якорь гликозилфосфатидилинозитола представляет собой гликановый мостик между фосфатидилинозитолом и фосфоэтаноламином, который находится в амидной связи с карбоксильным концом белка. Эта структура обычно представляет собой единственный якорь на липидной двухслойной мембране для таких белков (Глава 12). Гликосфинголипид (часто называемый гликолипидом) состоит из гликана, обычно присоединенного через глюкозу или галактозу к конечной первичной гидроксильной группе липидной части церамида, которая состоит из длинноцепочечного основания (сфингозина) и жирной кислоты (глава 11).Гликолипиды могут быть нейтральными или анионными. Ганглиозид — это анионный гликолипид, содержащий один или несколько остатков сиаловой кислоты. Следует отметить, что они представляют собой только наиболее распространенные классы гликанов, обнаруженные в эукариотических клетках. Есть несколько других менее изученных типов гликанов, обнаруженных на одной или другой стороне клеточной мембраны в клетках животных (главы 13, 17 и 18), и многие другие типы гликанов у растений, водорослей и прокариот.
Хотя разные классы гликанов имеют уникальные области ядра, по которым они различаются, определенные внешние структурные последовательности часто являются общими для разных классов гликанов.Например, N- и O-гликаны и гликосфинголипиды животных часто несут субтерминальные дисахаридные единицы Galβ1-4GlcNAcβ1- ( N, -ацетиллактозамин или LacNAc) или, реже, GalNAcβ1-4GlcNAcβ1- (LacdiNAc). Единицы LacNAc иногда могут повторяться, давая расширенные поли- N- ацетилактозамины (иногда неправильно называемые «полилактозаминами») (Глава 14). Реже может повторяться мотив LacdiNAc (называемый polyLacdiNAc). Внешние единицы LacNAc могут быть модифицированы фукозилированием или разветвлением и, как правило, блокируются у позвоночных сиаловой кислотой или, реже, сульфатными эфирами, единицами Fuc, α-Gal, β-GalNAc или β-GlcA (главы 14 и 15). .Напротив, эукариотические гликозаминогликаны представляют собой линейные сополимеры повторяющихся единиц кислотного дисахарида, каждый из которых обычно содержит гексозамин (GlcN или GalN) и гексозу (Gal) или гексуроновую кислоту (GlcA или IdoA) (Глава 17). Тип дисахаридной единицы определяет гликозаминогликан как хондроитин или дерматансульфат (GalNAcβ1-4GlcA / IdoA), гепарин или гепарансульфат (GlcNAcα1-4GlcA / IdoA) или кератансульфат (Galβ1-4GlcNAc). Кератансульфат на самом деле представляет собой 6-O-сульфатированную форму поли- N -ацетиллактозамина, присоединенную к ядру N- или O-гликана, а не к типичной области связывания протеогликана, содержащей Xyl-Ser.Другой тип гликозаминогликанов, гиалуронан (полимер GlcNAcβ1-4GlcA), по-видимому, существует в основном в виде свободного гликана, не связанного с каким-либо агликоном (глава 16). Некоторые гликозаминогликаны содержат сложные эфиры сульфата, замещающие либо амино, либо гидроксильные группы (то есть N- или O-сульфатные группы). Другой анионный полисахарид, который может быть расширен из единиц LacNAc, — это полисиаловая кислота, гомополимер сиаловой кислоты, которая избирательно экспрессируется только на нескольких белках у позвоночных. Полисиаловые кислоты и гиалуронан также встречаются в виде капсульных полисахаридов некоторых патогенных бактерий (Глава 15).Для простоты в этом разделе основное внимание уделяется гликанам позвоночных. Многие другие классы гликанов существуют в других ветвях древа жизни (главы 21–26).
ГЛИКАНОВЫЕ СТРУКТУРЫ НЕ КОДИРУЮТСЯ НАПРЯМУЮ В ГЕНОМЕ
В отличие от белковых последовательностей, которые являются продуктами первичного гена, гликановые структуры не кодируются непосредственно в геноме и являются вторичными генными продуктами. Несколько процентов известных генов в геноме человека предназначены для производства ферментов и транспортеров, ответственных за биосинтез и сборку гликанов (глава 8), обычно в виде посттрансляционных модификаций белков или путем гликозилирования основных липидов.Сами гликаны представляют собой многочисленные комбинаторные возможности, генерируемые множеством конкурирующих и последовательно действующих гликозидаз и гликозилтрансфераз (глава 6) и субкомпартментальными «конвейерными» механизмами биосинтеза гликанов в аппарате Гольджи эукариот (глава 4). Таким образом, даже при полном знании уровней экспрессии всех соответствующих генных продуктов невозможно точно предсказать точные структуры гликанов, вырабатываемых данным типом клеток. Более того, небольшие изменения в сигналах окружающей среды могут вызвать резкие изменения гликанов, производимых данной клеткой.Именно этот изменчивый и динамичный характер гликозилирования делает его мощным способом создания и регулирования биологического разнообразия и сложности. Конечно, это также затрудняет изучение гликанов, чем нуклеиновые кислоты и белки.
СТРУКТУРНОЕ РАЗНООБРАЗИЕ В ОБЛАСТИ ГЛИКОЗИЛИРОВАНИЯ БЕЛКА
Одним из наиболее интересных и в то же время разочаровывающих аспектов гликозилирования белков является феномен микрогетерогенности. Таким образом, в любом конкретном сайте присоединения гликана на данном белке, синтезируемом конкретным типом клеток, может быть обнаружен ряд вариаций в структурах присоединенного гликана (а в некоторых случаях гликан может отсутствовать).Фактически, данный полипептид, кодируемый одним геном, может существовать во множестве «гликоформ», каждая из которых представляет собой отдельный молекулярный вид. Для некоторых гликопротеинов микрогетерогенность в определенном месте может быть весьма ограниченной, тогда как для других сайтов она может быть обширной даже в пределах одного и того же вида гликопротеинов. С механической точки зрения микрогетерогенность может быть вызвана быстротой, с которой происходят множественные, последовательные, частично конкурентные реакции гликозилирования и дегликозилирования в эндоплазматическом ретикулуме (ER) и аппарате Гольджи, через который проходит вновь синтезированный гликопротеин, наряду с отсутствием матрицы для направляя синтез и доступность гликанов на сайте для модифицирующих ферментов (Глава 4).Альтернативная возможность состоит в том, что каждая отдельная клетка или тип клеток на самом деле чрезвычайно специфична в гликозилировании, которое она производит, но что межклеточные вариации приводят к наблюдаемой микрогетерогенности образцов из природных многоклеточных источников. Каким бы ни была причина микрогетерогенности, она объясняет аномальное поведение гликопротеинов в аналитических методах / методах разделения и делает полный структурный анализ гликопротеина сложной задачей. С функциональной точки зрения биологическое значение микрогетерогенности остается неясным.Возможно, это тип генератора разнообразия, предназначенный для диверсификации эндогенных функций распознавания и / или для уклонения от микробов и паразитов, каждый из которых может связываться с высокой специфичностью только с определенными гликановыми структурами (главы 37 и 42).
КЛЕТОЧНАЯ БИОЛОГИЯ ГЛИКОЗИЛИРОВАНИЯ
Наиболее хорошо изученные пути биосинтеза основных классов эукариотических гликанов находятся в компартментах ER и Гольджи (Глава 4). Вновь синтезированные белки, происходящие из ЭПР, либо котрансляционно, либо посттрансляционно модифицируются гликанами на различных этапах своего пути к конечному пункту назначения.N-гликаны частично собираются на донорах липидов на цитоплазматической стороне ЭР, а затем переворачиваются через мембрану, где завершается сборка олигосахаридов и происходит перенос на формирующийся белок. Затем этот олигосахарид урезается и удлиняется путем добавления одного моносахарида за раз, когда белок проходит через ЭР и Гольджи. В этих реакциях гликозилирования используются активированные формы моносахаридов (нуклеотидные сахара; глава 5) в качестве доноров для реакций, катализируемых гликозилтрансферазами (подробности об их биохимии, молекулярной генетике и клеточной биологии см. В главах 4, 6 и 8).Доноры нуклеотидных сахаров синтезируются в цитозольном или ядерном компартменте из моносахаридных предшественников эндогенного или экзогенного происхождения и затем активно транспортируются через бислой мембраны в просвет компартментов ER и Гольджи (Глава 5). Примечательно, что часть гликоконъюгата, которая обращена внутрь этих компартментов, в конечном итоге будет обращена к внешней стороне клетки или внутренней части секреторной гранулы или лизосомы и будет топологически не подвергнута воздействию цитозоля.Биосинтетические ферменты (гликозилтрансферазы, сульфотрансферазы и др.), Ответственные за катализ этих реакций, хорошо изучены (глава 6), и их расположение помогло определить различные функциональные компартменты пути ER-Golgi. Классическая модель предполагает, что эти ферменты физически выстраиваются вдоль этого пути в точной последовательности, в которой они фактически работают. Эта модель кажется чрезмерно упрощенной, поскольку существует значительное совпадение в распределении этих ферментов, а фактическое распределение данного фермента зависит от типа клетки.
Все топологические соображения, упомянутые выше, обращены вспять в отношении ядерного и цитоплазматического гликозилирования, потому что активные центры соответствующих гликозилтрансфераз обращены к цитозолю, который находится в прямом сообщении с внутренней частью ядра. До середины 1980-х годов общепринятой догмой было то, что гликоконъюгаты встречаются исключительно на внешней поверхности клеток, на внутренней (просветной) поверхности внутриклеточных органелл и на секретируемых молекулах. Предполагалось, что цитозоль и ядро не обладают способностью к гликозилированию.Однако теперь ясно, что определенные отдельные типы гликоконъюгатов синтезируются и находятся в цитозоле и ядре (Глава 18). Действительно, один из них, названный O-GlcNAc (глава 19), вполне может быть численно наиболее распространенным типом гликоконъюгата во многих типах клеток. Тот факт, что эту главную форму гликозилирования так долго упускали из виду многие исследователи, подчеркивает относительно неизведанное состояние области гликобиологии.
Как и все компоненты живых клеток, гликаны постоянно превращаются в процесс деградации, и ферменты, которые катализируют этот процесс, расщепляют гликаны либо на внешнем (невосстанавливающем) конце (экзогликозидазы), либо внутри (эндогликозидазы) (главы 4 и 44).Некоторые концевые моносахаридные звенья, такие как сиаловые кислоты, иногда удаляются, а новые звенья повторно присоединяются во время рециркуляции эндосом без деградации лежащей в основе цепи. Окончательная полная деградация большинства эукариотических гликанов обычно осуществляется множеством гликозидаз в лизосоме. После разложения их индивидуальные единичные моносахариды обычно экспортируются из лизосом в цитозоль для повторного использования (). В отличие от относительно медленного оборота гликанов, происходящих от пути ER-Golgi, моносахаридные модификации O-GlcNAc ядра и цитоплазмы кажутся более динамичными (Глава 19).В некоторых случаях внеклеточные или внутриклеточные свободные гликаны также могут служить сигнальными молекулами (Глава 40).
РИСУНОК 1.8.
Биосинтез, использование и оборот обычного моносахарида. Эта схема показывает биосинтез, судьбу и обмен галактозы, общего моносахаридного компонента гликанов животного происхождения. Хотя небольшие количества галактозы могут поступать извне (подробнее …)
ИНСТРУМЕНТЫ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ИССЛЕДОВАНИЯ ГЛИКОЗИЛИРОВАНИЯ
В отличие от олигонуклеотидов и белков, гликаны обычно не встречаются в линейном, неразветвленном виде.Даже будучи линейными (например, ГАГ), они часто содержат множество заместителей, таких как сульфатные группы, которые не распределены равномерно. Таким образом, полное секвенирование гликанов обычно невозможно одним методом и требует повторяющихся комбинаций физических, химических и ферментативных подходов, которые вместе дают детали структуры (для обсуждения разделения и анализа с низким и высоким разрешением, включая масс-спектрометрию и ядерный магнитный резонанс [ЯМР], см. главу 50). Менее подробная информация о структуре может быть достаточной для изучения биологии некоторых гликанов и может быть получена с помощью простых методов, таких как использование ферментов (эндогликозидаз и экзогликозидаз), лектинов и других гликан-связывающих белков (главы 48 и 50). химическая модификация или расщепление, метаболическое радиоактивное мечение, антитела или клонированные гликозилтрансферазы (главы 53 и 54).Гликозилирование также может быть нарушено различными способами, например, ингибиторами гликозилирования и праймерами (главы 55 и 56) и генетическими манипуляциями гликозилирования в интактных клетках и организмах (глава 49). Направленный синтез гликанов in vitro химическими и ферментативными методами также добился больших успехов в последние годы, предоставив множество новых инструментов для изучения гликобиологии (главы 53, 54 и 57). Создание сложных библиотек гликанов различными путями еще больше улучшило этот химический и биологический интерфейс (главы 53 и 54), включая создание микрочипов гликанов.
ГЛИКОМИКА
Аналогично геномике и протеомике, гликомика представляет собой систематическое методологическое разъяснение «гликома» (совокупности гликановых структур) данного типа клетки или организма (главы 51 и 52). На самом деле гликом намного сложнее, чем геном или протеом. Помимо значительно большего структурного разнообразия гликанов, приходится сталкиваться со сложностями микрогетерогенности гликозилирования (см. Выше) и динамическими изменениями, которые происходят в ходе развития, дифференцировки, метаболических изменений, старения, злокачественности, воспаления или инфекции.Дополнительное разнообразие возникает из-за внутривидовых и межвидовых вариаций гликозилирования. Таким образом, данный тип клеток у данного вида может проявлять большое количество возможных состояний гликома. Гликомический анализ сегодня обычно состоит из извлечения целых типов клеток, органов или организмов; освобождение всех гликановых цепей от их связей; и каталогизация их с помощью таких подходов, как масс-спектрометрия. В варианте, называемом гликопротеомика, гликаны анализируются, оставаясь прикрепленными к фрагментам гликопротеинов, генерируемым протеазой.Полученные результаты представляют собой впечатляющее улучшение по сравнению с тем, что было возможно несколько десятилетий назад, но они все еще аналогичны вырубке всех деревьев в лесу и их каталогизации без внимания к планировке леса и ландшафту (это обсуждается в главе 15). сложная проблема с точки зрения только одного класса моносахаридов, сиаловых кислот; см.).
Гликомический анализ, таким образом, необходимо дополнить классическими методами, такими как окрашивание срезов ткани или проточная цитометрия, с использованием лектинов или гликан-специфических антител, которые помогают понять гликом, принимая во внимание гетерогенность гликозилирования на уровне различных клеток. типы и субклеточные домены в исследуемой ткани.Это даже более важно из-за общего наблюдения, что удаление клеток из их нормальной среды и помещение их в культуру ткани может привести к серьезным изменениям в аппарате гликозилирования клетки. Однако такие классические подходы страдают плохой количественной оценкой и относительной нечувствительностью к структурным деталям. Комбинация этих двух подходов в настоящее время потенциально возможна посредством микродиссекции с помощью лазерного захвата определенных типов клеток непосредственно из срезов тканей, а полученные образцы исследуются с помощью масс-спектрометрии.Совершенно очевидно, что необходимы новые методы визуализации in situ и характеристики гликанов в нетронутом «лесу».
Поскольку большинство генов, участвующих в путях биосинтеза гликанов, были клонированы от множества организмов, сегодня возможно получить косвенное геномное и транскриптомное представление о гликоме в конкретном типе клеток (глава 8). Однако, учитывая относительно слабую корреляцию между уровнями мРНК и белка, а также сложную линию сборки и конкурентный характер клеточных путей гликозилирования Гольджи, даже полное знание паттернов экспрессии мРНК всех соответствующих генов в данной клетке не может позволить точно предсказать распределение и структура гликанов в этом типе клеток.Таким образом, пока нет надежного косвенного пути к выяснению гликома, кроме фактического анализа с использованием ряда методов.
ДЕФЕКТЫ ГЛИКОЗИЛИРОВАНИЯ В ОРГАНИЗМАХ И КУЛЬТИВИРУЕМЫХ КЛЕТКАХ
Описано множество мутантных вариантов культивируемых клеточных линий с измененными гликановыми структурами и специфическими дефектами биосинтеза гликанов, наиболее распространенными из которых являются лектин-резистентные (Глава 49). Действительно, за некоторыми исключениями, мутанты со специфическими дефектами на большинстве стадий основных путей биосинтеза гликанов были обнаружены в культивируемых клетках животных.Использование таких клеточных линий имело большое значение для выяснения деталей путей биосинтеза гликанов. Их существование подразумевает, что многие типы гликанов не имеют решающего значения для оптимального роста отдельных клеток, растущих в защищенной и относительно неизменной среде культуральной чашки. Скорее, большинство гликановых структур д. Играть более важную роль в обеспечении взаимодействий клетка-клетка и клетка-матрикс в интактных многоклеточных организмах и / или взаимодействий между организмами. В соответствии с этим предположением, генетические дефекты, полностью устраняющие основные классы гликанов у интактных животных, вызывают гибель эмбрионов (Глава 45).Как и следовало ожидать, встречающиеся в природе жизнеспособные мутанты животных этого типа, как правило, обладают фенотипами болезни средней степени тяжести и демонстрируют сложные фенотипы, включающие несколько систем. Менее серьезные генетические изменения компонентов внешней цепи гликанов имеют тенденцию давать жизнеспособные организмы с более специфическими фенотипами (Глава 45). В целом, можно многому научиться, изучая последствия естественных или индуцированных генетических дефектов в интактных многоклеточных организмах, включая человека (Глава 45).
БИОЛОГИЧЕСКИЕ РОЛИ ГЛИКАНОВ РАЗНООБРАЗНЫ
Основная тема этого тома — исследование и разъяснение биологической роли гликанов. Интересно отметить, что за короткое время, прошедшее с момента выхода первого издания, мы перестали спрашивать: «А что же гликаны делают?» к необходимости объяснять большое количество сложных и иногда нежизнеспособных фенотипов с модифицированным гликозилированием у людей, мышей, мух и других организмов. Как и любая биологическая система, при оптимальном подходе тщательно рассматривается взаимосвязь структуры и биосинтеза с функцией (глава 7).Как можно догадаться по их повсеместной и сложной природе, биологические роли гликанов заметно разнообразны. В самом деле, вопрос о том, каковы эти роли, сродни задаче того же вопроса о белках. Таким образом, все предложенные теории относительно функции гликанов оказываются частично правильными, и для каждой также могут быть найдены исключения. Неудивительно, что для такой разнообразной группы молекул биологические роли гликанов также охватывают спектр от незначительных до тех, которые имеют решающее значение для развития, роста, функционирования или выживания организма (глава 7).Разнообразные функции, приписываемые гликанам, можно просто разделить на две общие категории: (i) структурные и модуляторные функции (включающие сами гликаны или их модуляцию молекул, к которым они присоединены) и (ii) специфическое распознавание гликанов гликанами. связывающие белки. Конечно, любой гликан может опосредовать один или оба типа функций. Связывающие белки, в свою очередь, делятся на две широкие группы: лектины и сульфатированные GAG-связывающие белки (главы 27, 28 и 38). Такие молекулы могут быть внутренними для организма, синтезировавшего родственные гликаны (например,g., см. главы 31–36, 38 и 39) или внешнего (см. главы 37 и 42 для получения информации о микробных белках, которые связываются со специфическими гликанами на клетках-хозяевах). Атомные детали этих гликан-белковых взаимодействий были выяснены во многих случаях (главы 29 и 30). Хотя есть исключения из этого понятия, в отношении лектинов возникла следующая общая тема: моновалентное связывание имеет тенденцию к относительно низкому сродству, и такие системы обычно достигают своей специфичности и функции за счет достижения высокой авидности посредством взаимодействия поливалентных массивов гликанов с родственными им. сайты связывания лектина.
ИЗМЕНЕНИЯ ГЛИКОЗИЛИРОВАНИЯ В РАЗВИТИИ, ДИФФЕРЕНЦИАЦИИ И ЗЛОКАЧЕСТВЕННОСТИ
Каждый раз, когда разрабатывается новый инструмент (например, антитело или лектин), специфичный для обнаружения определенного гликана, и используется его для исследования его экспрессии в интактных организмах, обычно находят исключительно специфические временные и пространственные паттерны экспрессии этого гликана в отношении клеточной активации, эмбрионального развития, органогенеза и дифференцировки (см. примеры в главе 41). Определенные относительно специфические изменения в экспрессии гликанов также часто обнаруживаются в ходе трансформации и прогрессирования в злокачественные новообразования (Глава 47), а также в других патологических ситуациях, таких как воспаление (Глава 46).Эти пространственно и временно контролируемые паттерны экспрессии гликанов подразумевают участие гликанов во многих нормальных и патологических процессах, точные механизмы которых понятны только в некоторых случаях.
ЭВОЛЮЦИОННЫЕ СООБРАЖЕНИЯ В ГЛИКОБИОЛОГИИ
Удивительно мало еще известно об эволюции гликозилирования. Есть четко общие и уникальные особенности гликозилирования в разных царствах и таксонах. Среди животных может иметь место тенденция к увеличению сложности N- и O-гликанов в недавно появившихся («высших») таксонах.Внутривидовые и межвидовые вариации гликозилирования также относительно обычны. Было высказано предположение, что более конкретные биологические роли гликанов часто опосредуются необычными структурами, необычными представлениями общих структур или дальнейшими модификациями самих обычно встречающихся сахаридов. Такие необычные структуры, вероятно, являются результатом уникальных паттернов экспрессии соответствующих гликозилтрансфераз или других ферментов, модифицирующих гликаны. С другой стороны, такие необычные гликаны могут быть мишенями для специфического распознавания инфекционными микроорганизмами и различными токсинами.Таким образом, по крайней мере часть разнообразия экспрессии гликанов в природе должна быть связана с давлением эволюционного отбора, создаваемым межвидовыми взаимодействиями (например, хозяина с патогеном или симбионтом). Другими словами, два разных класса распознавания гликанов, упомянутые выше (опосредованные внутренними и внешними гликановыми связывающими белками), конкурируют друг с другом в отношении конкретной гликановой мишени. Специализированные гликаны, экспрессируемые паразитами и микробами, которые представляют большой интерес с биомедицинской точки зрения (главы 21, 22, 23 и 43), предположительно сами подвергаются давлению эволюционного отбора.Эти вопросы дополнительно рассматриваются в главе 20, в которой также обсуждается ограниченная информация о том, как различные пути биосинтеза гликанов, по-видимому, эволюционировали и расходились в разных формах жизни.
ГЛИКАНЫ В МЕДИЦИНЕ И БИОТЕХНОЛОГИИ
Многочисленные природные биоактивные молекулы представляют собой гликоконъюгаты, и присоединенные гликаны могут оказывать сильное влияние на биосинтез, стабильность, действие и круговорот этих молекул в интактных организмах. Например, сульфатированный гликозаминогликановый гепарин и его производные являются одними из наиболее часто используемых лекарств в мире.Все антибиотики-аминогликозиды содержат углеводные компоненты, необходимые для активности. По этой и многим другим причинам гликобиология и химия углеводов становятся все более важными в современной биотехнологии. Патентование гликопротеинового препарата, получение одобрения FDA на его использование и мониторинг его производства — все это требует знания структуры его гликанов. Более того, гликопротеины, в состав которых входят моноклональные антитела, ферменты и гормоны, в настоящее время являются основными продуктами биотехнологической промышленности, объем продаж которых составляет десятки миллиардов долларов в год, и этот показатель продолжает расти все более быстрыми темпами.Кроме того, некоторые болезненные состояния человека включают изменения в биосинтезе гликанов, которые могут иметь диагностическое и / или терапевтическое значение. Растущее значение гликобиологии в медицине и биотехнологии обсуждается в главах 56 и 57.
ГЛИКАНЫ В НАНОТЕХНОЛОГИИ, БИОЭНЕРГИИ И МАТЕРИАЛОВЕДЕНИИ
Хотя традиционно не считаются частью «гликобиологии», многие природные и синтетические гликаны являются ключевыми компонентами нанотехнологий. , Биоэнергетика и материаловедение. Гликонаноматериалы (Глава 58) обладают настраиваемыми химическими и физическими свойствами и могут быть построены на различных каркасах для исследования взаимодействий между клетками, тканями и организмами.Присоединенные гликаны могут изменять свойства наноматериала, оптимизируя растворимость и биосовместимость, а также снижая цитотоксичность. Гликонаноматериалы использовались в качестве агентов визуализации, спектроскопических инструментов, мониторов клеточных систем и носителей для вакцинации и доставки лекарств. Растительные гликаны используются для многих целей: источников энергии, строительных материалов, одежды, бумажных изделий, кормов для животных, пищевых добавок и напитков (Глава 59). Обеспокоенность по поводу пагубного воздействия на окружающую среду и уменьшения запасов нефти и ее побочных продуктов значительно повысила интерес к использованию растительных гликанов для производства энергии, получения полимеров с улучшенными или новыми функциональными возможностями, а также в качестве источников ценных хемосинтетических прекурсоров (Глава 59).
БЛАГОДАРНОСТИ
Авторы выражают признательность покойному Натану Шарону за вклад в предыдущую версию этой главы, а также за полезные комментарии и предложения всех редакторов.
ДОПОЛНИТЕЛЬНОЕ ЧТЕНИЕ
- Радемахер Т.В., Парех РБ, Двек РА. 1988. Гликобиология. Анну Рев Биохим 57: 785–838. [PubMed: 3052290]
- Дрикамер К., Тейлор МЭ. 1998. Развитие взглядов на гликозилирование белков. Тенденции Biochem Sci 23: 321–324. [PubMed: 9787635]
- Etzler ME.1998. Олигосахаридная передача сигналов растительных клеток. J Cell Biochem Suppl 30–31: 123–128. [PubMed: 9893263]
- Gagneux P, Varki A. 1999. Эволюционные соображения в связи разнообразия олигосахаридов с биологической функцией. Гликобиология 9: 747–755. [PubMed: 10406840]
- Роземан С. 2001. Размышления о гликобиологии. J Biol Chem 276: 41527–41542. [PubMed: 11553646]
- Spiro RG. 2002. Гликозилирование белков: природа, распределение, ферментативное образование и последствия гликопептидных связей для болезней.Гликобиология 12: 43R – 56R. [PubMed: 12042244]
- Haltiwanger RS, Lowe JB. 2004. Роль гликозилирования в развитии. Анну Рев Биохим 73: 491–537. [PubMed: 15189151]
- Шэрон Н., Лис Х. 2004. История лектинов: от гемагглютининов до молекул биологического распознавания. Гликобиология 14: 53Р – 62Р. [PubMed: 15229195]
- Охцубо К., Март Дж. Д.. 2006. Гликозилирование в клеточных механизмах здоровья и болезней. Клетка 126: 855–867. [PubMed: 16959566]
- Патнаик С.К., Стэнли П.2006. Устойчивые к лектину мутанты гликозилирования СНО. Методы Энзимол 416: 159–182. [PubMed: 17113866]
Дрикамер К., Тейлор МЭ. 2006. Введение в гликобиологию, Vol. 2. Издательство Оксфордского университета, Оксфорд.
Камерлинг Дж., Бунс Дж. Дж., Ли Й, Сузуки А., Танигучи Н., Вораген AGJ. 2007. Всесторонняя гликология, стр. 1–4. Elsevier Science, Лондон.
- Hart GW, Slawson C, Ramirez-Correa G, Lagerlof O. 2011. Перекрестный разговор между O-GlcNAcylation и фосфорилированием: роли в передаче сигналов, транскрипции и хронических заболеваниях.Анну Рев Биохим 80: 825–858. [Бесплатная статья PMC: PMC3294376] [PubMed: 21391816]
- Варки А. 2011. Эволюционные силы, формирующие механизм гликозилирования Гольджи: почему гликаны клеточной поверхности универсальны для живых клеток. Холодная весна Харб Perspect Biol 3: a005462. [Бесплатная статья PMC: PMC3098673] [PubMed: 21525513]
- Aebi M. 2013. N-связанное гликозилирование белка в ER. Биохим Биофиз Акта 1833: 2430–2437. [PubMed: 23583305]
- Варки А. 2013.Омикс: объясните «темную материю» биологии. Природа 497: 565. [PubMed: 23719451]
- Endo T. 2015. Гликобиология α-дистрогликана и мышечной дистрофии. J Biochem 157: 1–12. [PubMed: 25381372]
- Misra S, Hascall VC, Markwald RR, Ghatak S. 2015. Взаимодействия между гиалуронаном и его рецепторами (CD44, RHAMM) регулируют активность воспаления и рака. Фронт Иммунол 6: 201. [Бесплатная статья PMC: PMC4422082] [PubMed: 25999946]
- Варки А., Каммингс Р.Д., Эби М., Пакер Н.Х., Сибергер П.Х., Эско Д.Д., Стэнли П., Харт Дж., Дарвилл А., Киношита Т. и др. .2015. Номенклатура символов для графических представлений гликанов. Гликобиология 25: 1323–1324. [Бесплатная статья PMC: PMC4643639] [PubMed: 26543186]
- Aoki-Kinoshita K, Agravat S, Aoki NP, Arpinar S, Cummings RD, Fujita A, Fujita N, Hart GM, Haslam SM, Kawasaki T, et al. 2016. GlyTouCan 1.0 — международный репозиторий структур гликанов. Нуклеиновые кислоты Res 44: D1237 – D1242. [Бесплатная статья PMC: PMC4702779] [PubMed: 26476458]
Ученые открывают новый ключ к химическому происхождению жизни — ScienceDaily
Химики-органики из Йоркского университета добились значительного прогресса в установлении происхождения углеводов (сахаров ), которые образуют строительные блоки жизни.
Команда под руководством доктора Пола Кларка из химического факультета Йорка воссоздала процесс, который мог произойти в пребиотическом мире.
Работая с коллегами из Ноттингемского университета, они сделали первый шаг к тому, чтобы показать, как развиваются простые сахара — треоза и эритроза. Исследование опубликовано в Organic & Biomolecular Chemistry .
Все биологические молекулы могут существовать как левосторонние или правосторонние формы.Все сахара в биологии состоят из молекул правой формы, и все же все аминокислоты, из которых состоят пептиды и белки, состоят из левой формы.
Исследователи обнаружили, что использование простых левых аминокислот для катализирования образования сахаров привело к образованию преимущественно правых форм сахаров. Это могло бы объяснить, как произошли углеводы и почему правая форма преобладает в природе.
Доктор Кларк сказал: «Есть много фундаментальных вопросов о происхождении жизни, и многие люди думают, что это вопросы биологии.Но для того, чтобы жизнь эволюционировала, у вас должен быть момент, когда неживые существа станут живыми — все до этого момента — химия.
«Мы пытаемся понять химическое происхождение жизни. Один из интересных вопросов заключается в том, откуда берутся углеводы, потому что они являются строительными блоками ДНК и РНК. То, что мы достигли, является первым шагом на этом пути, чтобы показать, как простые сахара — треоза и эритроза — возникли.Мы создали эти сахара из очень простого набора материалов, которые, по мнению большинства ученых, были в то время, когда зародилась жизнь.«
История Источник:
Материалы предоставлены Йоркским университетом . Примечание. Содержимое можно редактировать по стилю и длине.
первичных открытий для первого использования в лечении T1D
Кредит: Катерина Кон / Научная фотобиблиотека
В 1921 году Фредерик Бантинг и Чарльз Бест разработали серию экспериментов, чтобы определить, как поджелудочная железа участвует в углеводном обмене.Их работа, опубликованная в 1922 году, основана на результатах исследований за предыдущие 40–50 лет, показывающих, что поджелудочная железа, а точнее островки Лангерганса, была ключевой для углеводного обмена и могла быть вовлечена в патогенез заболевания, которое мы теперь знаем. как диабет 1 типа (T1D). Эта работа привела к идентификации инсулина.
Вместе с Джоном Маклаудом, Бантинг и Бест предположили, что метаболизм углеводов контролируется либо изменением крови при прохождении через поджелудочную железу, либо островками Лангерганса, производящими внутреннюю секрецию.Бантинг и Бест начали с удаления поджелудочной железы у нескольких собак, которые затем стали проявлять признаки диабета, включая повышение уровня глюкозы в крови и моче. Затем собакам вводили различные экстракты поджелудочной железы, после чего уровни глюкозы в крови и моче упали, а их общее состояние здоровья улучшилось. Бантинг и Бест отметили, что степень эффекта варьировалась в зависимости от того, насколько концентрированным был экстракт. Они также обнаружили, что экстракты, содержащие сок поджелудочной железы (содержащие пищеварительные ферменты), сводят на нет положительное влияние экстракта поджелудочной железы на уровень глюкозы.Эти результаты демонстрируют, что секреция поджелудочной железы участвует в метаболизме углеводов.
После этих выводов исследователи начали работу по очистке экстракта. Раннее использование этого экстракта поджелудочной железы пациентами было безуспешным из-за высокого содержания в нем белка. Затем к команде присоединился Джеймс Бертрам Коллип, чтобы помочь в дальнейшей очистке экстракта поджелудочной железы для введения инсулина. Исследователи разработали метод производства большего количества инсулина, чтобы можно было вводить его пациентам.
В больнице общего профиля Торонто, Канада, началась работа по введению инсулина небольшому количеству пациентов с СД1 под тщательным наблюдением. Леонард Томпсон (14 лет), как известно, был одним из этих первых пациентов и потенциально был первым пациентом, которому вводили инсулин. Как и в предыдущих исследованиях с животными, у этих пациентов после введения инсулина уровни глюкозы в крови и моче упали. Пациенты также сообщили о полном исчезновении субъективных симптомов, связанных с СД1.
Сообщая о случае Леонарда Томпсона, исследователи отметили его низкий вес, вялость и высокий уровень глюкозы в крови и моче. После ежедневного введения инсулина Леонард быстро почувствовал себя лучше и стал более внимательным, а уровень глюкозы в крови и моче снизился. После отмены лечения на 2 дня симптомы вернулись. В своей статье 1922 года в журнале Canadian Medical Association Journal исследователи отмечают, что «эти результаты, взятые вместе, не оставляют сомнений в том, что в этих экстрактах мы имеем терапевтическую меру неоспоримой ценности при лечении определенных фаз болезнь у человека.
Исследователи отметили, что их первые результаты были достаточно положительными, чтобы требовать дальнейшей работы по уточнению схемы лечения и улучшению результатов лечения пациентов. В следующие десятилетия наблюдался быстрый прогресс в использовании инсулина для лечения СД1, например, открытие в 1930-х годах того, что действие инсулина можно продлить с помощью добавления протамина.
Бантинг и Маклауд были удостоены Нобелевской премии по физиологии и медицине за их работу по определению инсулина. Признавая ключевое участие Беста и Коллипа, Бантинг и Маклауд решили разделить призовой фонд со своими двумя коллегами.Как отметил Бантинг в своей лекции о присуждении Нобелевской премии, инсулин не является лекарством от СД1; вместо этого это лечение, которое позволяет людям с СД1 усваивать углеводы. Исследования T1D значительно продвинулись вперед за 100 лет, прошедших после основополагающей статьи Бантинга и Беста, но лекарство так и осталось неуловимым. Остается надеяться, что лекарство будет найдено в ближайшие несколько лет.
Дополнительная литература
Banting, F. G. et al. Эффект от сахарного диабета при удалении поджелудочной железы. Сделка.Жопа. Амер. Врачи 37 , 337 (1922).
Banting, F. G. et al. Экстракты поджелудочной железы в лечении сахарного диабета: предварительное сообщение. Банка. Med. Доц. J. 12 , 141–146 (1922).
де Лейва-Идальго, А. и де Лейва-Перес, А. Опыт первых пациентов, получавших инсулин (1922–1923). Am. J. Ther. 27 , e13 – e23 (2020).
История: меняющееся представление о еде
Пионеры исследований в области питания определили энергетическую ценность пищи, а также помогли опровергнуть неправильные представления о различных заболеваниях, от которых страдает человечество.
Нутригеномика — и остальная часть современной науки о питании — опирается на основы, заложенные в конце восемнадцатого века.
Нельзя сказать, что до этого никто не интересовался тем, как работает еда. Древние цивилизации Египта, Греции, Рима, Персии, Китая и Индии знали о связи между едой и здоровьем. «У всех были свои правила питания, многие из которых действуют и сегодня», — говорит Клаус Лейтцманн, диетолог из Университета Гиссена в Германии.«Древние египтяне использовали чеснок в лечебных целях».
Некоторые из наших истин о еде восходят к тысячелетиям. Древнегреческий врач Гиппократ рекомендовал тщательно пережевывать пищу перед проглатыванием и употреблять в умеренных количествах для поддержания хорошего здоровья. В средние века немецкая монахиня и христианский мистик Хильдегард из Бингена «много знала о еде», — говорит Лейтцманн. «Она дала несколько очень разумных рекомендаций», например, есть приготовленную, а не сырую пищу.
Химик восемнадцатого века Антуан Лавуазье исследует, аналогичен ли выдыхаемый воздух дымам двигателя внутреннего сгорания.Кредит: BETTMANN / CORBIS
Но до восемнадцатого века было мало научных исследований, касающихся состава пищи или того, как ее обрабатывает организм. Исследователи того времени «зависели от экспериментального наблюдения», — говорит Лейтцманн. Их метод был «корми и наблюдай». Французский химик Антуан Лавуазье, которого считают отцом современной химии, первым провел исследования, которые привели к современной науке о нутригеномике.
Лавуазье был одним из первых ученых, разработавших лабораторное оборудование для проверки того, что происходит с едой после ее проглатывания.До его работы ученые знали, что вес принятой пищи превышает вес выделенных фекалий и мочи. Они объяснили эту потерю потоотделением. Но Лавуазье считал, что пища является топливом, и что организм, как и двигатели, работающие на топливе, которые разрабатывались в то время, должен выделять углекислый газ как продукт сгорания. Он подозревал, что эта потерянная материя была вызвана выдыхаемым углекислым газом.
Чтобы проверить свою теорию, в начале 1780-х годов Лавуазье изобрел новый тип устройства — ледяной калориметр.Он состоял из внешней оболочки, заполненной льдом, для поддержания постоянной температуры 0 ° C, в которой находилась камера, в которой находилась морская свинка. Тепло тела животного растопило лед. Взвесив воду, вытекающую из калориметра, Лавуазье смог оценить метаболическое тепло и сравнить его с теплотой, производимой зажженной свечой или горящим углем.
Его теория оказалась верной. Лавуазье заявил: «Дыхательный газообмен — это горение, подобное горению свечи».
В сегодняшнем мире подсчета калорий это не похоже на откровение.Но в то время это был прорыв. «Теоретически важно было понять, что телу необходима энергия для функционирования и что одна из основных функций пищи — обеспечивать ее», — говорит Элизабет Несвальд, историк науки из Университета Брока в Онтарио, Канада. «Это была основа для определения того, что кому-то нужно, чтобы выжить; что приводит к увеличению веса, что приводит к потере веса, что делает возможным физический труд и какова взаимосвязь между едой и физическим трудом ».
Исследование Лавуазье также подчеркнуло важность состава пищи и понимание того, что кал, моча, потоотделение и дыхание являются неотъемлемой частью этого уравнения.
«Ранние диетологи потратили большую часть своего времени на изучение экскрементов других людей».
«Эти первые ученые-диетологи потратили большую часть своего времени — или времени своих помощников — на изучение и анализ экскрементов других людей», — говорит Несвальд. «В экспериментах по питанию было жизненно важно оценить разницу между входом и выходом — входящей пищей и всеми выходящими продуктами».
Этот метод, известный как «испытания баланса», был впервые применен в 1830-х годах французским химиком Жан-Батистом Буссинго.Он провел испытания баланса азота — составного элемента белков — путем сравнения содержания азота в сене, овсе и картофеле, скармливаемых коровам и лошадям, с экскрементами животных и, в случае коров, с молоком. Он показал, что корм для животных содержит достаточно азота для удовлетворения потребностей организма, положив конец предположениям о том, что дополнительный азот был получен из атмосферы.
Исследование макронутриентов
К середине девятнадцатого века ученые узнали, что основными элементами в пище являются углерод, азот, водород и кислород, и разделили составляющие пищи на четыре основных типа: углеводы, жиры, белок и воду.Однако химический состав первых трех классов был неизвестен.
Следующий шаг вперед сделал немецкий химик Юстус фон Либих. Не по годам развитый фон Либих (назначенный профессором Гиссенского университета в 21 год) изобрел «калиаппарат», специальную стеклянную посуду для анализа углерода в органических соединениях.
Лаборатория фон Либиха, возможно, первая учебная лаборатория, привлекала ученых со всего мира. Он помог обучить поколение исследователей питания, работа которых продолжится до начала двадцатого века.Например, в 1860-х годах два протеже фон Либиха — физиолог Карл фон Фойт и химик Макс Йозеф фон Петтенкофер — получили финансирование от правительства Баварии на строительство современной дыхательной камеры, достаточно большой, чтобы вместить человека. Камера могла измерять суточный баланс углерода и азота и, таким образом, оценивать потребности человека в белке.
Несвальд отмечает, что большая часть исследований в области питания в этот период была сосредоточена не на здоровье людей, а скорее на поиске самых дешевых и простых способов накормить «институционализированное и обнищавшее население», чтобы предотвратить пищевые бунты.Фон Войт, по словам Несвальда, посетил тюрьмы и работные дома, «чтобы оценить, чем людей кормили и каково состояние их здоровья, с целью предоставления рекомендаций по питанию».
Концепция пищи как топлива, которая содержит важные диетические компоненты, получила дальнейшее развитие в Соединенных Штатах. Агрохимик Уилбур Олин Этуотер провел время в лаборатории фон Войта в качестве постдока, вернувшись в США в 1871 году, чтобы возглавить науку о питании. В 1890-х годах Этуотер провел пять лет, создав дыхательный калориметр, больший, чем у фон Фойта, и способный удерживать людей дольше суток.Его измерения были настолько точными, что его энергетические эквиваленты белков, жиров и углеводов используются до сих пор. Этуотер был первым, кто использовал слово «калория» в качестве единицы энергии для еды. (Калорийность пищевой энергии на самом деле эквивалентна 1000 калорий тепловой энергии.)
Ученые вскоре начали понимать, что, помимо снабжения энергией и макроэлементами, еда также играет более тонкую роль в здоровье и болезнях. Японский врач Такаки Канехиро, который учился в 1870-х годах в Медицинской школе больницы Святого Томаса в Лондоне, был редким исключением из доминирования Германии в области питания в девятнадцатом веке.«Он был первым, кто показал, что бери-бери возникает в результате недоедания», — говорит Кацухико Ёкои, диетолог из Университета Сейтоку в Японии. Раньше бери-бери считали инфекционным заболеванием.
К началу двадцатого века другие ученые всего мира начали изучать связи между недостаточностью питательных веществ и другими заболеваниями, включая рахит и цингу. Не имея возможности объяснить эти недуги с точки зрения жиров, белков или углеводов, некоторые ученые начали подозревать существование другого класса пищевых ингредиентов.
Калориметр Атуотера-Розы, используемый для измерения потребности человека в энергии. Предоставлено: БИБЛИОТЕКА ВЕСЛЕЙСКОГО УНИВЕРСИТЕТА, СПЕЦИАЛЬНЫЕ КОЛЛЕКЦИИ И АРХИВЫ
Польский биохимик Казимир Функ в 1912 году, изучая бери-бери, выделил тиамин, питательное вещество, которое защищает от этого заболевания. Он назвал это вещество «жизненно важным амином», который вскоре стал «витамином».
Борьба с цингой — это пример науки, позже уточняющей ассоциацию болезней, связанных с питанием.В середине восемнадцатого века шотландский военно-морской врач Джеймс Линд обнаружил, что цингу можно лечить или предотвратить, употребляя цитрусовые. Но он ошибочно полагал, что в болезни виноват морской воздух. Последовали и другие ошибочные предположения: например, в 1846 году шотландский токсиколог Роберт Кристисон выдвинул гипотезу о том, что цинга вызвана дефицитом белка. Цинга продолжала быть спорадической проблемой в начале двадцатого века. Только в 1932 году американский биохимик Чарльз Глен Кинг показал, что цинга вызывается дефицитом недавно открытого витамина С.
Исследования на животных привели к дальнейшим открытиям, связанным с витаминами и болезнями. Биохимик из США Элмер Вернер Макколлум выучил немецкий язык, чтобы читать работы прошлых исследователей питания, которые вдохновили его на эксперименты на крысах. В Университете Висконсина, где Макколлум первоначально работал, протоколы исследований предусматривали использование коров в качестве животных моделей. Но Макколлум убедил начальство позволить ему попробовать более мелких животных. Он купил 12 крыс-альбиносов в зоомагазине и основал первую в США колонию крыс для экспериментов по питанию.В 1913 году его исследования на этих крысах привели его к идентификации первого жирорастворимого витамина, витамина А, а позже показали, что именно витамин D — а не витамин А, как некоторые думали, — предотвращает рахит.
Доказать связь между питательными микроэлементами и болезнями было нелегко. Сотрудник Службы общественного здравоохранения США и эпидемиолог Джозеф Голдбергер предположил, что пеллагра, которая в то время была основным заболеванием, вызывающим диарею, дерматит, слабоумие и смерть, была связана с диетой, а не инфекционным заболеванием, как преобладали в то время.В 1916 году, чтобы доказать свою точку зрения, Гольдбергер и его ассистент подвергли себя серии тестов — они вливали друг другу кровь больного пеллагрой, вымывали выделения из носа и горла человека, инфицированного пеллагрой, и втирали их в собственное тело. , и проглоченные капсулы, содержащие корки сыпи у больных пеллагрой. И все же, несмотря на такое сильное воздействие, у них не развилась пеллагра. Однако Голдбергеру не удалось найти причину, связанную с диетой. Прошло еще два десятилетия, прежде чем американский биохимик Конрад Эльвехджем понял, что пеллагра вызвана дефицитом ниацина (витамина B3).
К 1944 году было обнаружено так много питательных микроэлементов, что некоторые считали, что область питания полностью определена, и больше почти ничего не осталось. Но в то время как составные части еды могли быть извлечены, их влияние на организм только начинало цениться.
От Лавуазье через фон Либиха до современных ученых, таких как Хосе Ордовас (см. «Большая наука за столом», стр. S2), исследования в области питания были сосредоточены на все меньших и меньших элементах. По мере того, как ученые глубже исследуют биохимические механизмы поглощения и функционирования организма, открывая тайны по ходу дела, они также вызывают новые вопросы, пока мы не дойдем до того, «как наши гены взаимодействуют с пищей, которую мы едим?» И это вопрос, на который мы все еще пытаемся ответить сегодня.
Информация об авторе
Принадлежность
Нед Стаффорд — научный писатель из Гамбурга.
Нед Стаффорд
Об этой статье
Цитируйте эту статью
Стаффорд, Н. История: изменение представления о еде. Nature 468, S16 – S17 (2010). https://doi.org/10.1038/468S16a
Скачать цитату
Поделиться этой статьей
Все, с кем вы поделитесь следующей ссылкой, смогут прочитать это содержание:
Получить ссылку для совместного использованияИзвините, ссылка для совместного использования в настоящее время отсутствует доступно для этой статьи.
Предоставлено инициативой по обмену контентом Springer Nature SharedIt
Первое в мире открытие нового углеводного «вкуса»
Исследователи Deakin показали, что вкусовая чувствительность к углеводам увеличивает потребление энергии и углеводов и приводит к увеличению объема талии.Ученые Deakin определили потенциальный седьмой «вкус» — углеводов — и работают над выяснением того, как он связан с потреблением крахмалистой пищи.
Исследователи из Центра передовых сенсорных наук (CASS) Университета Дикина показали, что вкусовая чувствительность к углеводам увеличивает потребление энергии и углеводов и приводит к увеличению объема талии.
Ведущий исследователь профессор Рассел Кист сказал, что углеводы долгое время считались невидимыми на вкус.
«Обычно сахар с его приятным сладким вкусом является наиболее востребованным из углеводов», — сказал профессор Кист.
«Но наши исследования показали, что есть ощутимые вкусовые качества, вызываемые другими углеводами, независимо от сладкого вкуса».
В исследовании профессора Киста были изучены два углевода, мальтодекстрин и олигофруктоза, которые содержатся в обычных продуктах питания, таких как хлеб, макаронные изделия и рис.
Первоначальное тестирование, проведенное доктором Джулией Лоу, академиком Школы физических упражнений и питания Дикина, показало, что эти углеводы можно почувствовать во рту.
Затем исследователиCASS провели исследование, чтобы выяснить, связана ли чувствительность к углеводам с потреблением людьми крахмалистых продуктов.
Исследование, опубликованное в журнале Journal of Nutrition , изучило 34 взрослых и обнаружило значительную корреляцию между тем, насколько человек был чувствителен к этим углеводам, их диетическим потреблением углеводов, количеством потребляемой энергии и размером их талии.
«Те, кто был наиболее чувствителен к углеводному вкусу, ели больше этих продуктов и имели большую талию», — сказал доктор Лоу.
«Мы специально изучили размеры талии, поскольку они являются хорошим показателем риска заболеваний, связанных с питанием.«
Профессор Кист сказал, что эта линия новых исследований вкусов важна, потому что растущая проблема хронических заболеваний, связанных с питанием, таких как ожирение, требует более глубокого понимания движущих сил пищи, которую мы потребляем.
«Повышенное потребление энергии, в особенности более калорийной пищи, считается одним из основных факторов глобального роста избыточного веса и ожирения, а углеводы представляют собой главный источник энергии в нашем рационе», — сказал он.
Команда профессора Киста ранее называла жир «шестым вкусом».
Исследования вкуса жира изучали способность языка определять жир как особый вкус, аналогичный способности людей ощущать сладкий, кислый, горький, соленый и умами — пять традиционных или классических вкусов.
«Интересно, что мы обнаружили в исследованиях вкуса жира, что люди, которые были более чувствительны к жиру, потребляли меньше жирной пищи, но с углеводами все наоборот», — сказал профессор Кист.
«Это может означать, что люди, которые более чувствительны к« вкусу »углеводов, также имеют некоторую форму подсознательного ускорителя, который увеличивает потребление углеводов или крахмалистой пищи. Но нам нужно провести гораздо больше исследований, чтобы определить причину».
Новое исследование подчеркивает связь между жирным вкусом и ожирением
Дополнительная информация: Юлия YQ Low et al.Чувствительность вкуса к углеводам связана с потреблением крахмала и окружностью талии у взрослых, The Journal of Nutrition (2017). DOI: 10.3945 / jn.117.254078 Предоставлено Университет Дикина
Ссылка : Первое в мире открытие нового углеводного «вкуса» (2017, 30 октября) получено 22 октября 2021 г.

