Жир белый, бурый, бежевый | Наука и жизнь
У врачей есть все основания считать, что избыточный вес до добра не доводит. Как правило, с повышенной массой тела связан целый комплекс расстройств: от сердечно-сосудистых до обмена веществ. А число людей с той или иной формой ожирения постоянно растёт. Когда человек чувствует холод, мозг даёт сигнал белым адипоцитам расщепить жиры-триглицериды, и получившиеся в результате жирные кислоты с кровью приходят в бурый жир, где и «сгорают».‹
›
Как можно удержать вес в пределах нормы? Ответ, казалось бы, проще некуда — меньше ешьте, больше двигайтесь. В действенности этих средств никто не сомневается, однако помогают они далеко не всем. У некоторых людей особенности обмена веществ таковы, что жир накапливается при любой диете. Порой мы просто не можем противиться чувству голода: мозг требует калорий без оглядки на избыточный вес. Выполнять предписания насчёт физической нагрузки тоже не всегда удаётся, особенно жителям городов.
Поэтому ожирение стало одной из самых изучаемых тем в современной медицине, и усилия многих исследователей направлены на поиск средства, которое помогло бы предотвратить накопление жира. Можно, например, попытаться изменить пищевое поведение через мозг и нейроэндокринную систему. Другой путь помешать накоплению жира — воздействие на кишечную микрофлору, поскольку именно от неё во многом зависит, что из пищи будет всасываться в кровь, а что нет. Наконец, избыток липидов можно просто сжечь, то есть расщепить их в каких-нибудь обменных процессах.
Между тем жир жиру рознь. То, что откладывается на ягодицах и на талии, это белая жировая ткань, состоящая преимущественно из белых адипоцитов (жировых клеток). Их функция — запасать разнообразные липиды, и выглядят они как огромная жировая капля. Цитоплазма, ядро и другие компоненты клетки в них есть, но они ютятся где-то между липидной массой и мембраной. Иначе выглядят клетки бурого жира: в них жировых капель несколько, и в цитоплазме очень много митохондрий, которые благодаря железосодержащим белкам придают клеткам более тёмный, бурый цвет.
С биохимической точки зрения клетки бурого жира устроены на первый взгляд бессмысленно. В их митохондриях разорвана связь между окислением органических молекул (то есть липидов) и синтезом энергетических молекул АТФ. Как известно, в ходе окисления молекул в митохондриях на их внутренних мембранах создаётся градиент протонов: по одну сторону мембраны протонов больше, чем по другую. Этот градиент нужен для того, чтобы работал встроенный в мембрану фермент для синтеза АТФ: энергия, запасённая в химических связях АТФ, легко высвобождается и используется в подавляющем большинстве молекулярных процессов в клетке. А вот в буром жире энергия от окисляемых продуктов в АТФ почти не запасается. Но и впустую она не тратится, а уходит в тепло.
Все клетки в той или иной степени позволяют какой-то доле получаемой энергии утекать в тепло, однако клетки бурого жира специализированы именно на этой функции — создавать тепло из запасённых липидов. Легко догадаться, что бурые адипоциты служат важным элементом системы терморегуляции у теплокровных животных.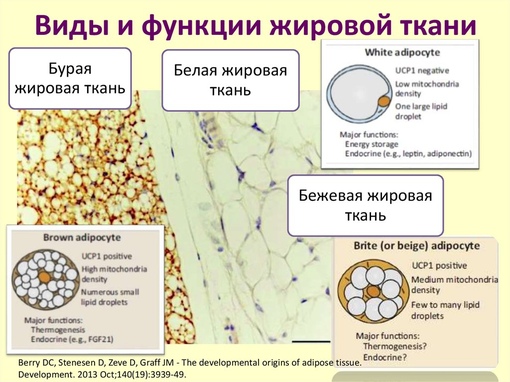 На самом деле зоологи давно заметили, что бурый жир особенно развит у зверей, впадающих в зимнюю спячку. Поддерживать температуру тела с помощью других механизмов, например дрожанием, «спящие» звери не могут, и бурый жир приходится весьма кстати.
На самом деле зоологи давно заметили, что бурый жир особенно развит у зверей, впадающих в зимнюю спячку. Поддерживать температуру тела с помощью других механизмов, например дрожанием, «спящие» звери не могут, и бурый жир приходится весьма кстати.
Бурый жир защищает от переохлаждения и младенцев, — у них он составляет до 5% от массы тела. У взрослых людей, как полагали до недавнего времени, бурые адипоциты перестают выполнять свою функцию, теряют митохондрии и превращаются в подобие обычных белых жировых клеток.
Однако несколько лет назад бурый жир нашли и у взрослых. Оказалось, какая-то его часть остаётся в районе шеи, плеч и верхней части грудной клетки. Более того, выяснилось, что количество бурого жира у взрослых увеличивается на холоде, что понятно, ведь бурый жир нужен именно для обогрева.
И поскольку «топка» бурого жира работает на липидах, сама собой возникла идея: нельзя ли использовать его для избавления от избыточного веса? Но тогда нужен некий «рубильник», который активировал бы бурую жировую ткань, когда это нужно. Чтобы реализовать эту идею, требуется, во-первых, понять молекулярные и клеточные механизмы, которые обеспечивают появление бурого жира в организме, а во-вторых, убедиться, что он действительно помогает от ожирения и сопутствующих проблем с обменом веществ.
Чтобы реализовать эту идею, требуется, во-первых, понять молекулярные и клеточные механизмы, которые обеспечивают появление бурого жира в организме, а во-вторых, убедиться, что он действительно помогает от ожирения и сопутствующих проблем с обменом веществ.
Хотя клетки бурого жира находили не только в специальных «депо», но и в толще белого жира, считалось, что у них всё равно существуют свои особые предшественники, которые потом развиваются в бурые адипоциты. Однако исследователи из Швейцарской высшей технической школы Цюриха выяснили, что белый жир и бурый жир могут непосредственно превращаться друг в друга. Эксперименты ставили на мышах, у которых следили за отдельными клетками белого жира: при понижении температуры эти клетки «бурели», а при повышении «белели». Получается, что бурый жир может образовываться непосредственно из жира белого.
Бурая жировая ткань густо пронизана кровеносными сосудами; они не только приносят ей топливо, но и забирают с собой тепло. Удалось даже найти нервные клетки, которые дают сигнал к расщеплению жиров, — ими оказались некоторые нейроны гипоталамуса. Они контролировали именно метаболическую активность клеток бурого жира. То есть аппетит и потребление пищи оставались прежними, но зато в бурожировой «топке» сжигалось большее количество калорий.
Удалось даже найти нервные клетки, которые дают сигнал к расщеплению жиров, — ими оказались некоторые нейроны гипоталамуса. Они контролировали именно метаболическую активность клеток бурого жира. То есть аппетит и потребление пищи оставались прежними, но зато в бурожировой «топке» сжигалось большее количество калорий.
Мозг может управлять бурым жиром не только с помощью собственно нейронных сигналов, но и с помощью гормонов-нейропептидов, называемых орексинами. Эти нейропептиды синтезируются опять же в гипоталамусе, участвуют в регуляции циклов сна — бодрствования и влияют на энергетический обмен и аппетит. Оказалось, что орексины напрямую действуют на клетки белого жира, способствуя их превращению в бурые адипоциты. (Возможно, что одним лишь прямым влиянием дело не ограничивается, поскольку орексины включены в сложную систему нескольких нейропептидов, контролирующих метаболизм, и могут действовать на бурый жир через своих «агентов влияния».) Если у мышей гены орексинов отключали, животные набирали вес даже при умеренном питании.
Не стоит, однако, думать, что бурый жир находится под опекой всего лишь пары-тройки нейропептидов и группы нервных клеток. Самое деятельное участие в превращении одной жировой ткани в другую принимает иммунная система. Несколько лет назад исследователи из Калифорнийского университета в Сан-Франциско (США) обнаружили, что макрофаги, присутствующие в белом жире, понуждают жировые клетки при понижении температуры стать бурыми. Обычно о макрофагах говорят как о клетках-«уборщиках», которые ликвидируют последствия «иммунных войн», и их активная роль в метаболизме выяснилась лишь недавно. Под действием особых сигнальных белков макрофаги понуждают жировую ткань к сжиганию своих запасов. А буквально недавно удалось связать иммунные сигналы, управляющие макрофагами, с работой мышц. При физических упражнениях и опять-таки при понижении окружающей температуры из мышц высвобождается особый гормон (называемый метеорин-подобным гормоном), который через иммунные сигнальные белки интерлейкины действует на макрофаги, находящиеся в жировой ткани, а дальше всё разворачивается по вышеописанному сценарию.
Расшифровка механизмов управления бурым жиром обычно сопряжена с поиском молекулярных «волшебных кнопок» — регуляторных белков, с помощью которых можно активировать появление новых бурых клеток или усилить их активность. Так, недавно исследователи из университета Содружества Виргинии (США) опубликовали статью, в которой предлагали на роль включателя бурого жира фермент киназу Tyk2. До сих пор этот фермент изучали как один из перспективных противораковых белков. (Здесь можно вспомнить о том, что ожирение часто развивается вместе с онкологическими заболеваниями.) Таких примеров много, сообщения о белках-активаторах бурого жира появляются регулярно. Естественно, в каждой подобной работе проверяется их влияние на избыточный вес. Пока что всё, что активирует бурый жир, помогает от лишнего веса избавиться. Но помогает ли бурый жир избавиться от метаболических проблем, сопровождающих ожирение?
Исследователи из Онкологического института Даны — Фарбера (США) ответили на этот вопрос утвердительно. Они нашли белок, связывающий тепловое сжигание калорий с воспалительными процессами, которые начинаются в чрезмерно разросшейся жировой ткани. Именно воспаление, как считается, провоцирует устойчивость тканей и органов к инсулину, что есть прямая дорога к диабету второго типа. Оказалось же, что белок TRPV4, содержащийся в белых адипоцитах, мешает сжиганию жира и способствует воспалительным процессам в жировой ткани. Если синтез TRPV4 подавляли, то ни ожирения, ни воспаления у подопытных животных не было, хотя питались они высококалорийной жирной пищей. На самом деле в других работах тоже отмечалась связь между активацией бурого жира и исчезновением признаков диабета, однако нужно было найти именно конкретное молекулярное связующее звено. Им оказался TRPV4. Правда, надо учитывать, что исследования такого рода лишь одним звеном не ограничиваются и обычно молекулярные биологи достают за пойманное звено целую сигнальную цепочку, каждый член которой может стать мишенью для лекарств.
Они нашли белок, связывающий тепловое сжигание калорий с воспалительными процессами, которые начинаются в чрезмерно разросшейся жировой ткани. Именно воспаление, как считается, провоцирует устойчивость тканей и органов к инсулину, что есть прямая дорога к диабету второго типа. Оказалось же, что белок TRPV4, содержащийся в белых адипоцитах, мешает сжиганию жира и способствует воспалительным процессам в жировой ткани. Если синтез TRPV4 подавляли, то ни ожирения, ни воспаления у подопытных животных не было, хотя питались они высококалорийной жирной пищей. На самом деле в других работах тоже отмечалась связь между активацией бурого жира и исчезновением признаков диабета, однако нужно было найти именно конкретное молекулярное связующее звено. Им оказался TRPV4. Правда, надо учитывать, что исследования такого рода лишь одним звеном не ограничиваются и обычно молекулярные биологи достают за пойманное звено целую сигнальную цепочку, каждый член которой может стать мишенью для лекарств.
В основном подобные эксперименты ставятся на мышах, так что резонно было бы задать вопрос, насколько полученные результаты можно экстраполировать на человека. Но буквально в июле этого года в журнале «Diabetes» вышла статья, в которой сотрудники медицинского отделения Техасского университета в Галвестоне (США) пишут об однозначной связи между количеством бурого жира у человека, уровнем глюкозы в крови и реакцией клеток на инсулин. Чем активней был бурый жир, чем больше его было, тем больше калорий сгорало и тем активней глюкоза всасывалась из крови в клетки тканей. Так что бурый жир действительно мог бы стать хорошим медицинским инструментом в борьбе с ожирением и диабетом, и учёные не зря ищут средство, с помощью которого можно было бы быстро и эффективно активировать бурую жировую ткань.
Но буквально в июле этого года в журнале «Diabetes» вышла статья, в которой сотрудники медицинского отделения Техасского университета в Галвестоне (США) пишут об однозначной связи между количеством бурого жира у человека, уровнем глюкозы в крови и реакцией клеток на инсулин. Чем активней был бурый жир, чем больше его было, тем больше калорий сгорало и тем активней глюкоза всасывалась из крови в клетки тканей. Так что бурый жир действительно мог бы стать хорошим медицинским инструментом в борьбе с ожирением и диабетом, и учёные не зря ищут средство, с помощью которого можно было бы быстро и эффективно активировать бурую жировую ткань.
Большая часть таких поисков нацелена на молекулы-мишени, вовлечённые в управление бурым жиром. Различные подходы отличаются тут по эффективности и вероятности побочных эффектов. Например, сотрудники биотехнологической компании «Genetech» утверждают, что могут активировать бурые адипоциты и нормализовать обмен веществ всего одной инъекцией антител, активирующих клеточные рецепторы к гормону FGF21 (фактору роста фибробластов 21). У мышей с диабетом, получивших инъекцию, уровень глюкозы целый месяц держался в норме, а сами мыши похудели на 10%. Однако антитела эти испытаны пока что только на животных. С другой стороны, исследователи из Кембриджа (Великобритания) полагают, что предпочтение нужно отдать «их» белку под названием BMP8B, который не просто активирует бурый жир, но делает это очень специфично — то есть, подействовав каким-то препаратом на BMP8B, мы почти не рискуем задеть другой молекулярно-клеточный процесс. Стоит также упомянуть недавно открытый гормон ирисин, — он спасает от ожирения и диабета, превращая белый жир в бурый, и при этом способствует нарастанию мышечной ткани. То есть действие этого гормона сходно с походом в тренажёрный зал: минус жир, плюс мышцы.
У мышей с диабетом, получивших инъекцию, уровень глюкозы целый месяц держался в норме, а сами мыши похудели на 10%. Однако антитела эти испытаны пока что только на животных. С другой стороны, исследователи из Кембриджа (Великобритания) полагают, что предпочтение нужно отдать «их» белку под названием BMP8B, который не просто активирует бурый жир, но делает это очень специфично — то есть, подействовав каким-то препаратом на BMP8B, мы почти не рискуем задеть другой молекулярно-клеточный процесс. Стоит также упомянуть недавно открытый гормон ирисин, — он спасает от ожирения и диабета, превращая белый жир в бурый, и при этом способствует нарастанию мышечной ткани. То есть действие этого гормона сходно с походом в тренажёрный зал: минус жир, плюс мышцы.
Среди разных советов, как активировать бурый жир, оригинально выглядит предложение использовать виагру. О том, что этот легендарный препарат ещё и от ожирения помогает, сообщили исследователи из Боннского университета (Германия), опубликовавшие в прошлом году статью в «The Journal of the Federation of American Societies for Experimental Biology». Виагра, или силденафил, увеличивала количество бурого жира у мышей, а кроме того, подавляла воспалительные процессы в белой жировой ткани.
Виагра, или силденафил, увеличивала количество бурого жира у мышей, а кроме того, подавляла воспалительные процессы в белой жировой ткани.
Ну а может ли человек сам поспособствовать увеличению в организме доли бурого жира, не дожидаясь появления лекарственных препаратов? Такой способ есть, и это — спорт и физкультура. Выше мы уже упоминали про метеорин-подобный гормон, высвобождающийся из мышц при физическом напряжении. Также мышечные нагрузки увеличивают синтез в мышцах транскрипционного фактора PGC-1α, который включает в клетках белого жира гены, превращающие их в бурые адипоциты. (Белковый фактор PGC-1α работает в сигнальной цепочке, связанной с белком TRPV4, с помощью которого удалось «связать» бурый жир с диабетом.)
Если же вы не хотите тратить время на физические упражнения, похудеть вам помогут друзья. В 2011 году исследователи из университета Огайо (США) выяснили, что повышенная социальная активность помогает толстым мышам сбросить вес, а худых защищает от ожирения, даже если кормить их жирной пищей.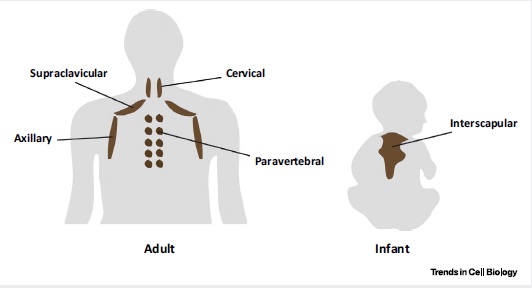 Общение с другими мышами увеличивало в организме животных долю бурого жира, а связующим молекулярным звеном был довольно известный белок под названием «нейротрофический фактор мозга» (BDNF), уровень которого повышался в нервных клетках во время интенсивной социальной жизни.
Общение с другими мышами увеличивало в организме животных долю бурого жира, а связующим молекулярным звеном был довольно известный белок под названием «нейротрофический фактор мозга» (BDNF), уровень которого повышался в нервных клетках во время интенсивной социальной жизни.
Наконец, ещё один способ активации бурого жира, который сам собой напрашивается, это холод. Действительно, если активность бурых жировых клеток увеличивается от холода, то почему бы тем, кто страдает от избыточного веса, не помёрзнуть в терапевтических целях? Оценить эффективность такого способа попытались сотрудники университета Маастрихта (Нидерланды). В течение 10 дней они заставляли добровольцев по шесть часов каждый день сидеть в помещении с температурой воздуха 15оC. Бурый жир у участников эксперимента действительно активировался, они переставали мёрзнуть, а их энергетические расходы возрастали на 30%. Правда, пока всё равно непонятно, достаточно ли такой активации для действительно значимого похудания.
Но если не хватит одного бурого жира, поможет белый, — он, как оказалось, тоже может расщеплять жир с выделением тепла, если вокруг холодает. Исследователи из Гарварда (США) выяснили, что белые адипоциты сами, без вмешательства нервной системы и независимо от бурого жира, могут чувствовать холод и участвовать в терморегуляции.
Справедливости ради нужно сказать, что с бурым жиром связаны некоторые данные, которые могут охладить энтузиазм по его поводу. Например, он, как ни странно, увеличивал в отдельных экспериментах риск атеросклероза, провоцируя увеличение доли «плохих» жиров — липопротеинов низкой плотности — в крови. Впрочем, эти результаты нужно ещё подтвердить в клинических исследованиях.
Не исключено, что разнообразие липидных тканей не ограничивается белым и бурым жиром. Два года назад сотрудники Онкологического института Даны — Фарбера (США) обнаружили, что в организме человека есть ещё и бежевый жир. Его клетки похожи на клетки бурого жира и также сжигают избыток липидов с образованием тепла, но отличаются по некоторым существенным биохимическим и генетическим характеристикам. Возможно, что те адипоциты, которые у человека считаются бурыми, на самом деле бежевые. Впрочем, даже если взрослый бурый жир действительно ненастоящий, исследователям просто нужно переключиться на бежевый», который тоже можно использовать для регуляции метаболизма и предотвращения ожирения.
Возможно, что те адипоциты, которые у человека считаются бурыми, на самом деле бежевые. Впрочем, даже если взрослый бурый жир действительно ненастоящий, исследователям просто нужно переключиться на бежевый», который тоже можно использовать для регуляции метаболизма и предотвращения ожирения.
Об активации бурого жира | Медицинский центр Doctor.ru
Бурый жир, находящийся в организме каждого человека, позволяет сжигать жиры. При его активации происходит перекачка жирных кислот из белой жировой ткани в бурую. В отличие от более распространенного собрата, откладывающегося под кожей, в сальниках и капсулах внутренних органов, бурый жир вместо накапливания энергии сжигает ее в больших количествах, выделяя тепло.
Бурый жир улучшает обмен веществ, защищая от ожирения и диабета, улучшает чувствительность к инсулину.
Специалисты Американской Диабетической Ассоциации полагают, что бурый жир содержит в себе очень важный потенциал для пациентов, страдающих ожирением и диабетом. Ткань активированного бурого жира действительно может сжечь огромное количество глюкозы и жиров и помочь контролировать уровень сахара в крови. Примечательно и то, что у людей, имеющих лишний вес, количество бурого жира снижено, а его активность подавлена.
Ткань активированного бурого жира действительно может сжечь огромное количество глюкозы и жиров и помочь контролировать уровень сахара в крови. Примечательно и то, что у людей, имеющих лишний вес, количество бурого жира снижено, а его активность подавлена.
В настоящее время появился новый медикаментозный метод накопления и активации бурого жира у взрослых людей. В медицинском центре «DOCTOR.RU» такая процедура проводится!
Мы всегда следим за новинками в сфере современной медицины и косметологии, внимательно изучаем составы, безопасность и только тогда предлагаем их Вашему вниманию. Наша позиция, как медицинского центра заключается в том, чтобы Вы могли получать множество передовых и уникальных методик на высочайшем уровне профессионализма.
Суть нового препарата заключается в том, что он после введения в определенную область отложения жира медленно и физиологически переводит клетки белого жира в бурый. То есть, увеличивается количество митохондрий в клетке жира и она работает на его сжигание из окружающих клеток белого жира. Образно мы создаем «печки-топки», в которых на постоянной основе при соблюдении нижеперечисленных правил будет плавиться жир.
Образно мы создаем «печки-топки», в которых на постоянной основе при соблюдении нижеперечисленных правил будет плавиться жир.
Эффективность работы бурой жировой ткани у человека
Бурый жир составляет не более 1-2% от массы тела. В активированном состоянии бурый жир может тратить до 300 Вт (по результатам некоторых исследований эта цифра доходит до 400 Вт) на килограмм веса взрослого человека. Это 21 кВт на 70-килограммового человека.
Для сравнения: человек среднего веса в покое сжигает около 1 кВт энергии. Улавливаете суть? Активировав бурый жир, Вы можете лежать на диване и сжигать в двадцать раз больше энергии, чем раньше.
Бурая жировая ткань: протокол активации
Как и для остальных аспектов здоровья, для бурого жира работают четыре правила: световое, температурное, нагрузочное (стрессовое) и пищевое. Давайте разберемся, каким образом мы можем активировать бурый жир.
Итак, вначале мы разберем эти правила, а затем обсудим, чего не следует делать, чтобы не уменьшать активность бурой жировой ткани.
Температурное правило
Самый главный триггер активации бурой жировой ткани – это снижение температуры окружающей среды. Суть состоит в том, что нет необходимости хранить жир, когда Вам нужно свободное тепло, чтобы выжить.
Как показали недавние исследования, для этих целей достаточно на несколько градусов снизить обычную температуру в помещении. В исследовании было установлено, что со снижением температуры окружающей среды количество сжигающих калории клеток бурой жировой ткани увеличивается. У людей с более высоким содержанием бурого жира его активация холодом улучшает показатели энергетического метаболизма.
Так, в исследовании на 5 добровольцах, в спальных комнатах которых была установлена температура на уровне 19○С, было продемонстрировано увеличение бурой жировой ткани и ее сжигающей калории активности на 30-40%. В то же время увеличение комнатной температуры до 26○С вело к снижению содержания и активности бурого жира. Вообще 19○ С – это достаточно комфортная температура. Вы можете компенсировать ее более теплым одеялом (дышать будете все равно более прохладным воздухом).
В то же время увеличение комнатной температуры до 26○С вело к снижению содержания и активности бурого жира. Вообще 19○ С – это достаточно комфортная температура. Вы можете компенсировать ее более теплым одеялом (дышать будете все равно более прохладным воздухом).
Итак, подытожим, какие правила нужно соблюдать!
1. Спим в хорошо проветриваемом помещении при температуре 19-20○С.
В другом японском исследовании, в котором приняли участие 12 человек, молодых людей с низким количеством бурого жира просили на протяжении 6 недель проводить по 2 часа в день в комнате с температурой около 17○C. В начале этого 6-недельного исследования молодые люди при 17○С сжигали в среднем около 108 ккал дополнительно (в сравнении с количеством килокалорий, сжигаемых при нормальной окружающей температуре), а в конце исследования дополнительно сжигалось уже около 289 ккал. Обратите внимание, что это всего 2 часа в день! Доктор Matthias Bluher в своих экспериментах помещал людей ежедневно на 10 минут на холод (40○C), в результате чего через 4 недели они теряли в среднем по 3-4 килограмма.
2. Уменьшаем температуру в помещениях до 20○C.
Принцип охлаждения работает абсолютно у всех. Классическая школа закаливания предлагает множество вариантов закаливания. В качестве закаливающих процедур широко используется пребывание и занятие спортом на свежем воздухе, а также водные процедуры (обтирание, обливание, купание, контрастный душ). Одним из самых распространённых видов закаливания является хождение босиком. Холодная вода отнимает тепло тела в 32 раза быстрее, чем холодный воздух. Плавание или ходьба в прохладной воде значительно увеличивает потери тепла, более чем на 50%.
При длительных перерывах в закаливании его эффект снижается или теряется совсем. Также Вы можете следить за тем, чтобы не надевать избыток одежды на улице и дома, принимать дома «воздушные ванны», которые более безопасны, чем обливание.
Пребывание ночью в прохладном помещении (при 19○C) не только увеличит количество бурого жира, но и нормализует сон, что, в свою очередь, также поможет справиться с проблемой лишнего веса.
Начинать закаливание (любое из предложенных видов) нужно только после консультации у врача, так как закаливание – это тренировка, а не лечение, и людям с заболеваниями и слабым иммунитетом подобные процедуры могут быть противопоказаны!
Закаливание следует рассматривать как попытку приблизить образ жизни человека к естественному, не дать угаснуть врождённым адаптационным способностям организма. Безусловно, снижение комнатной температуры не станет панацеей от лишнего веса, но может быть важным дополнительным шагом наряду с физической активностью и правильным питанием.
Исследования показали, что холод может быть даже эффективнее физических нагрузок! Австралийские ученые обнаружили, что дрожание от холода подобно более длительной по времени физической нагрузке и стимулирует превращение запасающего энергию белого жира в энергосжигающий бурый жир. Клетки бурого жира могут стать новой терапевтической мишенью для борьбы с ожирением, жировым перерождением печени и сахарным диабетом.
Главное – принцип безопасности!
Холодовая адаптация опосредована рецепторами на поверхности кожи, а не глубокими холодовыми рецепторами ядра. Это холодовой сенсорный афферентный цикл. Переохлаждение ядра тела очень опасно!
Нагрузочное (стрессовое правило)
Физическая нагрузка тренирует наши мышцы, делает их сильнее, одновременно сжигая калории. Собственно говоря, это касается не только мышц, а вообще любой ткани: интенсивная работа требует энергии, добываемой при расщеплении жиров. На молекулярном уровне это сопровождается активацией ряда регуляторных белков – транскрипционных факторов, которые, в свою очередь, «будят» гены, отвечающие за перестройку метаболизма в клетках и тканях.
Давно известно, что при физической нагрузке затраты энергии возрастают непропорционально сильно: энергии тратится больше, чем требуется для выполнения упражнений или работы.
Физическая активность активирует бурую жировую ткань. Этому способствуют иризин и фактор транскрипции PGC1-α.
Недавние исследования показали, что физические упражнения влекут за собой выделение неизвестного ранее гормона иризина, который заставляет белый жир становиться бурым и препятствует ожирению. Гормон служит передатчиком информации между различными тканями организма (поэтому его и назвали в честь древнегреческой богини Ириды или Ирис – вестницы Олимпа).
В одной из недавних работ было продемонстрировано, что иризин циркулирует в плазме крови всех исследованных людей, а его концентрация у молодых женщин-атлеток в несколько раз выше, чем у женщин среднего возраста, страдающих ожирением.
Известно также, что при нагрузке в скелетных мышцах повышается содержание белка – фактора транскрипции PGC1-α. В то же время известно, что когда при физической нагрузке в мышцах возрастает количество белка PGC1, это благоприятно воздействует не только на сами мышцы, но и на весь организм. У трансгенных мышей с повышенным уровнем PGC1 под старость не развивается ожирение и диабет и живут они дольше обычных. Сначала было установлено, что после 3 недель бегания в колесе или плавания у тех же трансгенных мышей (с повышенным уровнем PGC1) резко (в 25–65 раз) возрастает количество термогенина в подкожном белом жире, и там увеличивается число клеток бурого жира.
Световое правило
Исследователи из Лейденского университета нашли совсем простой способ держать бурый жир в тонусе. Оказывается, нужно просто по вечерам поменьше сидеть при искусственном свете.
Известно, что стимуляция бурого жира происходит при участии β3 адренергического рецептора. При его активации клетки сжигают больше липидов и выделяют больше тепла. Патрик
Ренсен и его коллеги обнаружили, что если мышей держать при искусственном освещении 16 часов, а то и все 24 часа в сутки, то у них снижается активность рецептора, соответственно, бурые жировые клетки начинают хуже работать, и липидные молекулы отправляются в запасающий белый жир. С мышами, у которых световой день длился стандартно 12 часов, ничего такого не происходило (заметим, что мыши – животные сумеречные, то есть светлое время суток для них – как для нас ночь).
В результате у мышей, которых долго держали на свету, накапливалось на 25-50% больше жира, хотя у животных из всех групп прием пищи и физическая активность были одинаковые.
Разумеется, тут дело не в самом по себе искусственном свете, а в суточном ритме, который портится из-за освещённости в неурочное время: биологические часы говорят о том, что уже давно должна быть ночь, а глаза продолжают видеть свет. Конечно, мы всё равно заснём, пусть и при искусственном освещении, но на биологических часах это всё равно отразится. Известно, что даже если ложиться спать в правильное время, то всё равно яркое освещение, которое сопровождает нас до последнего, само по себе может причинить вред.
Ну а то, что сбитый циркадный ритм связан с ожирением, давно уже подтверждено как практическими экспериментами, так и клиническими исследованиями. По некоторым данным, слишком долгий световой день провоцирует ожирение даже сильнее, чем неправильное питание. И, по-видимому, эффект здесь не в последнюю очередь обусловлен неправильной работой бурого жира. Его взаимодействие с биологическими часами в мозге осуществляется через симпатическую нервную систему: если бурую жировую ткань отключали от симпатических нервных путей, то эффект был такой же, как и при расстройстве суточного ритма – бурые клетки переставали сжигать жиры.
Есть ли такая же взаимосвязь между активностью бурого жира и суточным ритмом у человека, покажут дальнейшие исследования. Похожие результаты были получены специалистами из университета Вандербильта, которые обнаружили, что чувствительность к инсулину у клеток зависит от времени суток, и при нарушенном световом суточном ритме клетки начинают жить на одной только глюкозе, откладывая жиры про запас. Результат – избыточный вес! Эти эксперименты тоже ставили на животных. С другой стороны, повторим, медицинская статистика говорит о том, что и у людей нарушенный суточный ритм часто сопровождается разными нехорошими физиологическими эффектами, в том числе и в обмене веществ. В общем, тем, кто хочет похудеть, можно порекомендовать не только правильно питаться, но и вовремя ложиться спать или хотя бы не злоупотреблять перед сном всевозможными гаджетами.
Таким образом, все то, что увеличивает уровень мелатонина, увеличивает и количество бурого жира, помогая худеть. То есть, чтобы похудеть после 40-60 лет, первым делом надо нормализовать сон. Это поможет и бурый жир нарастить, и устранить те проблемы со здоровьем, к которым приводит нехватка сна.
Пищевое правило
Постоянные подъемы инсулина или повышенный уровень инсулина подавляет работу бурой жировой ткани. «Мерзлявость» – это одно из проявлений инсулинорезистентности. Поэтому соблюдение простых правил (отсутствие перекусов, выдерживание пауз между приемами пищи, снижение углеводов) помогут Вам восстановить активность бурой жировой ткани. Одно из правил интервального голодания – 12-часовой перерыв между приемами пищи – окажется очень эффективным для стимуляции и увеличения клеток бурого жира. Надо заметить,что в этот перерыв нельзя употреблять ничего, кроме чистой воды: то есть, ни таблеток, ни БАДов, ни фруктов, ни любых других напитков, кроме чистой воды. Соблюдать такой перерыв очень легко в ночное время. Смысл таков: если Вы покушали в 22:00, то завтракаете только в 10:00.
У кого снижен уровень бурого жира?
К сожалению, пока измерить уровень бурой жировой ткани сложно. Раньше для определения наличия клеток бурого жира исследователи брали участки жировой ткани на биопсию. Но благодаря успехам визуализирующих диагностических методик стало возможно идентифицировать бурый жир и без травматизации тела человека. Для определения бурой жировой ткани на сегодняшний день применяют методику ПЭТ-КТ (позитронно-эмиссионная томография с компьютерной томографией). Сразу отметим, что делать этого не нужно. Такие исследования делаются добровольцам и только в рамках научных исследований!
Группа риска:
1. Возрастные люди. С возрастом количество бурой жировой ткани уменьшается. Поэтому у взрослых бурый жир составляет лишь небольшую часть от общей массы жира.
2. Люди с избыточным весом. Неясно, причина это или следствие. Ученые это пока так и не определили. Непонятно, то ли худые люди более стройные из-за того, что у них больше бурой (активной) составляющей, то ли полные не так сильно «мёрзнут» из-за наличия дополнительной прослойки белого жира.
3. Люди с нарушенной чувствительностью к инсулину и расстройствами регуляции глюкозы. У людей с нормальным уровнем сахара коричневого жира больше, чем у тех, у кого он повышен.
4. Мужчины. Так как у женщин бурого жира больше, чем у мужчин.
5. Люди, принимающие бета-блокаторы. Они имеют меньше бурого жира, чем те, кто на этих лекарствах не сидит. Бета-блокаторы используются для лечения артериальной гипертензии.
6. Люди с заболеваниями щитовидной железы. Уменьшается активность бурого жира при проблемах со щитовидкой.
Мысли на перспективу
Холодные среды вызывают давно закопанную эпигенетическую программу у всех млекопитающих, которая позволяет преобразовывать белую жировую ткань (WAT) в бурую (BAT), чтобы жечь калории как свободное тепло, одновременно не генерируя АТФ, и не увеличивая ROS (реактивные виды кислорода). Это позволяет нам более медленно стареть, в то же время увеличивая метаболизм и способность работать на меньших калориях, при этом сжигая жир, чтобы вырабатывать тепло для согрева.
Мы снижаем наши жировые запасы в организме, улучшая композицию тела! Низкие температуры также повышают мРНК IGF-1, чрезвычайно увеличивая выброс гормона роста. Это увеличивает эффективность аутофагии и быстро улучшает мышечную и сердечную функцию. Холод делает всё это без упражнений!
Холод также увеличивает GnRH (гонадотропин-рилизинг-гормон) и способствует улучшению репродуктивной активности. Это важно в холоде, так как у большинства млекопитающих беременность протекает в течение зимних месяцев. Вот где для млекопитающих возникает связь с HCG. Лептин контролирует все яйцеклетки и плацентарную функцию у всех млекопитающих. Чем ниже уровни лептина, тем более «живой и здоровой» будет беременность. Врачи знают о крепкой связи лептина, инсулина с синдромом поликистозных яичников!
Холодные условия могут также улучшить плодовитость, потому что холод снижает количество лептина, в то время как его рецептор становится сверхчувствительным.
И самое главное: активизировать и увеличить количество бурого жира в определенных местах вам поможет введение новейшего нанопептидного препарата производства США в места локальных жировых отложений.
В медицинском центре «DOCTOR.RU» разработана и активно применяется определенная методика, которая применяется однократно и способствует созданию «депо» бурого жира в интересующих вас местах навсегда. То есть, создаем «печки-топки» для белого жира и условия для устранения проблемы навсегда. Ранее таких возможностей не было, так как любые методики снижения веса и избавления от подкожно-жировой клетчатки носили временный характер.
Даже липосакция, кавитация или мезотерапевтическое уничтожение жировых клеток не гарантирует результат навсегда. Это связано с тем, что оставшиеся жировые клетки могут увеличиваться до бесконечности.
Для понимания: количество жировых клеток одинаковое у самого худого и самого полного человека в мире, но различие заключается только в откладывающемся жире. А откладываться он может практически неограниченно. Жировая клетка может увеличиваться до огромных размеров, пределы этого увеличения практически отсутствуют. При наличии клеток бурого жира в жировой ткани любое охлаждение будет приводить к активации термогенеза, а, следовательно, к сжиганию белого жира. Все это будет работать даже в том случае, если Вы не будете соблюдать вышеперечисленных правил, так как холодный ветер или холодная погода в наших условиях всегда будут присутствовать в вашей жизни, хотя бы периодически.
Ждем вас на процедуру в медицинский центр «DOCTOR.RU»! Количество препарата определяется индивидуально. Это связано с масштабами коррекции. Процедура проводится не чаще 1 раза в год, так как полный эффект развивается только в течение 10-12 месяцев.
Источник: http://nk-doctor.ru/article/buryj-zhir/
Жир белый, бурый, бежевый
Кирилл Стасевич
«Наука и жизнь» №11, 2014
У врачей есть все основания считать, что избыточный вес до добра не доводит. Как правило, с повышенной массой тела связан целый комплекс расстройств: от сердечно-сосудистых до обмена веществ. А число людей с той или иной формой ожирения постоянно растёт.
Как можно удержать вес в пределах нормы? Ответ, казалось бы, проще некуда — меньше ешьте, больше двигайтесь. В действенности этих средств никто не сомневается, однако помогают они далеко не всем. У некоторых людей особенности обмена веществ таковы, что жир накапливается при любой диете. Порой мы просто не можем противиться чувству голода: мозг требует калорий без оглядки на избыточный вес. Выполнять предписания насчёт физической нагрузки тоже не всегда удаётся, особенно жителям городов.
Поэтому ожирение стало одной из самых изучаемых тем в современной медицине, и усилия многих исследователей направлены на поиск средства, которое помогло бы предотвратить накопление жира. Можно, например, попытаться изменить пищевое поведение через мозг и нейроэндокринную систему. Другой путь помешать накоплению жира — воздействие на кишечную микрофлору, поскольку именно от неё во многом зависит, что из пищи будет всасываться в кровь, а что нет. Наконец, избыток липидов можно просто сжечь, то есть расщепить их в каких-нибудь обменных процессах.
Между тем жир жиру рознь. То, что откладывается на ягодицах и на талии, это белая жировая ткань, состоящая преимущественно из белых адипоцитов (жировых клеток). Их функция — запасать разнообразные липиды, и выглядят они как огромная жировая капля. Цитоплазма, ядро и другие компоненты клетки в них есть, но они ютятся где-то между липидной массой и мембраной. Иначе выглядят клетки бурого жира: в них жировых капель несколько, и в цитоплазме очень много митохондрий, которые благодаря железосодержащим белкам придают клеткам более тёмный, бурый цвет.
С биохимической точки зрения клетки бурого жира устроены на первый взгляд бессмысленно. В их митохондриях разорвана связь между окислением органических молекул (то есть липидов) и синтезом энергетических молекул АТФ. Как известно, в ходе окисления молекул в митохондриях на их внутренних мембранах создаётся градиент протонов: по одну сторону мембраны протонов больше, чем по другую. Этот градиент нужен для того, чтобы работал встроенный в мембрану фермент для синтеза АТФ: энергия, запасённая в химических связях АТФ, легко высвобождается и используется в подавляющем большинстве молекулярных процессов в клетке. А вот в буром жире энергия от окисляемых продуктов в АТФ почти не запасается. Но и впустую она не тратится, а уходит в тепло.
Все клетки в той или иной степени позволяют какой-то доле получаемой энергии утекать в тепло, однако клетки бурого жира специализированы именно на этой функции — создавать тепло из запасённых липидов. Легко догадаться, что бурые адипоциты служат важным элементом системы терморегуляции у теплокровных животных. На самом деле зоологи давно заметили, что бурый жир особенно развит у зверей, впадающих в зимнюю спячку. Поддерживать температуру тела с помощью других механизмов, например дрожанием, «спящие» звери не могут, и бурый жир приходится весьма кстати.
Бурый жир защищает от переохлаждения и младенцев, — у них он составляет до 5% от массы тела. У взрослых людей, как полагали до недавнего времени, бурые адипоциты перестают выполнять свою функцию, теряют митохондрии и превращаются в подобие обычных белых жировых клеток.
Однако несколько лет назад бурый жир нашли и у взрослых. Оказалось, какая-то его часть остаётся в районе шеи, плеч и верхней части грудной клетки. Более того, выяснилось, что количество бурого жира у взрослых увеличивается на холоде, что понятно, ведь бурый жир нужен именно для обогрева.
И поскольку «топка» бурого жира работает на липидах, сама собой возникла идея: нельзя ли использовать его для избавления от избыточного веса? Но тогда нужен некий «рубильник», который активировал бы бурую жировую ткань, когда это нужно. Чтобы реализовать эту идею, требуется, во-первых, понять молекулярные и клеточные механизмы, которые обеспечивают появление бурого жира в организме, а во-вторых, убедиться, что он действительно помогает от ожирения и сопутствующих проблем с обменом веществ.
Хотя клетки бурого жира находили не только в специальных «депо», но и в толще белого жира, считалось, что у них всё равно существуют свои особые предшественники, которые потом развиваются в бурые адипоциты. Однако исследователи из Швейцарской высшей технической школы Цюриха выяснили, что белый жир и бурый жир могут непосредственно превращаться друг в друга. Эксперименты ставили на мышах, у которых следили за отдельными клетками белого жира: при понижении температуры эти клетки «бурели», а при повышении «белели». Получается, что бурый жир может образовываться непосредственно из жира белого.
Бурая жировая ткань густо пронизана кровеносными сосудами; они не только приносят ей топливо, но и забирают с собой тепло. Удалось даже найти нервные клетки, которые дают сигнал к расщеплению жиров, — ими оказались некоторые нейроны гипоталамуса. Они контролировали именно метаболическую активность клеток бурого жира. То есть аппетит и потребление пищи оставались прежними, но зато в бурожировой «топке» сжигалось большее количество калорий.
Мозг может управлять бурым жиром не только с помощью собственно нейронных сигналов, но и с помощью гормонов-нейропептидов, называемых орексинами. Эти нейропептиды синтезируются опять же в гипоталамусе, участвуют в регуляции циклов сна–бодрствования и влияют на энергетический обмен и аппетит. Оказалось, что орексины напрямую действуют на клетки белого жира, способствуя их превращению в бурые адипоциты. (Возможно, что одним лишь прямым влиянием дело не ограничивается, поскольку орексины включены в сложную систему нескольких нейропептидов, контролирующих метаболизм, и могут действовать на бурый жир через своих «агентов влияния».) Если у мышей гены орексинов отключали, животные набирали вес даже при умеренном питании.
Не стоит, однако, думать, что бурый жир находится под опекой всего лишь пары-тройки нейропептидов и группы нервных клеток. Самое деятельное участие в превращении одной жировой ткани в другую принимает иммунная система. Несколько лет назад исследователи из Калифорнийского университета в Сан-Франциско (США) обнаружили, что макрофаги, присутствующие в белом жире, понуждают жировые клетки при понижении температуры стать бурыми. Обычно о макрофагах говорят как о клетках-«уборщиках», которые ликвидируют последствия «иммунных войн», и их активная роль в метаболизме выяснилась лишь недавно. Под действием особых сигнальных белков макрофаги понуждают жировую ткань к сжиганию своих запасов. А буквально недавно удалось связать иммунные сигналы, управляющие макрофагами, с работой мышц. При физических упражнениях и опять-таки при понижении окружающей температуры из мышц высвобождается особый гормон (называемый метеорин-подобным гормоном), который через иммунные сигнальные белки интерлейкины действует на макрофаги, находящиеся в жировой ткани, а дальше всё разворачивается по вышеописанному сценарию.
Расшифровка механизмов управления бурым жиром обычно сопряжена с поиском молекулярных «волшебных кнопок» — регуляторных белков, с помощью которых можно активировать появление новых бурых клеток или усилить их активность. Так, недавно исследователи из университета Содружества Виргинии (США) опубликовали статью, в которой предлагали на роль включателя бурого жира фермент киназу Tyk2. До сих пор этот фермент изучали как один из перспективных противораковых белков. (Здесь можно вспомнить о том, что ожирение часто развивается вместе с онкологическими заболеваниями.) Таких примеров много, сообщения о белках-активаторах бурого жира появляются регулярно. Естественно, в каждой подобной работе проверяется их влияние на избыточный вес. Пока что всё, что активирует бурый жир, помогает от лишнего веса избавиться. Но помогает ли бурый жир избавиться от метаболических проблем, сопровождающих ожирение?
Исследователи из Онкологического института Даны—Фарбера (США) ответили на этот вопрос утвердительно. Они нашли белок, связывающий тепловое сжигание калорий с воспалительными процессами, которые начинаются в чрезмерно разросшейся жировой ткани. Именно воспаление, как считается, провоцирует устойчивость тканей и органов к инсулину, что есть прямая дорога к диабету второго типа. Оказалось же, что белок TRPV4, содержащийся в белых адипоцитах, мешает сжиганию жира и способствует воспалительным процессам в жировой ткани. Если синтез TRPV4 подавляли, то ни ожирения, ни воспаления у подопытных животных не было, хотя питались они высококалорийной жирной пищей. На самом деле в других работах тоже отмечалась связь между активацией бурого жира и исчезновением признаков диабета, однако нужно было найти именно конкретное молекулярное связующее звено. Им оказался TRPV4. Правда, надо учитывать, что исследования такого рода лишь одним звеном не ограничиваются и обычно молекулярные биологи достают за пойманное звено целую сигнальную цепочку, каждый член которой может стать мишенью для лекарств.
В основном подобные эксперименты ставятся на мышах, так что резонно было бы задать вопрос, насколько полученные результаты можно экстраполировать на человека. Но буквально в июле этого года в журнале Diabetes вышла статья, в которой сотрудники медицинского отделения Техасского университета в Галвестоне (США) пишут об однозначной связи между количеством бурого жира у человека, уровнем глюкозы в крови и реакцией клеток на инсулин. Чем активней был бурый жир, чем больше его было, тем больше калорий сгорало и тем активней глюкоза всасывалась из крови в клетки тканей. Так что бурый жир действительно мог бы стать хорошим медицинским инструментом в борьбе с ожирением и диабетом, и учёные не зря ищут средство, с помощью которого можно было бы быстро и эффективно активировать бурую жировую ткань.
Большая часть таких поисков нацелена на молекулы-мишени, вовлечённые в управление бурым жиром. Различные подходы отличаются тут по эффективности и вероятности побочных эффектов. Например, сотрудники биотехнологической компании «Genetech» утверждают, что могут активировать бурые адипоциты и нормализовать обмен веществ всего одной инъекцией антител, активирующих клеточные рецепторы к гормону FGF21 (фактору роста фибробластов 21). У мышей с диабетом, получивших инъекцию, уровень глюкозы целый месяц держался в норме, а сами мыши похудели на 10%. Однако антитела эти испытаны пока что только на животных. С другой стороны, исследователи из Кембриджа (Великобритания) полагают, что предпочтение нужно отдать «их» белку под названием BMP8B, который не просто активирует бурый жир, но делает это очень специфично — то есть подействовав каким-то препаратом на BMP8B, мы почти не рискуем задеть другой молекулярно-клеточный процесс. Стоит также упомянуть недавно открытый гормон ирисин, — он спасает от ожирения и диабета, превращая белый жир в бурый, и при этом способствует нарастанию мышечной ткани. То есть действие этого гормона сходно с походом в тренажёрный зал: минус жир, плюс мышцы.
Среди разных советов, как активировать бурый жир, оригинально выглядит предложение использовать виагру. О том, что этот легендарный препарат ещё и от ожирения помогает, сообщили исследователи из Боннского университета (Германия), опубликовавшие в прошлом году статью в The Journal of the Federation of American Societies for Experimental Biology. Виагра, или силденафил, увеличивала количество бурого жира у мышей, а кроме того, подавляла воспалительные процессы в белой жировой ткани.
Ну а может ли человек сам поспособствовать увеличению в организме доли бурого жира, не дожидаясь появления лекарственных препаратов? Такой способ есть, и это — спорт и физкультура. Выше мы уже упоминали про метеорин-подобный гормон, высвобождающийся из мышц при физическом напряжении. Также мышечные нагрузки увеличивают синтез в мышцах транскрипционного фактора PGC-1α, который включает в клетках белого жира гены, превращающие их в бурые адипоциты. (Белковый фактор PGC-1α работает в сигнальной цепочке, связанной с белком TRPV4, с помощью которого удалось «связать» бурый жир с диабетом.)
Если же вы не хотите тратить время на физические упражнения, похудеть вам помогут друзья. В 2011 году исследователи из университета Огайо (США) выяснили, что повышенная социальная активность помогает толстым мышам сбросить вес, а худых защищает от ожирения, даже если кормить их жирной пищей. Общение с другими мышами увеличивало в организме животных долю бурого жира, а связующим молекулярным звеном был довольно известный белок под названием «нейротрофический фактор мозга» (BDNF), уровень которого повышался в нервных клетках во время интенсивной социальной жизни.
Наконец, ещё один способ активации бурого жира, который сам собой напрашивается, это холод. Действительно, если активность бурых жировых клеток увеличивается от холода, то почему бы тем, кто страдает от избыточного веса, не помёрзнуть в терапевтических целях? Оценить эффективность такого способа попытались сотрудники университета Маастрихта (Нидерланды). В течение 10 дней они заставляли добровольцев по шесть часов каждый день сидеть в помещении с температурой воздуха 15°C. Бурый жир у участников эксперимента действительно активировался, они переставали мёрзнуть, а их энергетические расходы возрастали на 30%. Правда, пока всё равно непонятно, достаточно ли такой активации для действительно значимого похудания.
Но если не хватит одного бурого жира, поможет белый, — он, как оказалось, тоже может расщеплять жир с выделением тепла, если вокруг холодает. Исследователи из Гарварда (США) выяснили, что белые адипоциты сами, без вмешательства нервной системы и независимо от бурого жира, могут чувствовать холод и участвовать в терморегуляции.
Справедливости ради нужно сказать, что с бурым жиром связаны некоторые данные, которые могут охладить энтузиазм по его поводу. Например, он, как ни странно, увеличивал в отдельных экспериментах риск атеросклероза, провоцируя увеличение доли «плохих» жиров — липопротеинов низкой плотности — в крови. Впрочем, эти результаты нужно ещё подтвердить в клинических исследованиях.
Не исключено, что разнообразие липидных тканей не ограничивается белым и бурым жиром. Два года назад сотрудники Онкологического института Даны—Фарбера (США) обнаружили, что в организме человека есть ещё и бежевый жир. Его клетки похожи на клетки бурого жира и также сжигают избыток липидов с образованием тепла, но отличаются по некоторым существенным биохимическим и генетическим характеристикам. Возможно, что те адипоциты, которые у человека считаются бурыми, на самом деле бежевые. Впрочем, даже если взрослый бурый жир действительно ненастоящий, исследователям просто нужно переключиться на бежевый, который тоже можно использовать для регуляции метаболизма и предотвращения ожирения.
откуда он в нас берется и зачем нужен – блог FITBAR.RU
Помимо известного всем нам белого жира, который отвечает за накопление энергии, человеческое тело содержит в себе ещё и жир бурого цвета . Бурый жир заложен в нас как неотъемлемая часть организма при рождении. Какие функции он выполняет, и почему играет важную роль в жизни человека? Рассказываем всё, что знаем о буром жире в этой статье.
Бурый жир: почему он есть и сколько его в нас
У детей первого месяца жизни, бурая жировая ткань составляет ок. 5% от массы тела, и находится в районе почек, шеи, плеч и верхней части спины. В первые 2 недели, она служит младенцам средством адаптации к окружающему миру, позволяя поддерживать терморегуляцию на нужном уровне. По истечении двухнедельного срока, количество бурого жира в организме начинает снижаться, и у взрослого человека не превышает показателя в 2%.
Продолжительное время, ученые считали, что функции бурого жира в организме человека полностью утрачивают своё значение к концу первого года жизни. Только в 2008 году, благодаря появлению новой системы визуализации метаболизма в тканях, было доказано, что жировая ткань бурого цвета оказывает влияние на жизненные процессы. Также стало ясно, что большая часть бурого жира располагается в области над ключицей ,и его вес составляет всего около 20-30 гр. Однако, этого количества вполне достаточно, чтобы выполнять несколько важнейших для здоровья функций.
Бурый жир: почему он так нужен
Наличие бурого жира в организме человека — одна из причин, почему мы как вид существуем до сих пор. Процесс термогенеза, позволяющий температуре тела находиться на одном и том же уровне, не был бы возможен без наличия бурой жировой ткани. Но, хотя терморегуляция является важнейшим фактором в жизни человека, есть ещё две важнейших функции бурого жира в нашем организме: жиросжигание и контроль уровня сахара в крови.
В отличии от белого жира, который имеется у каждого человека в более значительном объёме и отвечает за накопление энергетических единиц, бурый жир выполняет противоположную функцию . Он пережигает энергию в больших количествах, превращая её в тепло и производя перекачку жирных кислот из белого жира в бурый. Причем, для того, чтобы получить нужное количество энергоединиц, бурый жир начинает задействовать белый, особенно в условиях низких температур . Также этот процесс обусловлен продолжительностью светового дня: чем он короче, тем выше активность бурого жира у человека.
Интересно, что вырабатываемая жировой бурой тканью энергия колоссальна: она способна достигать показателя в 300 — 400 ватт/, или 21 Кватт на кг веса! Это потрясающе, потому что в состоянии покоя человек расходует не более 1 Кватта/на кг массы, что меньше в 21 раз. Таким образом, если бурая жировая ткань активна (например, при низких температурах), то человеческий организм даже не двигаясь пережигает белый жир, и избавляется от лишних кило.
Что касается влияния бурого жира на уровень сахара в крови, то здесь он выступает опять же в роли «пережигателя», только уже для глюкозы, причем в огромных объёмах. Поэтому активность бурой жировой ткани позволяет избежать возникновения сахарного диабета.
Бурый жир — полезная составляющая человека, но тогда встаёт вопрос: как можно его активизировать? Некоторые специалисты считают, что заставить «работать» бурую жировую ткань способны:
- ежедневный холодный душ
- ледяные ванны три раза в неделю
- приём около 0,5 литра ледяной воды каждое утро
- прикладывание льда к груди и спине по 30 мин./в день
Однако, эффективность подобных рекомендаций пока не получила научного подтверждения. Ввиду недавнего доказательства наличия бурой жировой ткани у человека, его потенциал пока не изучен до конца. Но даже то, что бурый жир помогает бороться с сахарным диабетом и ожирением уже послужило толчком к поиску учеными средства, позволяющего активизировать этот вид ткани в человеческом организме. На сегодняшний день, препараты, которые позволят стимулировать активизацию бурого жира находятся в стадии разработки, и должны появиться на рынке в ближайшее десятилетие.
Не пропусти интересные новости и события в телеграм-канале: https://tlgg.ru/fitbarnews
Оцените статью
Как сделать белый жир – бурым, или «Таблетка» от ожирения
: 07.08.2015Жировая ткань, как известно, бывает двух видов – белая и бурая. Белый жир, «работающий» на долгосрочное запасание энергии в виде молекул АТФ, с трудом расщепляется – именно он откладывается у нас на животе и бедрах. Клетки бурого жира устроены по-другому: они содержат много митохондрий, в энергетическом цикле которых разорвана связь между окислением липидов и синтезом АТФ. Поэтому вся энергия, получаемая при окислении веществ в клетках бурого жира, превращается в тепло — он как будто специально создан, чтобы сжигать калории и помогать нам худеть! Но подавляющую часть жировой ткани во взрослом организме составляет белая, а бурая в относительно большом количестве есть только у грызунов, у животных, впадающих в спячку, и новорожденных детей. Точнее, так считалось до недавнего времени…
В 2009 г. совершенно случайно, при проведении диагностических процедур по поводу опухоли было обнаружено, что и у взрослых людей есть бурый жир. Это удалось сделать благодаря методу визуализации активного метаболизма в ткани – позитронно-эмиссионной томографии, объединенной с компьютерной томографией. В том же году пять независимых групп исследователей подтвердили этот результат, доказав, что в шейно-надключичной области взрослых людей действительно имеются участки жировой ткани, биохимически и гистологически идентичные бурому жиру.
Правда, доля людей, у которых имеются существенные отложения такого жира, оказалась совсем небольшой — 3% мужчин и 7,5% женщин. Хотя в одном из экспериментов, где участвовали молодые мужчины, у 23 человек из 24 испытуемых наблюдалось повышение метаболической активности бурого жира под действием холода. И, кстати, эта активность была обратно пропорциональна уровню избыточного веса.
Все эти изыскания привели к признанию того факта, что бурый жир так или иначе может присутствовать у взрослых людей, и увеличение его количества или активности может быть мишенью для фармакологического вмешательства, конечная цель которого – борьба с ожирением и сопутствующими ему заболеваниями, такими как сахарный диабет.
После этого работа закипела. Как обычно, начали с лабораторных мышей, и одно из таких исследований чуть не произвело сенсацию. Было обнаружено, что белый жир может превращаться в бурый под воздействием гормона иризина, который вырабатывается в организме человека естественным путем при выполнении физических упражнений. К сожалению, также выяснилось, что в отличие от мышей у людей в бурый жир под действием иризина трансформируются лишь единичные клетки белого жира. Конечно, эти результаты – хорошее подтверждение пользы умеренных физических нагрузок, но это все же не «волшебная таблетка».
Что касается человека, то при проведении экспериментов на клетках человеческой белой жировой ткани их все же удалось заставить приобретать признаки бурой жировой ткани — под действием холода. При этом в клетках возрастал уровень характерного для митохондрий бурого жира белка UCP1 (термогенина), который и содействует превращению жира непосредственно в тепло. И здесь опять можно вспомнить слова известной песенки «закаляйся, если хочешь быть здоров» и понять, что холод – это все же не метод терапии.
Но вот недавно ученые из медицинского отделения Техасского университета (Галвестон, США) обнаружили, что у человека белый жир приобретает свойства бурого в еще одной ситуации – при ожогах третьей степени.
Все началось с наблюдений, что людям после тяжелых ожогов во время восстановительного периода требуется больше калорий для поддержания массы тела, чем обычно. В исследовании на 48 больных с тяжелыми ожогами у одной группы больных образцы жировой ткани были взяты в первые дни после поступления в больницу, у другой – через несколько недель, в восстановительном периоде.
Выяснилось, что в клетках жировой ткани второй группы уровень термогенина был существенно повышен, т.е. клетки начали приобретать функциональные признаки бурой жировой ткани. Хотя такой жир был не столь эффективен как «естественный», но даже он позволял сжигать в среднем 263 дополнительных калории каждый день без каких-либо изменений физической нагрузки или питания. Если бы удалось добиться такого уровня повышения активности бурого жира медикаментозным способом, то это было бы вполне достаточно для применения на практике.
Ученые предполагают, что преобразование белого жира в бурый в случае ожогов связано с компенсаторной реакцией организма на потерю значительной части кожи – органа, участвующего в поддержании терморегуляции. Сейчас ученые исследуют, какие конкретно молекулярные механизмы опосредуют такое преобразование клеток жира: возможно, его запускает высокий уровень адреналина – гормона стресса. Только после того, как будут выяснены точные молекулярные механизмы этого явления, мы сможем приблизиться к конечной цели – разработке лекарства от излишнего веса.
По: http://news.sciencemag.org и http://www.ncbi.nlm.nih.gov
Подготовила Мария Перепечаева
: 07.08.2015Ученые открыли самый опасный ген ожирения
Новое, чрезвычайно интересное исследование опубликовал всемирно известный научный журнал Cell Metabolism. Ученые из института Каролинска в Швеции выявили ген, который, по их мнению, отвечает за развитие самого опасного в плане осложнений жира в организме человека. Ученые говорят, что ген может быть фактором риска развития инсулинорезистентности и сахарного диабета 2 типа.
Белый и бурый жир
Исследователи говорят, что ген EBF1 может быть ответственнен за развитие белой жировой ткани — или «плохого жира — в людях.
Белая жировая ткань, известная как «плохой» жир, представляет собой рыхлую ткань, состоящую в основном из жировых клеток, называемых адипоцитами. Эти жировые клетки выполняют функцию хранения и высвобождения энергии в организме. Существует два типа жира у человека: белый жир (белая жировая ткань) и бурый жир (бурая жировая ткань). В последние годы бурый жир был признан «хорошим» жиром. Было показано, что его основная роль состоит в кумуляции и выработке энергии для обеспечения физиологических процессов. Ученые выяснили, что у людей с нормальным весом более вероятно накопление именно бурого жира, и при физической нагрузке он служит энергетическим субстратом.
В противоположность бурому, белый жир считается «плохим» жиром. У тех, кто имеет избыточный вес или страдает ожирением, как правило, накапливается избыточное количество белого жира в подкожной клетчатке.
По мнению шведских исследователей, увеличение размера или количества жировых клеток может привести к избыточному накоплению белой жировой ткани. Специалисты отмечают, что по данным последних исследований наличие небольшого количества крупных жировых клеток – гипертрофированных адипоцитов – связано с повышением риска развития сахарного диабета 2 типа. А в своем последнем исследовании, опубликованном в журнале Cell Metabolism, ученые обнаружили, что гипертрофия связана с геном под названием EBF1. Низкая экспрессия EBF1 способствует развитию гипертрофии адипоцитов и инсулинорезистентности.
Ген ожирения
В ходе исследования команда ученых набирала образцы жировой ткани у участников, которые имели мелкие или крупные жировые клетки. Было обнаружено, что у пациентов с укрупненными жировыми клетками экспрессия EBF1 в жировой ткани гораздо ниже по сравнению с лицами, у которых жировые клетки были небольших размеров. Также у этих лиц был изменен транспорт липидов движение в крови и инсулинорезистентность. Инсулинорезистентность является неспособностью клеток организма адекватно реагировать на гормон инсулин, когда происходит повышение уровня глюкозы в крови (например, после приема пищи). Инсулинорезистентность является важным фактором риска развития диабета у людей с крупными адипоцитами, т.к. при инсулинорезистентности нередко повышается уровень глюкозы и липидов в крови.
Дальнейшие эксперименты проводились на мышах, у которых была целенаправленно снижена экспрессия гена EBF1 ген. У мышей развивалась гипертрофия жировых клеток, а из адипоцитов начинали интенсивно высвобождаться липиды. Когда мышей кормили продуктами с высоким содержанием жиров, у них развивалась инсулинорезистентность.
Новые возможности
Исследователи выяснили, что ген EBF1 действует как фактор транскрипции. Он связывается с белком, который управляет другими генами, регулирует образование жировых клеток и контролирует ход некоторых метаболических процессов. Один из соавторов материала, профессор Петр Арнер говорит, что эти результаты могут дать новые возможности лечения диабета типа 2: «Наши данные являются важным шагом вперед в понимании того, каким образом жировая ткань связана с развитием метаболических расстройств. Это первый случай обнаружения гена, который может привести к нарушению обмена веществ в жировой ткани человека. В будущем, вероятно, будет возможно разработать препараты, которые улучшают функцию EBF1 в жировой ткани. Это в свою очередь откроет новые пути лечения диабета 2 типа».
Очень часто научные разработки находят широкое практическое применение. Яркий пример – криолиполиз, или разрушение жировой ткани под действием холода. Одним из эффективных, удобных, современных и безопасных способов устранения локальных избыточных жировых отложений, которые плохо поддаются диетам и физическим упражнениям, признана процедура ZLipo Med. Непосредственно в области жировой ловушки формируется складка кожи и подкожной клетчатки, помещается в специальный аппликатор и охлаждается. Жировая ткани естественным образом разрушается, а её остатки выводятся из организма. Эффект всего от одной процедуры поражает воображение – обработанные участки уменьшаются в объёме ткани на 20-25% за счёт жировой ткани.
Бурая жировая ткань связана с кардиометаболическим здоровьем — Ассоциация гинекологов-эндокринологов России
Brown adipose tissue is associated with cardiometabolic health
Согласно результатам крупного исследования, наличие бурой жировой ткани по данным визуализационных методик связано со снижением риска кардиометаболических нарушений, включая диабет 2 типа, артериальную гипертензию и ишемическую болезнь сердца, эта корреляция оказалась особенно выраженной у лиц с ожирением.
Бурая жировая ткань (англ. brown adipose tissue) ─ один из двух видов жировой ткани у млекопитающих. Хотя особенности бурого жира изучались в течение многих лет у новорожденных и в исследованиях на животных, только в последнее время этому вопросу стали уделять большое внимание у взрослых лиц. Было показано, что содержание бурого жира снижается с возрастом.
В отличие от белых адипоцитов (клеток белой жировой ткани), имеющих одну крупную жировую каплю, в адипоцитах бурого жира обнаруживается некоторое число небольших жировых капель и множество митохондрий, содержащих железо, что определяет бурый цвет этой ткани. Окислительная активность митохондрий бурого жира в 20 раз превышает таковую белого жира. В отличие от сохраняющего энергию белого жира, бурый жир обладает термогенными свойствами и способен «сжигать» энергию, поэтому повышение его содержания связано с улучшением метаболических процессов в организме.
Новое исследование является самым крупным, выполненным с участием людей и подтвердившим ранее полученные данные о благоприятном влиянии бурого жира на здоровье. Доктор Tobias Becher и его коллеги из Рокфеллеровского университета (Rockefeller University, Нью Йорк) 4 января с.г. опубликовали онлайн статью в журнале Nature Medicine. По мнению авторов, их исследование «указывает на важный вклад бурой жировой ткани в кардиометаболическое здоровье, что может означать определенный терапевтический потенциал у человека».
Долгое время проведение крупномасштабных исследований бурого жира казалось практически невозможным, потому что он обнаруживается только при использовании методов визуализации и представляется неэтичным подвергать пациентов облучению только для изучения этого вопроса. В 2009 г. авторам данной статьи пришла в голову мысль, что недалеко от их лаборатории многие тысячи пациентов ежегодно посещают Memorial Sloan Kettering Cancer Center для проведения позитронно-эмиссионной томографии (ПЭТ) / компьютерной томографии (КТ) в ходе скрининга на онкологические заболевания. Поскольку радиологи обычно обращают внимание на наличие бурой жировой ткани и упоминают о ней в своих заключениях, чтобы не было неверного истолкования таких находок при скрининге рака, эта информация была доступна в электронной медицинской документации, как и данные о наличии заболеваний. Это позволило Becher и его коллегам изучить возможную взаимосвязь между наличием бурого жира и состоянием здоровья пациентов.
Авторы провели анализ результатов 134 529 ПЭТ / КT сканирований, выполненных у 52 487 пациентов между июнем 2009 г. и мартом 2018 г. Участники были разделены на 2 группы по наличию или отсутствию у них бурой жировой ткани. В целом, бурый жир был обнаружен у 5 070 пациентов (9,7%), чаще у женщин, чем у мужчин (13,8% vs. 4,9%; P < 0,0001) и его содержание снижалось с возрастом (P < 0,0001), что подтверждало данные предыдущих исследований. Наличие бурого жира независимо коррелировало с более низким риском кардиометаболических нарушений, а именно, с вероятностью наличия диабета 2 типа, диспипидемии, ИБС, гипертензии и сердечно-сосудистых заболеваний в целом, а также с лучшими показателями глюкозы в крови, триглицеридов и липопротеинов высокой плотности холестерина. Благоприятное воздействие бурой жировой ткани особенно отчетливо проявлялось у лиц с избыточным весом или ожирением, что подчеркивает потенциальную роль бурого жира в поддержании кардиометаболического здоровья.
Авторы отнесли к ограничениям своего исследования достаточно низкое число пациентов с наличием бурого жира (примерно 10% от общего числа участников). Вероятно, это число можно считать заниженным из-за выборки пациентов и тех рекомендаций, которые они получали перед скринингом, например, избегать физические нагрузки и потребление кофеина, т.е. тех влияний, которые, как полагают, способствует увеличению массы бурого жира.
Источник:
Becher T, Palanisamy S, Kramer DJ, et al. Brown adipose tissue is associated with cardiometabolic health. Nature Medicine Published 04 January 2021 https://www.nature.com/articles/s41591-020-1126-7
Примечание
Эстрогены оказывают значительное модулирующее влияние на энергетический баланс в организме и метаболизм жировой ткани, в том числе, благодаря центральному и периферическому влиянию на термогенез в бурой жировой ткани. Известно, что формирование висцерального ожирения в переходном периоде происходит до стойкого снижения уровня эстрогенов. В последние годы внимание исследователей обращено на другой гормон ─ ФСГ, рецепторы которого присутствуют во многих тканях, помимо яичников, вследствие чего повышение его уровня может приводить к метаболическим нарушениям [Chrusciel M, et al. Extragonadal FSHR Expression and Function─Is It Real? Front Endocrinol (Lausanne) 2019;10:32; Wang X, et al. Follicle stimulating hormone, its association with glucose and lipid metabolism during the menopausal transition. Obstet Gynecol Res 2020;46(8):1419-1424]. Повышение уровня ФСГ у женщин в переходном периоде может быть связано не только с возникновением вазомоторных симптомов и снижением костной массы, но также с нарушениями метаболических процессов, в том числе, термогенеза в буром жире [Liu P, et al. Blocking FSH Induces Thermogenic Adipose Tissue and Reduces Body Fat. Nature 2017;546(7656): 107–112].
Чем бурый жир отличается от других жиров?
Коричневый жир, также называемый коричневой жировой тканью, — это особый тип телесного жира, который включается (активируется), когда вы простужаетесь. Бурый жир выделяет тепло, помогающее поддерживать температуру тела в холодных условиях.
Коричневый жир содержит намного больше митохондрий, чем белый жир. Эти митохондрии являются «двигателями» бурого жира, которые сжигают калории для производства тепла.
Коричневый жир вызвал интерес у исследователей, потому что, похоже, он может использовать обычный телесный жир в качестве топлива.Кроме того, упражнения могут стимулировать гормоны, активирующие бурый жир.
Еще слишком рано говорить о том, можно ли использовать калорийность бурого жира для похудения. А пока не забудьте включить физическую активность в свои планы по снижению веса.
05 ноября 2020 г. Показать ссылки- Loh RKC, et al. Коричневая жировая ткань человека как мишень для лечения ожирения; за пределами термогенеза, вызванного холодом. Обзоры ожирения. 2017; 11: 1227. https: // онлайн-библиотека.wiley.com/doi/abs/10.1111/obr.12584. По состоянию на 8 октября 2018 г.
- Leung WKC и др. Ассоциация маркеров провоспалительного фенотипа и бежевого адипогенеза с метаболическим синдромом у взрослых китайцев с центральным ожирением. Журнал исследований диабета. 2018; 2018: 8956509. https://www.hindawi.com/journals/jdr/2018/8956509/. По состоянию на 8 октября 2018 г.
- Hwang Y-C и др. Отношение массы скелетных мышц к площади висцерального жира является основным фактором, связывающим циркулирующий иризин с метаболическим фенотипом.Сердечно-сосудистая диабетология. 2016; 15: 9. https://cardiab.biomedcentral.com/articles/10.1186/s12933-015-0319-8. По состоянию на 8 октября 2018 г.
- Ян X и др. Замена вредного висцерального жира на полезное сжигание энергии улучшает метаболические дисфункции. JCI Insight. 2017; 2: e89044. https://insight.jci.org/articles/view/89044. По состоянию на 8 октября 2018 г.
- Schwartz MW и др. Патогенез ожирения: научное заявление эндокринного общества. Эндокринные обзоры. 2017; 38: 267.
- Hensrud DD (заключение эксперта).Клиника Мэйо, Рочестер, Миннесота, 8 октября 2018 г.
- Браун К. и др. Неадренергический контроль липолиза и термогенеза в жировой ткани. Журнал экспериментальной биологии. 2018; 221: 165381.
.
Что такое коричневый жир? 5 увлекательных фактов
У каждого есть хоть немного бурого жира. В отличие от обычного старого белого жира, в котором накапливаются калории, бурые жировые клетки, заполненные митохондриями, сжигают энергию и выделяют тепло.
Когда-то считалось, что у людей только младенцы имеют бурый жир. Но в 2009 году исследователи обнаружили небольшое количество бурого жира у взрослых. Более того, они обнаружили, что люди с более низким индексом массы тела (ИМТ), как правило, имеют больше коричневого жира. Это открытие предполагает «потенциальную роль коричневого [жира] в метаболизме взрослого человека», — писали исследователи в своих выводах.
Из-за способности бурого жира сжигать калории ученые ищут способы использовать его силу для борьбы с ожирением.Вот пять интересных фактов по этой горячей теме.
1. Коричневый жир активируется от холода.
Согласно исследованию 2014 года, проведенному исследователями Национального института здравоохранения и опубликованному в журнале Diabetes, пребывание на холоде делает ваш бурый жир более активным и может даже вызвать рост новых клеток коричневого жира. «Это помогает нам комфортно поддерживать температуру тела», — сказала Барбара Кэннон, профессор физиологии Института Веннера-Гренна в Стокгольме и президент Шведской королевской академии наук.«Млекопитающие и птицы [поддерживают] более или менее постоянную температуру тела».
Коричневый жир помогает младенцам, у которых еще нет способности дрожать, оставаться в тепле. У взрослых, подвергающихся воздействию низких температур, бурый жир может служить «внутренней нагревательной рубашкой», чтобы согревать кровь, когда она течет обратно к сердцу и мозгу от наших холодных конечностей, Гарольд Сакс из VA Greater Los Angeles Healthcare System и Майкл Саймондс из Ноттингемского университета в Англии предложил в статью 2013 года.
2. Встречается в странных местах.
Коричневый жир находится в непредсказуемых частях тела. «Мы знаем, где можно найти бурый жир, но он не всегда есть у каждого человека. Есть область на шее и плечах, и именно там вы обычно его находите, но не у всех», — сказал Аарон Сайпесс. , руководитель отделения диабета, эндокринологии и ожирения Национального института диабета и болезней органов пищеварения и почек, а также член исследовательской группы, которая в 2009 году обнаружила бурый жир у взрослых.[Готовы к школе медицины? Проверьте свое тело сообразительностью]
В недавнем исследовании Сайпесс и его коллеги также обнаружили бурый жир в груди и позвоночнике у группы здоровых молодых людей. «Он находится во многих интересных местах брюшной полости», — сказала Сайпесс.
3. У вас хоть немного бурого жира.
Это есть у всех. «Наверное, у каждого есть несколько клеток бурого жира, даже если вы не можете увидеть его с помощью ПЭТ / КТ», — сказала Сайпесс Live Science. «Мы уверены, что вы можете их вырастить.Мы, вероятно, сможем вырастить его у кого угодно ».
4. Трудно найти.
Коричневый жир бывает трудно найти и изучить. Это потому, что коричневые и белые жировые клетки часто смешиваются вместе в жировой ткани, Сайпесс сказал. Обнаружение коричневых жировых клеток требует выполнения компьютерной томографии, чтобы показать, где находится жир, в сочетании с сканированием ПЭТ (которое требует введения людям радиоактивной глюкозы) для выявления наиболее метаболически активных клеток. Сайпесс и другие работают над поиском менее инвазивных, и менее дорогие способы определить коричневый жир и измерить его активность.
5. Когда-нибудь вы сможете принять таблетку, чтобы активировать свой бурый жир.
Препарат, который лечит людей с гиперактивным мочевым пузырем, может повысить активность бурого жира , согласно результатам, которые Сайпесс и его коллеги сообщили в январе 2015 года в журнале Cell. Лекарство, называемое мирабегроном, стимулирует рецепторы, называемые бета-3-рецепторами, которые заставляют гладкие мышцы — например, в мочевом пузыре — расслабляться. По словам исследователей, эти рецепторы также обнаружены как на коричневых, так и на белых жировых клетках.
Лекарства, которые вызывают бурый жир, могут быть полезны для лечения людей с жировой болезнью печени, накоплением жировых клеток в печени, которым может подвергнуться до 25 процентов людей в Соединенных Штатах, сказал Сайпесс.
Следите за Live Science @livescience, Facebook и Google+. Первоначально опубликовано на Live Science.
Что это такое, ожирение у новорожденных
Коричневая жировая ткань или бурый жир — это один из двух типов жира, который есть у людей и других млекопитающих.Его основная функция — превращать пищу в тепло тела. Иногда его называют «хорошим» жиром.
Новорожденные люди и спящие млекопитающие имеют высокий уровень бурого жира. Другой тип жира — белый или желтый жир.
Многое остается неизвестным о буром жире. Ученые только начинают понимать, что делает бурый жир. Если они смогут выяснить, как белый жир превращается в бурый, это может привести к лечению ожирения.
Белые адипоциты или белые жировые клетки имеют одну липидную каплю, но коричневые адипоциты содержат много маленьких липидных капель и большое количество железосодержащих митохондрий.Именно это высокое содержание железа придает коричневому жиру цвет от темно-красного до коричневого.
Коричневый жир имеет больше капилляров, чем белый жир, из-за более высокого потребления кислорода. Бурый жир также имеет множество немиелинизированных нервов, обеспечивающих симпатическую стимуляцию жировых клеток.
Липид — это еще одно название жира. Липиды — это вещества, растворяющиеся в спирте, но не в воде, например жир. Масло и воск также являются липидами. Липиды содержат кислород, водород и углерод. В них меньше кислорода, чем в углеводах.
Жир, который скапливается вокруг талии и бедер человека, относится к белому типу. Бурый жир в основном скапливается вокруг шеи.
Функции бурого жира начали выясняться совсем недавно. Основные различия между ними заключаются в следующем:
Белая жировая ткань (WAT) или белый жир — это результат накопления избыточных калорий. Когда мы потребляем слишком много калорий, организм превращает их в запас энергии в виде белого жира.
Распределение WAT влияет на метаболический риск.Большое количество белого жира вокруг брюшной полости связано с более высоким риском метаболических заболеваний, тогда как жир на бедрах и бедрах — нет.
Коричневая жировая ткань (BAT) или бурый жир выделяет тепло за счет сжигания калорий. В холодную погоду липидные запасы бурого жира истощаются, и его цвет становится темнее.
У людей и млекопитающих с более высоким уровнем бурого жира требуется больше времени, чтобы начать дрожать от холода, чем у людей с более низким уровнем. Новорожденные не дрожат от холода, потому что уровень коричневой жировой ткани в них выше, чем у людей старшего возраста.
Эксперименты показали, что добавление коричневого жира к мышам увеличивает скорость, с которой они сжигают энергию, уменьшает количество жира на их теле и защищает их от ожирения, вызванного диетой.
У новорожденных доля бурого жира выше, чем у взрослых, и с возрастом эта доля постепенно снижается.
Коричневый жир можно обнаружить у взрослых с помощью позитронно-эмиссионной томографии (ПЭТ). Это легче обнаружить, когда человек подвергся воздействию низких температур.Больше всего бурого жира можно найти в нижней части шеи взрослого человека и в области над ключицей.
У человека с избыточным весом пропорционально меньше коричневого жира, чем у человека без избыточного веса. Бурый жир может играть ключевую роль в поддержании стройности человека.
У новорожденных около 5 процентов веса тела составляет бурый жир. Обычно он располагается в верхней половине позвоночника и ближе к плечам.
Коричневая жировая ткань способствует выделению тепла. Он активируется, когда организму или телу требуется дополнительное тепло.Это может произойти, когда у человека начинается лихорадка или когда животное выходит из спячки. Это тепловыделение, также называемое термогенезом, также вызывается кормлением.
Функция коричневого жира у новорожденных заключается в защите их от переохлаждения, то есть снижения внутренней температуры тела. Гипотермия — серьезная проблема для недоношенных новорожденных и основная причина смерти.
У пожилых людей большая площадь поверхности, больше мускулов, пропорциональная меньшая площадь головы, способность дрожать и двигаться из холодных мест.У новорожденных этого нет. Высокий уровень бурого жира у новорожденных обеспечивает альтернативный способ регулирования течки.
Учитывая, что ожирение в настоящее время находится на высоком уровне, эксперты ищут способы похудеть, сократив потребление пищи или сжигая больше энергии.
Один из способов сжигания энергии — упражнения, но НИМ также способствует использованию энергии. Рассеивая энергию в виде тепла, он может противодействовать увеличению веса.
Эксперты говорят, что они еще не знают, как люди могут увеличить содержание коричневого жира, но есть некоторые мысли, что, если они смогут узнать, как превратить больше белого жира в бурый жир, это может помочь людям похудеть или предотвратить дополнительный вес. прирост.
Однако остается неизвестным, возможно ли это или полезно.
Исследование, проведенное учеными из Университета Шербрука, Канада, показало, что добровольцы с более высоким уровнем коричневого жира начинали дрожать при более низких температурах по сравнению с добровольцами с более низким уровнем.
Кроме того, когда бурые жировые клетки были активными, добровольцы сжигали дополнительные 250 калорий, что в 1,8 раза увеличивало скорость сжигания калорий.
Исследователи также обнаружили, что у худых людей бурого жира больше, чем у людей с ожирением, но они пришли к выводу, что еще слишком рано делать какие-либо выводы о потенциальных преимуществах бурого жира.
Был установлен ряд путей, которые можно использовать для разработки методов лечения ожирения. В декабре 2016 года исследователи объявили, что они обнаружили сигнальный путь, который может запустить процесс превращения белых жировых клеток в коричневые жировые клетки, что повысит их вероятность сжигания жира.
Однако остается еще много проблем. Например, даже если ученые смогут решить, как превратить белый жир в коричневый, как его можно активировать, чтобы сжигать больше энергии?
Другая проблема заключается в том, что даже если можно увеличить потребление коричневого жира для увеличения потребления калорий, человеческий организм все равно сможет компенсировать это увеличением голода, что приведет к более высокому потреблению калорий с пищей.
Это исследование все еще находится на ранней стадии, и пройдет много времени, прежде чем подобные выводы смогут быть применены на практике.
Что такое коричневый жир? Может ли это помочь вашему телу похудеть?
Если вы относитесь к миллионам американцев, которые пытаются стать здоровее и сбросить лишние килограммы, вам, вероятно, не интересно, лучше ли один тип жира по сравнению с другим. Но многие исследования показывают, что бурый жир в вашем теле может быть секретным оружием для похудения.
Коричневый жир, также называемый коричневой жировой тканью, — это особый вид телесного жира, который помогает выделять тепло при простуде. Вот почему обычно не замерзаешь насмерть, играя в снег или гуляя по ледяному ветру.
Особенностью бурого жира является то, что он содержит намного больше митохондрий, чем белый жир. Эти митохондрии являются «двигателями» бурого жира, которые сжигают калории для производства тепла. Многочисленные исследования показали, что воздействие холода увеличивает количество коричневого жира, присутствующего в организме, тем самым потенциально увеличивая количество сжигаемых телом калорий.
Может ли бурый жир помочь похудеть?
Коричневый жир вызвал большой интерес у исследователей, потому что, похоже, он использует обычный телесный жир в качестве топлива. Это особенно верно, если человек занимается физической активностью, потому что исследования показывают, что упражнения стимулируют гормоны, которые активируют бурый жир, чтобы творить чудеса.
Хотя исследования продолжаются, и нам все еще нужно больше понимания того, как бурый жир активируется для сжигания калорий, ученые надеются. Возможно, в будущем использование способности бурого жира сжигать калории, а также разработка лекарств, способствующих образованию в организме большего количества коричневого жира, станут многообещающими вариантами новых, инновационных методов лечения потери веса.
Но жир есть жир, правда?
Не совсем так. У большинства из нас в теле есть как белый, так и коричневый жир. Проще говоря, белый жир сохраняет энергию и калории, а коричневый жир сжигает энергию и калории.
Поскольку бурый жир сжигает калории для выделения тепла, его часто называют «хорошим» жиром. У младенцев много коричневого жира, но уровень бурого жира снижается по мере того, как мы становимся взрослыми. Взрослые, у которых относительно больше коричневого жира, как правило, моложе, стройнее и имеют нормальный уровень сахара в крови.
Но белый жир — это еще не все. Как уже упоминалось, он накапливает необходимые нам калории, помогает защитить наши внутренние органы, обеспечивая подушку, и (как и бурый жир) выделяет полезные гормоны (подробнее об этом ниже). Но избыток белого жира, особенно в области живота, может вызвать проблемы со здоровьем, которые приводят к повышенному риску сердечных заболеваний, гипертонии, диабета и других заболеваний.
Гормоны и жиры
И белый, и коричневый жир не просто хранят калории и высвобождают энергию, они играют важную роль в эндокринной функции, производя определенные гормоны, которые помогают регулировать глюкозу, холестерин и обмен веществ.
В недавнем прошлом было проведено множество исследований (в основном на мышах) и еще больше (в том числе на людях), в которых изучаются несколько типов гормонов, которые секретируются жировыми клетками или тесно с ними взаимодействуют, особенно бурый жир. Многие из этих гормонов играют ключевую роль в поддержании здоровья или вызывают заболевания. Вот лишь некоторые из исследований.
- В исследовании мышей с патологическим ожирением, проведенном в середине 1990-х годов, исследователи обнаружили, что у мышей не было гормона лептина, который секретируется жировыми клетками.Без лептина, регулирующего аппетит, животные всегда голодали и вырастали почти в два раза больше, чем контрольные мыши.
- Исследование , 2012 г., показало, что гормоны, вырабатываемые сердцем, называемые сердечными натрийуретическими пептидами, заставляют обычных накапливающих энергию белых жировых клеток превращаться у мышей в сжигающий энергию бурый жир. Когда мышей помещали в холодную среду, они производили больше сердечного гормона, который включал бурый жир, заставляя его сжигать больше калорий.
- Исследование , проведенное в 2016 году , показало, что упражнения могут помочь в контроле веса и предотвратить диабет, улучшая способность жировых клеток сжигать калории за счет повышения уровня гормона, называемого иризином, который вырабатывается во время упражнений.Исследования показывают, что ирисин может помочь превратить обычную белую жировую ткань в более метаболически активный бурый жир; ирисин помогает белому жиру имитировать положительный эффект бурого жира.
- В 2018 году исследователи из Германии и Финляндии обнаружили , что бурый жир взаимодействует с гормоном кишечника, называемым секретином, который сообщает мозгу, что тело насыщено во время еды, что помогает контролировать потребление пищи. Обычно, когда бурый жир и секретин работают вместе, мозг перестает чувствовать голод.
Если текущие исследования покажут такие же результаты на людях, жировая ткань и гормоны могут стать очень важным ключом к эффективному снижению веса.
Известно ли нам, как активировать бурый жир у человека?
Хотя многочисленные исследования показали, что воздействие холода увеличивает количество бурого жира , присутствующего в организме, что приводит к сжиганию большего количества калорий, до сих пор неясно, сколько холода нужно выдержать человеку, чтобы увеличить его или уровень полезного коричневого жира в ее организме.
Может пройти еще десять лет, прежде чем появятся конкретные исследования, показывающие, как увеличить и активировать наши запасы коричневого жира при простуде, но тем временем исследователи уже знают одно: упражнения , скорее всего, являются ключевыми.Если вы хотите запустить свою собственную машину для сжигания коричневых калорий, начните с выполнения программы упражнений .
Подпишитесь на блог INTEGRIS Health On Your Health
Подпишитесь на регулярные электронные письма с полезной и интересной информацией о здоровье и благополучии в Оклахоме от врачей и экспертов в области здравоохранения INTEGRIS Health.
Раскрывая секреты коричневого жира
В последние годы бурый жир привлек внимание как так называемый полезный жир, который может защитить от ожирения и связанных с ним рисков для здоровья, таких как сердечно-сосудистые заболевания и диабет.Два отдельных крупных исследования, одно из которых проведено доктором философии Лянгё Жуй. и один, сделанный Лин Ци, доктором философии, оба из отдела молекулярной и интегративной физиологии, помогают объяснить свойства бурого жира.
Коричневый жир и мозг
Расположенный в небольших карманах по всему телу, большинство млекопитающих используют бурый жир (и его близкий родственник бежевый жир), чтобы оставаться в тепле. «У мышей и людей, если у вас больше коричневого или бежевого жира, вы в большей степени защищены от метаболических заболеваний», — говорит Руи, специалист Louis G.Д’Альси — профессор физиологии Медицинской школы Университета Мэн, лаборатория которого изучает молекулярные и физиологические механизмы ожирения, диабета и жировой болезни печени. В новом исследовании, опубликованном в Nature Communications , Руи, первый автор Линь Цзян, доктор философии, и их коллеги раскрывают путь, по которому гормон лептин способствует снижению веса.
Лептин регулирует массу тела, контролируя аппетит и расход энергии, но как именно, остается загадкой. По словам Руи, известно, что лептин активирует коричневый и бежевый жир.Новое исследование раскрывает молекулярный ускоритель действия лептина в головном мозге под названием Sh3b1. Его команда обнаружила, что Sh3b1 в гипоталамусе, важной области мозга, контролирующей температуру тела и голод среди других функций, способствует стимуляции симпатической нервной системы. Симпатическая нервная система посылает сигналы коричневому и бежевому жиру, чтобы активировать его, таким образом поддерживая массу тела и метаболизм.
Команда продемонстрировала это доказательство принципа, создав две модели мыши.Мыши, у которых отсутствовал ген Sh3b1 в нейронах рецептора лептина, «обладали невероятно сниженным симпатическим влечением к коричневому и бежевому жиру и сниженной способностью стимулировать расход энергии», — говорит Руи. Это снижает способность бурого жира превращаться в тепло, что снижает внутреннюю температуру тела мышей. Более того, у мышей развились ожирение, инсулинорезистентность и ожирение печени. Напротив, мыши с дополнительной экспрессией Sh3b1 в мозгу были защищены от ожирения.
Понравились подкасты? Добавьте Michigan Medicine News Break на свое устройство с поддержкой Alexa или подпишитесь на обновления на iTunes , Google Play и Stitcher .
«Никто не знал, что Sh3b1 в мозге контролирует симпатическую нервную систему или необходим лептину для активации бурого жира для увеличения расхода энергии», — отмечает Руи.Что касается того, как это открытие может быть применено к людям, он говорит, что в конечном итоге есть надежда найти способ увеличить экспрессию Sh3b1 или его способность усиливать передачу сигналов лептина и сжигание жира.
Среди других авторов UM, внесших свой вклад в эту статью: Хаоран Су, Сяоинь Ву, Хонг Шен, Мин-Хён Ким, Юань Ли, Мартин Г. Майерс-младший и Чунг Оуян.
Коричневый жир и клетка
Коричневый жир приобретает свой цвет из-за большого количества железосодержащих митохондрий, в отличие от стандартного белого жира, связанного с ожирением.Команда под руководством Ци, профессора молекулярной и интегративной физиологии и внутренней медицины в Медицинской школе UM, изучает, как митохондрии, энергетическая установка клетки и другая клеточная структура, называемая эндоплазматическим ретикулумом (ER), участвует в производство белков и липидов, взаимодействующих внутри бурых жировых клеток.
В частности, они изучили роль белкового комплекса, участвующего в процессе, называемом ER-ассоциированной деградацией белка, или ERAD. Проще говоря, ERAD — это процесс удаления и разрушения неправильно свернутых белков, как вывоз мусора из ER.
«Все думали, что ERAD — это всего лишь часть общего клеточного ответа, когда клетки подвергаются стрессу ER», — говорит Ци. «За последние шесть лет мы показали, что он играет фундаментальную роль в здоровье и болезнях».
В новом исследовании, опубликованном в журнале Science , Ци вместе с первыми авторами Чжансен Чжоу, доктор философии, Маурисио Торрес, доктор философии, и их коллеги демонстрируют, как белковый комплекс ERAD влияет на правильную функцию митохондрий.
Как правило, ER и митохондрии постоянно взаимодействуют в точках соприкосновения, называемых мембранами, ассоциированными с митохондриями.Эти точки контакта отмечают области, в которых митохондрии разделяются для производства новых митохондрий и для обмена другими молекулами, такими как липиды и кальций. ER образует канальцы, которые окружают митохондрии, чтобы подготовить их к делению.
Используя современную трехмерную визуализацию, исследователи обнаружили, что происходит с митохондриями бурого жира, в которых отсутствует часть белкового комплекса ERAD, называемого Sel1L-Hrd1, при воздействии холода.
«Когда вы удаляете этот комплекс в коричневых адипоцитах, митохондрии становятся удлиненными и увеличенными», — говорит Ци.Трехмерное изображение позволило им увидеть ранее нераспознанное взаимодействие между митохондриями и ER, при этом митохондрии U-образно оборачиваются вокруг канальцев ER.
ПОДРОБНЕЕ В ЛАБОРАТОРИИ: Подпишитесь на нашу еженедельную рассылку новостей
Когда мышей помещали в холодную среду, концы внешней мембраны митохондрий загибались сами по себе, в конечном итоге сливаясь и полностью охватывая канальцы ER. В результате, по словам Ци, возникают аномально большие, деформированные, дисфункциональные митохондрии.
«Мы показали, что эти митохондрии не функционируют нормально, и мыши становятся чувствительными к холоду, температура их тела падает очень быстро», — говорит Ци. Другими словами, без этого белкового комплекса ERAD бурый жир не используется для выработки тепла. Под микроскопом этот дисфункциональный бурый жир имел более крупные капли липидов, чем бурый жир мышей с неповрежденным белковым комплексом.
«Это в высшей степени неожиданно. Результаты здесь фундаментально меняют наше понимание ER-митохондриальной коммуникации и дополнительно демонстрируют важность комплекса деградации ER в клеточной биологии.”
В этот документ также включены материалы следующих авторов UM: Кристофера Халбрука, Франсуазы Ван ден Берг, Рэйчел Б. Райнерт, Сивен Ван, Иньинг Луо, Аллена Х. Хантера, Томаса Х. Сандерсона, Аарона Тейлора, Костаса А. Лиссиотиса, Джун Ву и Дэниел А. Бирд.
Цитированных статей:
«Нейрон Sh3b1, экспрессирующий рецептор лептина, поддерживает симпатическую нервную систему и защищает от ожирения и метаболических заболеваний», Nature Communications , DOI: 10.1038 / s41467-020-15328-3
«Деградация, связанная с эндоплазматическим ретикулумом, регулирует митохондриальную динамику в коричневых адипоцитах», Science , DOI: 10.1126 / science.aay2494
Ученые открыли переключатель, который заставляет человека сжигать бурый жир энергии — ScienceDaily
Международная исследовательская группа обнаружила, как активировать бурый жир у людей, что может привести к новым методам лечения диабета 2 типа и ожирения. Сегодня в журнале Cell Metabolism опубликованы результаты сотрудничества между Центром исследований и университетских госпиталей в Шербруке (CRCHUS) и Центром фундаментальных метаболических исследований Novo Nordisk Foundation (CBMR) при Университете Копенгагена.
Коричневый жир сжигает энергию и выделяет тепло — процесс, называемый термогенезом — после того, как он активирован холодной температурой или химическими сигналами. У людей есть небольшие отложения бурого жира, и ученые давно выдвинули гипотезу, что поиск альтернативных способов фармакологической активации жира может помочь улучшить метаболизм.
Ученые обнаружили, что бета2-адренорецепторы (b2-AR) в коричневых жировых клетках ответственны за стимуляцию термогенеза. По словам доктораДенис Блондин из CRCHUS, открытие может объяснить, почему большинство клинических испытаний, в которых пытались заставить BAT сжигать энергию, оказались неэффективными.
«Мы показываем, что, возможно, мы все время стремились не к той цели. В отличие от грызунов, человеческая летучая мышь активируется за счет стимуляции бета2-адренорецептора, того же рецептора, который отвечает за высвобождение жира из нашей белой жировой ткани. »
Раскрытие терапевтического потенциала бурого жира
По словам доцента Камиллы Шеле из CBMR, это открытие имеет четкое терапевтическое применение.«Активация бурого жира сжигает калории, улучшает чувствительность к инсулину и даже влияет на регуляцию аппетита. Наши данные раскрывают ранее неизвестный ключ к разблокировке этих функций у людей, что потенциально может принести большую пользу людям, живущим с ожирением или диабетом 2 типа».
Осенью начнется вторая фаза исследований, в ходе которых будет предпринята попытка подтвердить открытие путем активации бурого жира лекарствами, нацеленными на b2-AR, — объясняет профессор Андре Карпентье из CRCHUS:
«Нашим следующим шагом будет использование препарата, который специально активирует эту мишень для бурого жира и определит, насколько он может быть полезен для сжигания жира и калорий у людей.Как только это будет сделано, начнутся исследования пациентов с диабетом 2 типа, чтобы определить, может ли этот подход быть полезным для улучшения метаболического контроля над болезнью ».
История Источник:
Материалы предоставлены Копенгагенским университетом Факультет здравоохранения и медицинских наук . Примечание. Содержимое можно редактировать по стилю и длине.
границ | Пищевые ингредиенты, участвующие в превращении белой жировой ткани в коричневую и в сжигании калорий
Введение
Ожирение определяется как аномальное накопление жира в организме из-за хронических периодов дисбаланса между потреблением и расходом энергии.Серьезную озабоченность вызывает высокий риск сопутствующей группы сопутствующих заболеваний, таких как сердечно-сосудистые заболевания, метаболический синдром и некоторые формы рака (Andolfi and Fisichella, 2018).
Управление массой тела в основном основано на изменении образа жизни и регулировании усвоения пищи. С другой стороны, подходы, направленные на повышение ЭЭ, представляют собой альтернативный инструмент для борьбы с ожирением и связанными с ним кардиометаболическими расстройствами (Khera et al., 2016).
В дополнение к хорошо известным WAT, хранящим липиды и претерпевающим патологические структурные и функциональные изменения во время ожирения, млекопитающие, включая взрослых людей, также оснащены BAT, наделенными термогенной способностью, называемой адаптивной или NST (Virtanen et al., 2009; Розенвальд и Вольфрам, 2014). БАТ представляет собой метаболически активную ткань, богатую митохондриями, содержащими UCP1, который опосредует разъединение транспорта электронов, что приводит к снижению выработки АТФ из аденозиндифосфата (АДФ) с последующим выделением тепла (Bartelt and Heeren, 2014; Rossato et al., 2014). Сегодня индукция термогенеза BAT представляет собой многообещающую защитную стратегию для борьбы с ожирением у людей за счет увеличения EE (Rosenwald and Wolfrum, 2014).
Однако NST не ограничивается только классическими коричневыми адипоцитами, поскольку определенные стимуляции, такие как воздействие холода или активаторы ADRB3, могут вызывать появление так называемых бежевых или коричневых адипоцитов в депо WAT в процессе, называемом «потемнение WAT» (Kiefer, 2017 ).Основные физиологические, биохимические и морфологические характеристики каждого подтипа жировой ткани кратко представлены на Рисунке 1.
Рисунок 1. Обзор основных характеристик белых, коричневых и бежевых адипоцитов.
Исследования последних десятилетий предоставили доказательства в поддержку роли биоактивных пищевых компонентов в профилактике и / или лечении ожирения и связанных с ним метаболических нарушений (Martínez-González et al., 2015; Amiot et al., 2016). Текущий мини-обзор направлен на обобщение последних результатов, касающихся активации BAT или потемнения WAT, вызванного определенными диетическими компонентами, включая капсаицин, ресвератрол, куркумин, зеленый чай, ментол и жирные кислоты омега-3, полученные из рыбы.
На рисунках 2 и 3 мы суммировали основные физиологические механизмы, участвующие в продвижении BAT через эти пищевые соединения.
Рис. 2. Пищевые компоненты, стимулирующие расход энергии, и механизмы их действия, участвующие в активации BAT или в индукции потемнения WAT.BAT — коричневая жировая ткань; WAT, белая жировая ткань; TRPM8, временный рецепторный потенциал катионного канала меластатина 8; UCP1, разобщающий белок 1; TRPV1, временный рецепторный потенциал ваниллоида 1; SNA, активность симпатического нерва; AMPK 5 ‘, протеинкиназа, активируемая аденозинмонофосфатом, SIRT1, сиртуин-1; PGC-1α, гамма-коактиватор 1-альфа рецептора, активируемого пролифератором пероксисом; COMT, катехол-O-метилтрансфераза цАМФ; циклический аденозинмонофосфат; ПДЭ, фосфодиэстеразы; ПНЖК, полиненасыщенные жирные кислоты.
Рисунок 3. Краткое изложение механизмов, участвующих в стимуляции коричневого адипогенеза, митохондриального биогенеза и расходования энергии некоторыми молекулами пищи. (a) Прямая и / или непрямая (через AMPK) активация SIRT1 вызывает деацетилирование и взаимодействие ключевых факторов транскрипции, способствующих коричневому и бежевому адипогенезу, таких как PPARα / γ и PRDM16. Комплекс PPAR / PRDM16 также способен связывать и активировать PGC1α, еще один кофактор, специфически экспрессируемый в коричневых и бежевых адипоцитах, который стимулирует транскрипцию нескольких генов, участвующих в термогенезе и митохондриальном биогенезе.Точно так же AMPK также может напрямую усиливать активность PGC1α путем фосфорилирования, тем самым увеличивая биогенез митохондрий. (b) Активация TRPM8 в коричневых адипоцитах усиливает экспрессию термогенных генов через Ca 2+ -зависимый сигнальный путь PKA. (c) Активация рецепторов TRPV1 в ЖКТ и последующая стимуляция афферентных путей блуждающего нерва приводит к активации нейронов в вентромедиальном гипоталамусе. Этот механизм действия вызывает независимый от холода адренергический ответ, который опосредует коричневый адипогенез.Адренергической стимуляции коричневых адипоцитов также может способствовать уменьшение деградации (d), цАМФ и (e), норэпинефрина посредством прямого ингибирования активности PDE и COMT, соответственно. TRPM8, временный рецепторный потенциал катионного канала меластатина 8; UCP1, разобщающий белок 1; TRPV1, временный рецепторный потенциал ваниллоида 1; SNA, активность симпатического нерва; AMPK, аденозинмонофосфат-активированная протеинкиназа, SIRT1, сиртуин-1; PGC-1α, гамма-коактиватор 1-альфа рецептора, активируемого пролифератором пероксисом; COMT, катехол-O-метилтрансфераза цАМФ; циклический аденозинмонофосфат; ПДЭ, фосфодиэстеразы; ПНЖК, полиненасыщенные жирные кислоты; Ас, ацетильная группа; цАМФ, циклический аденозинмонофосфат; ЭЭ — затраты энергии; PPARα / γ рецептор альфа / гамма, активируемый пролифератором пероксисом; PKA, протеинкиназа A, PRDM16; PR-домен, содержащий 16, (+), стимуляция; (-), торможение; ↑, увеличить.
Капсаицин и капсиноиды
Капсаицин (8-метил-N-ваниллил-6-ноненамид) является активным компонентом острого перца и принадлежит к роду растений стручкового перца. Этот алкалоид отвечает за остроту и жжение перца чили (Thiele et al., 2008). Капсиноиды, которые включают дигидрокапсиат, нордигидрокапсиат и капсиат, имеют ту же химическую структуру, что и капсаицин. Это активные ингредиенты, содержащиеся в не остром виде красного перца чили (Kobata et al., 1999). И капсаицин, и капсиноиды вызвали огромный интерес из-за их роли в усилении окисления жиров и ЭЭ (Ludy et al., 2012). Пероральное лечение капсиноидами (6 мг / кг в течение 12 недель) у пациентов с избыточным весом или ожирением было связано с потерей брюшного жира и увеличением окисления жиров по сравнению с группой плацебо (Snitker et al., 2009). Кроме того, Lejeune et al. (2003) показали, что лечение капсаицином (135 мг в день) у субъектов с избыточным весом индуцировало повышение ЭЭ в состоянии покоя. В другом рандомизированном плацебо-контролируемом исследовании капсиноиды (10 мг / кг в день) были способны увеличивать ЭЭ, VO 2 и усиливать сжигание жира (Inoue et al., 2007). Было показано, что термогенные эффекты и эффекты против ожирения капсаицина и капсиноидов опосредованы, по крайней мере частично, стимулированием активности BAT. Йонеширо и др. (2012) оценили краткосрочное влияние пищевых добавок капсиноидов (9 мг) на активность ЭЭ и НДТ у здоровых мужчин. Активность BAT оценивали с помощью [ 18 F] — FDG-PET. Авторы продемонстрировали значительное увеличение ЭЭ (на 15,2 кДж / ч) у субъектов с активными НДТ. С другой стороны, лишь небольшое увеличение EE (на 1.7 кДж / ч) после перорального приема капсиноидов наблюдалась в группе BAT-отрицательных (Yoneshiro et al., 2012).
Внутрижелудочное введение аналога капсаицина крысам индуцировало увеличение SNA BAT посредством активации каналов TRPV1, экспрессируемых вдоль желудочно-кишечного тракта (Ono et al., 2011). Эти результаты были подтверждены другим исследованием, которое показало TRPV1-зависимое повышение температуры толстой кишки и внутрилопаточного BAT после введения капсиноидов в тощую кишку у мышей.Этот эффект подавлялся внешней денервацией сегмента тощей кишки, что указывает на роль желудочно-кишечного блуждающего нерва в опосредованном капсиноидами термогенезе (Kawabata et al., 2009). В недавнем отчете было показано, что сочетание умеренного воздействия холода и капсиноидов у мышей C57BL / 6 способствует развитию как коричневых, так и бежевых адипоцитов в паховой WAT, что указывает на центрально-опосредованный эффект капсиноидов. Капсиноиды взаимодействуют с рецепторами TRPV1 в кишечнике, которые, в свою очередь, стимулируют афферентные пути блуждающего нерва, что приводит к активации нейронов вентромедиального гипоталамуса.Этот механизм действия вызывает независимый от холода адренергический ответ в WAT, что приводит к повышению уровня и стабильности PRDM16. Следовательно, два β-адренергических пути синергетически опосредуют биогенез бежевых адипоцитов, индуцированный капсиноидами (Ohyama et al., 2016).
Более того, Baskaran et al. (2016) показали, что капсаицин запускает потемнение WAT, способствуя экспрессии SIRT1, UCP1, BMP8B и PPARγ, PGC-1α в белых адипоцитах. SIRT1 представляет собой NAD + -зависимую деацетилазу нескольких факторов транскрипции, включая PGC-1α, следовательно, модулирующую окислительный метаболизм митохондрий (Cantó and Auwerx, 2009).В белых адипоцитах SIRT1 также индуцирует деацетилирование и взаимодействие PPARγ и PR-доманина, содержащего 16 (PRDM16), и тем самым регулирует ключевые факторы, участвующие в развитии BAT (Qiang et al., 2012). Несмотря на то, что прямой механизм, с помощью которого капсаицин и его производные активируют BAT, был продемонстрирован на животных моделях, на людях еще предстоит проделать большую работу.
Ресвератрол
Ресвератрол (транс-3,5,4′-тригидроксистильбен) — это природный полифенол, который привлек множество исследовательских интересов, главным образом в области лечения ожирения (Kim and Park, 2011).Это соединение сначала было обнаружено в корнях белого морозника, а затем в шелковице, красном вине, винограде и арахисе (Burns et al., 2002).
Было показано, что введение ресвератрола (400 мг / кг / день в течение 10 недель) мышам, получавшим HFD, снижает массу висцеральных жировых подушечек и подавляет адипогенез в эпидидимальных белых адипоцитах (Kim et al., 2011). Кроме того, Rayalam et al. (2008) предоставили дополнительные доказательства ингибирующего действия ресвератрола на адипогенез. Ресвератрол снижает жизнеспособность адипоцитов и подавляет экспрессию адипогенных факторов, таких как SREBP-1c, LPL, C / EBP-α, HSL и PPARγ.Кроме того, ресвератрол активировал гены, участвующие в митохондриальном биогенезе, такие как митофузин (Mfn) -2 и UCP1 (Rayalam et al., 2008).
Было показано, что низкие концентрации ресвератрола способствуют экспрессии коричневых адипогенных маркеров, включая UCP1, PRDM16, PGC1α и CIDEA, в стромальных сосудистых клетках, выделенных из пахового WAT мышей, что предполагает основную роль ресвератрола в потемнении WAT (Wang et al., 2015a ). Подобные результаты наблюдались в стромальных первичных сосудистых клетках, отделенных от межлопаточной BAT после лечения ресвератролом in vitro (Wang et al., 2017). Было высказано предположение, что потемнение ресвератрола опосредуется активацией 5′-аденозинмонофосфат-активируемой протеинкиназы (AMPK) α1, поскольку эти изменения отсутствовали в клетках, лишенных AMPKα1 (Wang et al., 2015a, 2017).
У мышей C57BL / 6J прием HFD с добавкой ресвератрола в течение 15 недель приводил к усилению адаптивного термогенеза в ответ на внешнее охлаждение. Более того, BAT мышей, получавших ресвератол, показали более крупные структуры митохондрий и содержание ДНК, значительное увеличение экспрессии генов путей, характерных для энергетического гомеостаза, включая PPARα, включающий β-окисление жирных кислот и UCP1.Эти эффекты сочетались с повышенной экспрессией гена SIRT1, что впоследствии усиливало активность PGC-1α в коричневых адипоцитах (Lagouge et al., 2006). В этом отчете авт. Предположили потенциальный вклад SIRT1-обеспечиваемой деациелляции PGC-1α в активацию BAT (Lagouge et al., 2006; Cantó and Auwerx, 2009). Аналогичным образом Andrade et al. (2014) показали, что кормление мышей стандартной диетой плюс ресвератрол индуцировало экспрессию генов SIRT1 и UCP1 в BAT. Кроме того, эффекты ресвератрола включают повышенную экспрессию других генов, таких как PTEN, который способствует EE, и Bmp7, который, как известно, играет центральную роль в развитии и дифференцировке бурого жира (Tseng et al., 2008).
Взятые вместе, эти результаты предполагают, что ресвератрол играет решающую роль в формировании и активации коричневых адипоцитов за счет усиления сигнального пути AMPK – SIRT1 – PGC-1α. Было высказано предположение, что ресвератрол может оказывать прямое стимулирующее действие на SIRT1 (Price et al., 2012), тогда как другие данные указывают на косвенную активацию через AMP (Wang et al., 2015a). В связи с этим сообщалось, что ресвератрол может напрямую ингибировать циклические АМФ (цАМФ) -специфичные PDE в скелетных мышцах и WAT мышей, что приводит к повышенным внутриклеточным уровням цАМФ.Активация EPAC, эффектора цАМФ, приводит к увеличению концентрации внутриклеточного кальция (Ca 2+ ), который активирует путь AMPK и впоследствии увеличивает активность SIRT1. Однако влияние этого ресвератрол-опосредованного сигнального пути цАМФ на коричневый адипогенез еще предстоит выяснить (Park et al., 2012). В отличие от исследований на животных, отсутствуют доказательства того, может ли ресвератрол влиять на потемнение WAT или активацию BAT у людей.
Куркумин
Куркумин, также называемый диферулоилметаном, представляет собой гидрофобный полифенол желтого цвета, содержащийся в экстрактах корней куркумы (растения из семейства имбирных).Куркумин обычно используется в качестве специи в кулинарии и признан за его потенциальную ценность в качестве средства против ожирения (Mantzorou et al., 2018). В недавнем клиническом исследовании оценивалась безопасность и эффективность 30-дневного лечения куркумином в сочетании с фосфатидилсерином у субъектов с избыточным весом, теряющих вес с помощью диеты и изменения образа жизни. В этом исследовании введение куркумина увеличивало потерю веса, увеличивало потерю жировой массы и вызывало уменьшение талии и окружности бедер (Di Pierro et al., 2015).
Wang et al. (2015b) продемонстрировали, что внутрижелудочное введение куркумина (50 или 100 мг / кг в день) мышам в течение 50 дней вызывает снижение жировой массы и веса тела без изменения приема пищи. После провокации холодом (воздействие 4 ° C) у мышей, получавших куркумин, наблюдалось повышение адаптивного термогенеза, концентрации норадреналина в крови и экспрессии характерных генов BAT (например, ADRB3, CIDEA, PRDM 16, PGC-1α и UCP1) в паховая WAT (Wang et al., 2015b).В другом исследовании Lone et al. (2016) добавили доказательства влияния диетического куркумина (10–20 мкМ / день) на индукцию бежевого фенотипа в белых адипоцитах крыс. Эти изменения сопровождались повышенной экспрессией генов маркеров бурого жира, таких как FGF21, Tbx1, TMEM26 и CIDEA, и некоторых белков-маркеров коричневых клеток, включая PRDM16, UCP1 и PGC-1α, в зависимости от дозы. Было показано, что эти вызванные куркумином эффекты потемнения опосредуются активацией AMPK-пути (Lone et al., 2016).
В недавнем исследовании у мышей, получавших HFD в сочетании с куркумином, было показано увеличение EE и адаптивного термогенеза после воздействия умеренного холода. В рамках этого исследования лечение куркумином было связано с повышенной экспрессией UCP1 в BAT, возможно, с участием PPAR-зависимых и независимых механизмов (Song et al., 2018).
Общей чертой этих исследований на животных и людях было введение высоких доз куркумина. Это было оправдано низкой системной биодоступностью перорального куркумина, что также может быть причиной негарантированных положительных результатов (Pan et al., 1999; Иресон и др., 2001). В связи с этим Nishikawa et al. (2018) продемонстрировали, что введение низких доз куркумина, но имеющих более высокую биодоступность по сравнению с нативным куркумином, усиливало потемнение in vivo WAT и увеличивало EE у мышей. Эти эффекты были вызваны выработкой норэпинефрина альтернативно активированными макрофагами в WAT (Nishikawa et al., 2018).
Зеленый чай
Зеленый чай — широко потребляемый напиток, получаемый из листьев Camellia Sinensis.В нескольких сообщениях указано, что зеленый чай может вызывать потерю веса за счет повышения ЭЭ и окисления жиров у людей (Westerterp-Plantenga et al., 2006). Эти положительные эффекты, по крайней мере частично, связаны с катехинами чая, такими как EGCG, который является наиболее активным катехином зеленого чая, эпигаллокатехином и галлатом эпикатехина (Basu and Lucas, 2007). Интересно, что экстракты зеленого чая содержат значительное количество кофеина, который известен своими термогенными свойствами (Westerterp-Plantenga et al., 2006).Потребление чайных катехинов крысами, получавшими диету с нормальным содержанием жира, вызывало увеличение экспрессии BAT UCP1 и потерю массы WAT (Nomura et al., 2008). Chen et al. (2017) показали, что пероральное введение зеленого чая через желудочный зонд в течение 8 недель улучшало параметры, связанные с ожирением, и повышало экспрессию маркеров BAT (например, PPAR-γ, PRDM-16 и PGC-1α) в WAT крыс, получавших HFD-диета.
Что касается исследований на людях, Dulloo et al. (1999) продемонстрировали, что зеленый чай усиливает ЭЭ и окисление жиров.В этом исследовании введение эквивалентного количества кофеина, содержащегося в экстрактах зеленого чая, не привело к аналогичным метаболическим эффектам (Dulloo et al., 1999). Тем не менее, катехины и кофеин могут синергически опосредовать термогенез BAT, индуцированный адренергическими рецепторами, действуя в различных контрольных точках оси норадреналин-цАМФ. Было высказано предположение, что катехины зеленого чая могут способствовать SNA, уменьшая деградацию норадреналина за счет прямого ингибирования COMT. Интересно, что кофеин может синергически продлевать действие норадреналина путем прямого ингибирования активности PDE (Dulloo et al., 1999, 2000). Синергетический термогенный эффект, проявляемый EGCG и кофеином, был дополнительно подтвержден после введения инкапсулированных смесей EGCG-кофеин (Bérubé-Parent et al., 2005).
Однако роль зеленого чая в борьбе с ожирением казалась спорной в нескольких исследованиях на людях (Huang et al., 2014). Было высказано предположение, что на эти результаты могут влиять состав тела, пищевые привычки и этническая принадлежность исследуемых популяций (Huang et al., 2014). Кроме того, большинство исследований было направлено на оценку влияния катехинов зеленого чая на окисление жиров, а не на термогенез (Rains et al., 2011), поэтому необходимы дополнительные исследования для выяснения роли зеленого чая в активации и привлечении BAT у людей.
Ментол
Ментол (2-изопропил-5-метилциклогексанол), также известный как мятная камфора, представляет собой циклический монотерпеновый спирт, произведенный синтетическим путем или полученный из мяты перечной Mentha piperita (Patel et al., 2007; Pergolizzi et al., 2018). На протяжении веков ментол находил применение в медицине благодаря своим многообещающим биологическим свойствам, включая противокашлевое, противовоспалительное, противозудное, антибактериальное и обезболивающее (Patel et al., 2007). Также известно, что ментол вызывает ощущение холода, активируя рецептор TRPM8, неселективный канал, проницаемый для Ca 2+ , который обнаруживает холодовые стимулы в термосенсорной системе (McKemy et al., 2002; Bautista et al., 2007). TRPM8 также экспрессируется в значительных количествах в легких, мужской репродуктивной системе и раковых тканях, где его функция еще недостаточно изучена (Tsavaler et al., 2001; Stein et al., 2004). Недавние исследования продемонстрировали экспрессию TRPM8 на мембране коричневых и белых адипоцитов (Ma et al., 2012; Россато и др., 2014; Jiang et al., 2017).
Было показано, что длительное введение ментола мышам увеличивает экспрессию и активность UCP1 в BAT, увеличивает EE, улучшает чувствительность к инсулину и предотвращает увеличение веса, вызванное HFD. Эти эффекты, как было установлено, опосредованы активацией TRPM8 в коричневых адипоцитах с последующим Ca 2+ -зависимым фосфорилированием PKA (Ma et al., 2012). Аналогичным образом Jiang et al. (2017) сообщили, что TRPM8 также экспрессируется на культивируемых белых адипоцитах мышей, и его активация ментолом усиливает экспрессию термогенных генов (UCP1, PGC1α) через сигнальный путь PKA в белых адипоцитах.Интересно, что введение ментола защищало мышей от HFD-ожирения и увеличивало количество бежевых адипоцитов (Jiang et al., 2017).
Кроме того, активация TRPM8 in vitro ментолом в белых адипоцитах человека индуцировала коричневоподобный фенотип, стимулировала экспрессию UCP1 и термогенез адипоцитов (Rossato et al., 2014). Более того, было показано, что местное нанесение ментола на кожу активирует TRPM8 и вызывает параллельное повышение NST и температуры тела (Tajino et al., 2007; Vizin et al., 2018).
В совокупности эти данные подтверждают доказательства перспективного использования ментола как многообещающего подхода к лечению ожирения и связанных с ним сопутствующих заболеваний путем регулирования энергетического баланса и метаболического гомеостаза.
Рыбные жирные кислоты омега-3
Омега-3 ПНЖК, такие как DHA и EPA, являются основными полиненасыщенными жирами, содержащимися в добавках рыбьего жира и в жирной рыбе, такой как лосось (Anderson and Ma, 2009). Было показано, что добавление рыбьего жира увеличивает экспрессию UCP1 (Takahashi and Ide, 2000) и уровни белка в межлопаточных летучих мышах крыс (Kawada et al., 1998). Недавно было показано, что диетические n-3 ПНЖК снижают количество висцеральных WAT и увеличивают массу межлопаточных BAT у крыс (Crescenzo et al., 2017).
Было показано, что рыбий жир увеличивает экспрессию многочисленных термогенных генов в BAT, включая β3 ADRB3, PRDM16, PGC1α и PPAR в BAT (Bargut et al., 2016; Pahlavani et al., 2017). Кроме того, в паховом WAT рыбий жир оказывает потемнение за счет привлечения бежевых адипоцитов. В другом исследовании Kim et al. (2015) добавили доказательства того, что добавление рыбьего жира крысам в течение 10 недель индуцировало набор бежевых адипоцитов за счет увеличения экспрессии UCP1, PGC1α, CIDEA и PRDM16 в паховой WAT.Авторы предположили, что рыбий жир способствует коричневому адипогенезу, действуя как лиганд TRPV1 в пищеварительном тракте, который запускает через мозг β2-адренергический симпатический ответ в жировых депо.
Кроме того, Laiglesia et al. (2016) недавно показали, что EPA вызывает переключение с белых на бежевые адипоциты в подкожных адипоцитах человека у субъектов с избыточной массой тела, способствуя активации оси AMPK / SIRT1 / PGC1-. Однако, несмотря на многообещающие данные исследований на мышах, мало что известно о термогенной активности n-3 ПНЖК у людей.
Заключение
Недавнее открытие метаболически активных BAT у взрослых людей повысило надежды на разработку новых методов лечения ожирения, которые могут регулировать образование коричневого или бежевого жира. В этом обзоре мы сосредоточились на нескольких диетических молекулах, которые, как было показано, регулируют активацию BAT или выработку бежевого жира. Несмотря на многообещающие данные, полученные на животных моделях или клеточных линиях, эти результаты должны быть подтверждены на людях путем дальнейших крупных клинических испытаний с относительно длительным периодом наблюдения и с учетом таких факторов, как этническая принадлежность, генетика и образ жизни.Более того, текущие знания, полученные из клеточных культур и животных моделей, предполагают, что полифенолы, в основном куркумин и ресвератрол, оказывают термогенный эффект при добавлении в значительно повышенных дозах. Следовательно, необходимы дальнейшие исследования для определения оптимального препарата, доз, а также биодоступности и безопасности этих молекул для человека.
Наконец, было показано, что описанные выше диетические компоненты имеют общие молекулярные мишени, участвующие в индукции коричневого адипогенеза.Затем будущие исследования должны проверить гипотезу о том, могут ли комбинированные добавки также действовать синергетически для активации NST у человека посредством активации BAT и / или рекрутирования бежевой жировой ткани.
Взносы авторов
Он написал рукопись. MR вычитал рукопись и дал рекомендации по общему направлению рукописи. Все авторы критически оценили окончательную версию статьи.
Финансирование
Этот проект получил финансирование в рамках исследовательской и инновационной программы Европейского Союза Horizon 2020 в рамках Соглашения о гранте Марии Склодовской-Кюри №691061.
Сокращения
ADRB3, β3-адренорецептор; AMPK, 5’аденозинмонофосфат-активируемая протеинкиназа; АТФ, аденозинтрифосфат; BAT — коричневая жировая ткань; BMP8B, костный морфогенетический белок 8b; C / EBP-α, альфа-связывающий белок-энхансер CCAAT; цАМФ, циклический аденозинмонофосфат; CD137, член рецептора фактора некроза опухоли; CIDEA, DFFA-подобный эффектор a; COMT, катехол-O-метилтрансфераза; ССЗ, сердечно-сосудистые заболевания; DHA, докозагексаеновая кислота; ЭЭ — затраты энергии; EGCG, галлат эпигаллокатехина; EPA, эйкозапентаеновая кислота; EPAC, обменный белок, непосредственно активируемый цАМФ; FAS, рецептор смерти; ФДГ-ПЭТ [ 18 F], фтордезоксиглюкозо-позитронно-эмиссионная томография; FGF21, фактор роста фибробластов 21; HFD, диета с высоким содержанием жиров; HSL, гормоночувствительная липаза; LPL, липопротеинлипаза; Mfn2, митофузин 2; мРНК, информационная РНК; НАД +, никотинамидадениндинуклеотид; NST, термогенез без дрожи; ПДЭ, фосфодиэстеразы; PGC-1α, гамма-коактиватор 1-альфа рецептора, активируемого пролифератором пероксисом; ПКА, протеинкиназа А; PPARγ, гамма-рецептор, активируемый пролифератором пероксисом; PRDM16, PR-домен, содержащий 16; PTEN, гомолог фосфатазы и тензина; ПНЖК, полиненасыщенные жирные кислоты; SIRT1, сиртуин-1; SNA, активность симпатического нерва; SREBP-1c, белок-1c, связывающий регуляторный элемент стерола; Tbx1, фактор транскрипции T-box 1; TMEM26, трансмембранный белок 26; TRPM8, временный рецепторный потенциал катионного канала меластатина 8; TRPV1, временный рецепторный потенциал ваниллоида 1; UCP1, разобщающий белок 1; ВО 2 , потребление кислорода; WAT, белая жировая ткань.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Список литературы
Амиот, М. Дж., Рива, К., и Винет, А. (2016). Влияние диетических полифенолов на особенности метаболического синдрома у людей: систематический обзор. Obes. Ред. 17, 573–586. DOI: 10.1111 / obr.12409
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Андраде, Дж.М., Фраде, А.С., Гимарайнш, Дж. Б., Фрейтас, К. М., Лопес, М. Т., Гимарайнш, А. Л. и др. (2014). Ресвератрол увеличивает маркеры термогенеза коричневой жировой ткани за счет увеличения SIRT1 и расхода энергии и уменьшения накопления жира в жировой ткани мышей, получавших стандартную диету. Eur. J. Nutr. 53, 1503–1510. DOI: 10.1007 / s00394-014-0655-6
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Баргут, Т. К., Сильва-э-Силва, А. К., Суза-Мелло, В., Мандарим-де-Ласерда, К.А., Агила М. Б. (2016). Мышей кормили рыбьим жиром и повышали уровень термогенных маркеров бурой жировой ткани. Eur. J. Nutr. 55, 159–169. DOI: 10.1007 / s00394-015-0834-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Баскаран П., Кришнан В., Рен Дж. И Тьягараджан Б. (2016). Капсаицин вызывает потемнение белой жировой ткани и борется с ожирением, активируя механизмы, зависимые от канала TRPV1. Br. J. Pharmacol. 173, 2369–2389.DOI: 10.1111 / bph.13514
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Басу А. и Лукас Э. А. (2007). Механизмы и влияние зеленого чая на сердечно-сосудистую систему. Nutr. Ред. 65, 361–375. DOI: 10.1111 / j.1753-4887.2007.tb00314.x
CrossRef Полный текст | Google Scholar
Баутиста, Д. М., Сименс, Дж., Глейзер, Дж. М., Цуруда, П. Р., Басбаум, А. И., Стаки, К. Л. и др. (2007). Рецептор ментола TRPM8 является основным детектором холода в окружающей среде. Природа 448, 204–208. DOI: 10.1038 / nature05910
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Берубе-Паран, С., Пеллетье, К., Доре, Дж., И Трембле, А. (2005). Влияние инкапсулированных экстрактов зеленого чая и гуараны, содержащих смесь эпигаллокатехин-3-галлата и кофеина, на 24-часовой расход энергии и окисление жиров у мужчин. Br. J. Nutr. 94, 432–436. DOI: 10.1079 / BJN20051502
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бернс, Дж., Йокота, Т., Ашихара, Х., Лин, М. Э. и Крозье, А. (2002). Растительные продукты и растительные источники ресвератрола. J. Agric. Food Chem. 50, 3337–3340. DOI: 10.1021 / jf0112973
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Cantó, C., и Auwerx, J. (2009). PGC-1alpha, SIRT1 и AMPK, сеть измерения энергии, которая контролирует расход энергии. Curr. Opin. Липидол. 20, 98–105. DOI: 10.1097 / MOL.0b013e328328d0a4
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Чен, Л.Х., Чиен, Ю. В., Лян, К. Т., Чан, К. Х., Фань, М. Х., Хуанг, Х. Ю. (2017). Экстракт зеленого чая индуцирует гены, связанные с потемнением белой жировой ткани, и ограничивает прибавку в весе у крыс, питающихся высокоэнергетической диетой. Food Nutr. Res. 61: 1347480. DOI: 10.1080 / 16546628.2017.1347480
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Крещенцо Р., Маццоли А., Канчелье Р., Бьянко Ф., Джакко А., Ливерини Г. и др. (2017). Полиненасыщенные жирные кислоты стимулируют липогенез de novo и улучшают гомеостаз глюкозы во время возобновления кормления диетой с высоким содержанием жиров. Фронт. Physiol. 8: 178. DOI: 10.3389 / fphys.2017.00178
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ди Пьерро, Ф., Брессан, А., Ранальди, Д., Рапачоли, Г., Джакомелли, Л., и Бертуччиоли, А. (2015). Потенциальная роль биодоступного куркумина в потере веса и уменьшении жировой ткани сальника: предварительные данные рандомизированного контролируемого исследования с участием людей с избыточным весом и метаболическим синдромом. Предварительное изучение. Eur. Rev. Med. Pharmacol. Sci. 19, 4195–4202.
PubMed Аннотация | Google Scholar
Dulloo, A.G., Duret, C., Rohrer, D., Girardier, L., Mensi, N., Fathi, M., et al. (1999). Эффективность экстракта зеленого чая, богатого полифенолами катехина и кофеином, в увеличении 24-часового расхода энергии и окисления жиров у людей. Am. J. Clin. Nutr. 70, 1040–1045. DOI: 10.1093 / ajcn / 70.6.1040
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Dulloo, A.G., Seydoux, J., Girardier, L., Chantre, P.и Вандермандер Дж. (2000). Зеленый чай и термогенез: взаимодействие между катехин-полифенолами, кофеином и симпатической активностью. Внутр. J. Obes. Relat. Метаб. Disord. 24, 252–258. DOI: 10.1038 / sj.ijo.0801101
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хуанг, Дж., Ван, Й., Се, З., Чжоу, Й., Чжан, Й., и Ван, X. (2014). Эффект зеленого чая от ожирения при вмешательстве человека и фундаментальных молекулярных исследованиях. Eur. J. Clin. Nutr. 68, 1075–1087.DOI: 10.1038 / ejcn.2014.143
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Иноуэ, Н., Мацунага, Ю., Сато, Х., и Такахаши, М. (2007). Повышенное расходование энергии и окисление жиров у людей с высокими показателями ИМТ за счет приема новых и не острых аналогов капсаицина (капсиноидов). Biosci. Biotechnol. Biochem. 71, 380–389. DOI: 10.1271 / bbb.60341
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Иресон, К., Орр, С., Джонс, Д. Дж., Вершойл, Р., Лим, К. К., Луо, Дж. Л. и др. (2001). Характеристика метаболитов химиопрофилактического агента куркумина в гепатоцитах человека и крысы, а также в крысах in vivo и оценка их способности ингибировать индуцированную сложным эфиром форбола продукцию простагландина E2. Cancer Res. 61, 1058–1064.
PubMed Аннотация | Google Scholar
Jiang, C., Zhai, M., Yan, D., Li, D., Li, C., Zhang, Y., et al. (2017). Активация TRPM8, индуцированная диетой ментолом, усиливает «потемнение» WAT и уменьшает ожирение, вызванное диетой. Oncotarget 8, 75114–75126. DOI: 10.18632 / oncotarget.20540
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кавабата Ф., Иноуэ Н., Масамото Ю., Мацумура С., Кимура В., Кадоваки М. и др. (2009). Нежелкие аналоги капсаицина (капсиноиды) увеличивают скорость метаболизма и усиливают термогенез через желудочно-кишечный TRPV1 у мышей. Biosci. Biotechnol. Biochem. 73, 2690–2697. DOI: 10.1271 / bbb.
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кавада, Т., Каяхаши, С., Хида, Ю., Кога, К., Надачи, Ю., и Фушики, Т. (1998). Добавка рыбьего жира (бонито) усиливает экспрессию разобщающего белка в коричневой жировой ткани крысы. J. Agric. Food Chem. 46, 1225–1227. DOI: 10.1021 / jf9711000
CrossRef Полный текст | Google Scholar
Кхера Р., Мурад М. Х., Чандар А. К., Дулай П. С., Ван З., Прокоп Л. Дж. И др. (2016). Связь фармакологического лечения ожирения с потерей веса и побочными эффектами: систематический обзор и метаанализ. JAMA 315, 2424–2434. DOI: 10.1001 / jama.2016.7602
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ким, М., Гото, Т., Ю, Р., Учида, К., Томинага, М., Кано, Ю. и др. (2015). Прием рыбьего жира вызывает активацию UCP1 в коричневой и белой жировой ткани через симпатическую нервную систему. Sci. Отчет 5: 18013. DOI: 10.1038 / srep18013
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ким, С., Джин, Ю., Чой, Ю.и Парк Т. (2011). Ресвератрол оказывает действие против ожирения за счет механизмов, включающих подавление адипогенных и воспалительных процессов у мышей. Biochem. Pharmacol. 81, 1343–1351. DOI: 10.1016 / j.bcp.2011.03.012
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кобата К., Суто К., Тодо Т., Ядзава С., Иваи К. и Ватанабэ Т. (1999). Нордигидрокапсиат, новый капсиноид из плодов не острого перца Capsicum annuum. J. Nat.Prod. 62, 335–336. DOI: 10.1021 / np9803373
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Lagouge, M., Argmann, C., Gerhart-Hines, Z., Meziane, H., Lerin, C., Daussin, F., et al. (2006). Ресвератрол улучшает функцию митохондрий и защищает от метаболических нарушений, активируя SIRT1 и PGC-1alpha. Cell 15, 1109–1122. DOI: 10.1016 / j.cell.2006.11.013
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Laiglesia, L.M., Lorente-Cebrián, S., Prieto-Hontoria, P. L., Fernández-Galilea, M., Ribeiro, S. M., Sáinz, N., et al. (2016). Эйкозапентаеновая кислота способствует биогенезу митохондрий и способствует появлению бежевых свойств подкожных адипоцитов у субъектов с избыточным весом. J. Nutr. Biochem. 37, 76–82. DOI: 10.1016 / j.jnutbio.2016.07.019
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Lejeune, M. P., Kovacs, E. M., and Westerterp-Plantenga, M. S. (2003). Влияние капсаицина на окисление субстрата и поддержание веса после умеренной потери веса у людей. Br. J. Nutr. 90, 651–659. DOI: 10.1079 / BJN2003938
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Лоне, Дж., Чой, Дж. Х., Ким, С. В., и Юн, Дж. У. (2016). Куркумин индуцирует фенотип, подобный коричневому жиру, в 3T3-L1 и первичных белых адипоцитах. J. Nutr. Biochem. 27, 193–202. DOI: 10.1016 / j.jnutbio.2015.09.006
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Луди, М. Дж., Мур, Г. Э., и Мэттес, Р. Д. (2012).Влияние капсаицина и капсиата на энергетический баланс: критический обзор и метаанализ исследований на людях. Chem. Чувства 37, 103–121. DOI: 10.1093 / chemse / bjr100
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ma, S., Yu, H., Zhao, Z., Luo, Z., Chen, J., Ni, Y., et al. (2012). Активация чувствительного к холоду канала TRPM8 запускает UCP1-зависимый термогенез и предотвращает ожирение. J. Mol. Cell Biol. 4, 88–96. DOI: 10.1093 / jmcb / mjs001
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Манцороу, М., Павлиду, Э., Васиос, Г., Цагалиоти, Э., и Джиагинис, К. (2018). Влияние куркумина на хронические заболевания человека: обзор последних клинических данных. Phytother. Res. 32, 957–975. DOI: 10.1002 / ptr.6037
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Мартинес-Гонсалес, М.А., Салас-Сальвадо, Дж., Эструч, Р., Корелла, Д., Фито, М., Рос, Э. и др. (2015). Преимущества средиземноморской диеты: выводы исследования PREDIMED. Прог. Кардиоваск. Дис. 58, 50–60. DOI: 10.1016 / j.pcad.2015.04.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
МакКеми, Д. Д., Нойхауссер, В. М., и Джулиус, Д. (2002). Идентификация холодового рецептора показывает общую роль TRP-каналов в термочувствительности. Природа 416, 52–58. DOI: 10.1038 / nature719
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Нисикава, С., Камия, М., Аояма, Х., Номура, М., Хёдо, Т., Озеки, А. и др. (2018). Высокодисперсный и биодоступный куркумин, но не нативный куркумин, вызывает образование коричневых адипоцитов у мышей. Мол. Nutr. Food Res. 62: 1700131. DOI: 10.1002 / mnfr.201700731
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Номура, С., Ичиносе, Т., Дзиндэ, М., Кавасима, Ю., Тачияшики, К., и Имаидзуми, К. (2008). Катехины чая усиливают экспрессию мРНК разобщающего белка 1 в коричневой жировой ткани крысы. J. Nutr. Biochem. 19, 840–847. DOI: 10.1016 / j.jnutbio.2007.11.005
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Охьяма К., Ногуса Ю., Шинода К., Судзуки К., Баннаи М. и Каджимура С. (2016). Синергетический эффект против ожирения за счет комбинации капсиноидов и низкой температуры за счет стимулирования биогенеза бежевых адипоцитов. Diabetes Metab. Res. Ред. 65, 1410–1423. DOI: 10.2337 / db15-0662
PubMed Аннотация | CrossRef Полный текст
Оно, К., Tsukamoto-Yasui, M., Hara-Kimura, Y., Inoue, N., Nogusa, Y., Okabe, Y., et al. (2011). Внутрижелудочное введение капсиата, временного агониста канала рецепторного потенциала, вызывает термогенные симпатические реакции. J. Appl. Physiol. 110, 789–798. DOI: 10.1152 / japplphysiol.00128.2010
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Пахлавани М., Разафиманджато Ф., Рамалингам Л., Калупахана Н. С., Мусса Х., Скоггин С. и др. (2017). Эйкозапентаеновая кислота регулирует метаболизм коричневой жировой ткани у мышей с высоким содержанием жира и в клональных коричневых адипоцитах. J. Nutr. Biochem. 39, 101–109. DOI: 10.1016 / j.jnutbio.2016.08.012
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Пан, М. Х., Хуанг, Т. М., и Лин, Дж. К. (1999). Биотрансформация куркумина путем восстановления и глюкуронизации у мышей. Drug Metab. Dispos. 27, 486–494.
PubMed Аннотация | Google Scholar
Парк, С. Дж., Ахмад, Ф., Филп, А., Баар, К., Уильямс, Т., Луо, Х. и др. (2012). Ресвератрол улучшает связанные со старением метаболические фенотипы, ингибируя фосфодиэстеразы цАМФ. Cell 3, 421–433. DOI: 10.1016 / j.cell.2012.01.017
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Перголицци, Дж. В. Младший, Тейлор, Р. мл., ЛеКуанг, Дж. А., Раффа, Р. Б. и Исследовательская группа Нема. (2018). Роль и механизм действия ментола в обезболивающих препаратах местного действия. J. Clin. Pharm. Ther. 43, 313–319. DOI: 10.1111 / jcpt.12679
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Прайс, Н. Л., Гомес, А.П., Линг, А. Дж., Дуарте, Ф. В., Мартин-Монтальво, А., Норт, Б. Дж. И др. (2012). SIRT1 необходим для активации AMPK и благотворного воздействия ресвератрола на функцию митохондрий. Cell Metab. 15, 675–690. DOI: 10.1016 / j.cmet.2012.04.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Qiang, L., Wang, L., Kon, N., Zhao, W., Lee, S., Zhang, Y., et al. (2012). Коричневое ремоделирование белой жировой ткани посредством SirT1-зависимого деацетилирования Pparγ. Ячейка 150, 620–632. DOI: 10.1016 / j.cell.2012.06.027
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Раялам, С., Янг, Дж. Ю., Амбати, С., Делла-Фера, М. А., и Бэйле, К. А. (2008). Ресвератрол вызывает апоптоз и подавляет адипогенез в адипоцитах 3T3-L1. Phytother. Res. 22, 1367–1371. DOI: 10.1002 / ptr.2503
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Россато М., Гранзотто М., Макки В., Porzionato, A., Petrelli, L., Calcagno, A., et al. (2014). Белые адипоциты человека экспрессируют холодовой рецептор TRPM8, активация которого вызывает экспрессию UCP1, активацию митохондрий и выработку тепла. Мол. Клетка. Эндокринол. 383, 137–146. DOI: 10.1016 / j.mce.2013.12.005
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Snitker, S., Fujishima, Y., Shen, H., Ott, S., Pi-Sunyer, X., Furuhata, Y., et al. (2009). Влияние нового лечения капсиноидами на ожирение и энергетический обмен у людей: возможные фармакогенетические последствия. Am. J. Clin. Nutr. 89, 45–50. DOI: 10.3945 / ajcn.2008.26561
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Сонг, З., Ревело, X., Шао, В., Тиан, Л., Цзэн, К., Лей, Х. и др. (2018). Куркумин в рационе нацелен на воспаление белой жировой ткани мышей и экспрессию UCP1 в коричневой жировой ткани. Ожирение 26, 547–558. DOI: 10.1002 / oby.22110
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Штейн, Р.Дж., Сантос, С., Нагатоми, Дж., Хаяши, Ю., Миннери, Б. С., Ксавьер, М. и др. (2004). Холодные (TRPM8) и горячие (TRPV1) рецепторы в мочевом пузыре и мужских половых путях. J. Urol. 172, 1175–1178. DOI: 10.1097 / 01.ju.0000134880.55119.cf
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Тажино К., Мацумура К., Косада К., Шибакуса Т., Иноуэ К., Фушики Т. и др. (2007). Нанесение ментола на кожу всего туловища у мышей вызывает вегетативные и поведенческие реакции выделения тепла. Am. J. Physiol. Regul. Интегр. Комп. Physiol. 293, R2128 – R2135. DOI: 10.1152 / ajpregu.00377.2007
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Такахаши Ю., Идэ Т. (2000). Пищевые жирные кислоты n-3 влияют на уровень мРНК коричневой жировой ткани, разобщая белок 1, лептин белой жировой ткани и переносчик глюкозы 4 у крыс. Br. J. Nutr. 84, 175–184.
PubMed Аннотация | Google Scholar
Тиле, Р., Мюллер-Зейтц, Э., и Петц, М. (2008). Плоды перца чили: предполагаемые предшественники жирных кислот, характерных для капсаициноидов. J. Agric. Food Chem. 56, 4219–4224. DOI: 10.1021 / jf073420h
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Цавалер Л., Шаперо М. Х., Морковски С. и Лаус Р. (2001). Trp-p8, новый ген, специфичный для простаты, активируется при раке простаты и других злокачественных новообразованиях и имеет высокую гомологию с белками кальциевых каналов, которые могут быть временными рецепторами. Cancer Res. 61, 3760–3769.
PubMed Аннотация | Google Scholar
Ценг, Ю. Х., Коккотоу, Э., Шульц, Т. Дж., Хуанг, Т. Л., Винней, Дж. Н., Танигучи, К. М. и др. (2008). Новая роль костного морфогенетического белка 7 в коричневом адипогенезе и расходе энергии. Природа 454, 1000–1004. DOI: 10.1038 / nature07221
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Виртанен, К. А., Лиделл, М. Э., Орава, Дж., Хеглинд, М., Вестергрен, Р., Niemi, T., et al. (2009). Функциональная коричневая жировая ткань у здоровых взрослых. N. Engl. J. Med. 360, 1518–1525. DOI: 10.1056 / NEJMoa0808949
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Визин, Р. К. Л., Моцко-Соареш, А. С. П., Арментано, Г. М., Исикава, Д. Т., Крус-Нето, А. П., Карреттьеро, Д. К. и др. (2018). Кратковременное лечение ментолом способствует устойчивому термогенезу без индукции компенсирующего потребления пищи у крыс линии Вистар: последствия для контроля ожирения. J. Appl. Physiol. 124, 672–683. DOI: 10.1152 / japplphysiol.00770.2017
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Wang, S., Liang, X., Yang, Q., Fu, X., Rogers, C.J., Zhu, M., et al. (2015a). Ресвератрол вызывает образование коричневых адипоцитов в белом жире за счет активации AMP-активируемой протеинкиназы (AMPK) α1. Внутр. J. Obes. 39, 967–976. DOI: 10.1038 / ijo.2015.23
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ван, С., Ван, X., Ye, Z., Xu, C., Zhang, M., Ruan, B., et al. (2015b). Куркумин способствует потемнению белой жировой ткани в зависимости от норадреналина. Biochem. Биофиз. Res. Commun. 466, 247–253. DOI: 10.1016 / j.bbrc.2015.09.018
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Wang, S., Liang, X., Yang, Q., Fu, X., Zhu, M., Rodgers, B.D., et al. (2017). Ресвератрол усиливает образование и функцию коричневых адипоцитов, активируя АМФ-активированную протеинкиназу (AMPK) α1 у мышей, получавших диету с высоким содержанием жиров. Мол. Nutr. Еда. Res. 61: 1600746. DOI: 10.1002 / mnfr.201600746
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Вестертерп-Плантенга, М., Дипвенс, К., Йоосен, А. М., Берубе-Паран, С., и Трембле, А. (2006). Метаболические эффекты специй, чая и кофеина. Physiol. Behav. 89, 85–91. DOI: 10.1016 / j.physbeh.2006.01.027
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Йонеширо, Т., Аита, С., Каваи, Ю., Иванага, Т., и Сайто, М. (2012). Невкусные аналоги капсаицина (капсиноиды) увеличивают расход энергии за счет активации коричневой жировой ткани у людей. Am. J. Clin. Nutr. 95, 845–850. DOI: 10.3945 / ajcn.111.018606
PubMed Аннотация | CrossRef Полный текст | Google Scholar
.