Чем полезны растительные белки и где их больше всего
Зачем вообще нужны белки
Человеческому телу жизненно необходимы 20 аминокислот: они участвуют в процессе деления клеток. 12 из них организм взрослого человека производит сам, остальные восемь должны поступать с пищей. Эти столь важные элементы содержатся как раз в белках, которых больше всего в продуктах животного происхождения.
Из белков строятся наши мышцы. Белки обеспечивают выработку иммунитета, передачу нервных импульсов, рост, развитие и восстановление клеток . Кроме того, они хорошо утоляют голод. В общем, обойтись без них никак нельзя.
В среднем каждой женщине в день требуется от 46 г белков, а мужчине — от 56 г в зависимости от веса.
Что особенного в растительных белках
В растениях тоже присутствуют белки, однако в гораздо меньших количествах, чем в мясе и молочных продуктах. Тем не менее растительные белки содержат тот же необходимый набор аминокислот, а значит, могут частично или полностью удовлетворить потребности организма .
При этом в растениях меньше жиров, чем в мясе, и вообще нет холестерина, поэтому с их помощью можно получить незаменимые белки без ненужного довеска.
Зачем переходить на растительные белки
Чтобы похудеть
Чаще всего отказываются от животных белков люди, которые стремятся сбросить вес. Растительная пища менее калорийная и жирная, поэтому многие именно на неё и переходят.
Но если долго питаться одними овощами, может возникнуть дефицит белков, а значит, самочувствие ухудшится. Поэтому употребление растительных белков — это залог похудения без вреда для здоровья.
По этическим соображениям
Многие становятся вегетарианцами или веганами, потому что им жалко животных. Обойтись без мяса или вообще без продуктов животного происхождения человеческий организм может, но без белков — нет. Поэтому сделавшие выбор в пользу растительной диеты получают их из других источников.
Чтобы вести здоровый образ жизни
Некоторые вынуждены переключиться на растительную диету по медицинским показаниям. Например, из-за высокого уровня холестерина, который может провоцировать возникновение тромбов в сосудах и сердечные приступы . Холестерин содержится только в животной пище, поэтому растительные белки безопаснее для людей с сердечно-сосудистыми заболеваниям.
Например, из-за высокого уровня холестерина, который может провоцировать возникновение тромбов в сосудах и сердечные приступы . Холестерин содержится только в животной пище, поэтому растительные белки безопаснее для людей с сердечно-сосудистыми заболеваниям.
Но подобные проблемы лучше предупреждать. Поэтому есть больше растительных белков и меньше животных полезно и здоровым людям. Это уменьшает риск возникновения проблем с сердцем, повышенного кровяного давления, диабета и ожирения.
Откуда получать растительные белки
Соя
Соя — безусловный лидер среди растений. 100 г её семян — это 36 г белков. Поэтому соевые продукты так ценятся в странах Дальнего Востока, где традиционно было мало развито мясное животноводство.
Доказано, что народы-любители сои меньше болеют раком, сердечно-сосудистыми заболеваниями и остеопорозом .
На наши тарелки соевые бобы попадают в основном в переработанном виде: в качестве соевого мяса, молока и сыра тофу.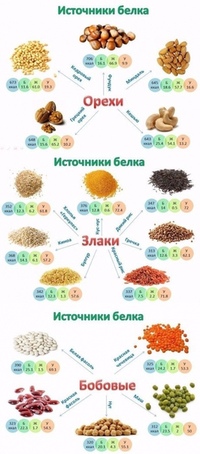
Другие бобовые
Чуть меньше белков — 21 г на 100 г веса — содержится в фасоли. Конечно, она будет полезнее, если купить её в высушенном виде, а потом самостоятельно замочить и сварить, но подойдут и консервы. Чечевица может похвастаться только 9 г белков на 100 г веса, зелёный горошек — 5 г.
А вот арахис опережает их всех: в 100 г плодов этого бобового растения содержится 26 г белков. Зато и жира там немало (49 г), поэтому налегать на эти «орехи» не стоит.
Сравнительно недавно в России стал популярен нут, или турецкий горох, из которого готовят хумус. Для стремящихся похудеть он — настоящая находка: 100 г нута — это 19 г белков и всего 6 г жиров.
Орехи
Орехи не уступают бобовым по содержанию белков. Например, 100 г миндаля — это 21 г белков, а 100 г фисташек — 20 г. Чуть меньше этих веществ в составе кешью (18 г), грецких орехов и фундука (по 15 г). Но стоит помнить, что орехи содержат много жиров.
Злаки
Ещё один важный источник растительных белков — это злаки. В 100 г овсянки, например, содержится 17 г белков, в пшенице — 14 г, в кукурузе — 9 г, в рисе — 2,7 г.
В 100 г овсянки, например, содержится 17 г белков, в пшенице — 14 г, в кукурузе — 9 г, в рисе — 2,7 г.
Овощи и фрукты
Овощи и фрукты, конечно, не лучший источник белков. Но и среди них есть свои чемпионы. Например, шпинат (2,9 г белков на 100 г), брокколи (2,8 г), спаржа (2,2 г), авокадо (2 г), банан (1,1 г) и вишня (1 г).
Читайте также
Без мяса: 7 продуктов с запасом белка растительного происхождения :: Здоровье :: РБК Стиль
© Shutterstock
Автор Фрида Морева
28 августа 2018
Многие сегодня по разным причинам ограничивают потребление продуктов животного происхождения или отказываются от них совсем.
Как известно, для стройной фигуры и крепкого здоровья необходим баланс белков, жиров и углеводов. А при строгой или вегетарианской диете есть риск дефицита белка (о том, как его обнаружить, мы уже писали) со всеми его неприятными последствиями в виде ослабления организма, потери мышечной массы и тонуса кожи. Рассказываем о семи растительных продуктах, которые помогут получать белок в большем количестве.
Самое очевидное решение, чтобы добыть растительный белок, — искать его в бобовых. Лидеры — это, определенно, красная чечевица — 18 граммов в одной порции (около стакана в готовом виде), красная фасоль — 16 граммов, черная фасоль — 14 граммов, маш — 14 граммов, нут — 14 граммов.
Обычно к гречке обращаются за железом (кроме того, что ее считают вкусной), но она также подойдет тем, кто старается есть больше белка. В одной порции гречки (около 150 граммов готовой крупы) — 5 граммов белка. То есть сидеть на одной гречке и получать достаточно белка не получится, но она неплохое подспорье для сбалансированного другими продуктами меню.
Любимый продукт западных специалистов по питанию. В России киноа стоит дорого, но у него достаточно экономичный расход. Важное правило: перед приготовлением киноа необходимо промыть, это избавит его от горьковатого привкуса. В одной порции киноа — 8 граммов белка.
Цельнозерновой хлеб с проростками
В обычном белом хлебе белка минимум, так что надеяться тут не на что. Другое дело — цельнозерновой, особенно те его разновидности, что содержат семена, орехи и проростки. В зависимости от состава один кусок такого хлеба может обеспечить вас 3–5 граммами белка. И конечно же, необработанное зерно вместе с его оболочкой дает организму множество витаминов (в первую очередь все та же В-группа) и микроэлементов.
Другое дело — цельнозерновой, особенно те его разновидности, что содержат семена, орехи и проростки. В зависимости от состава один кусок такого хлеба может обеспечить вас 3–5 граммами белка. И конечно же, необработанное зерно вместе с его оболочкой дает организму множество витаминов (в первую очередь все та же В-группа) и микроэлементов.
Соевый «творог» часто предлагается как верный источник белка (8 граммов в 100 граммах тофу) и почти так же часто отвергается из-за специфического вкуса. Секрет приготовления тофу в том, что он легко приобретает вкус маринада или того соуса, в котором готовится. Поэтому вместо того, чтобы пытаться есть тофу сам по себе, попробуйте приготовить с ним красный карри, чили или грибной суп. Мягкий тофу может стать альтернативой яйцам в утреннем «омлете». Среди других заслуг этого продукта — восемь важнейших аминокислот, витамин B1, магний, медь и цинк.
Тыквенные семена
Тыквенные семечки — постоянные участники всяческих списков самых полезных продуктов. В них и правда много нужных микроэлементов, антиоксидантов и внушительный запас магния (эффект «антистресс»). Хороши они и в качестве источника белка — 5 граммов в одной горсти (25–30 граммов).
В них и правда много нужных микроэлементов, антиоксидантов и внушительный запас магния (эффект «антистресс»). Хороши они и в качестве источника белка — 5 граммов в одной горсти (25–30 граммов).
Как и киноа, амарант в России — достаточно экзотическая и недешевая крупа. Но попробовать ее найти и приготовить стоит. Одна порция амаранта содержит 9 граммов белка. Амарант также встречается в виде муки, которую можно использовать для здоровых вариантов выпечки.
так ли полезен растительный белок и правда ли, что у веганов хрупкие кости?
Веганство как никакая другая диета требует от человека очень глубоких знаний — именно от этого будет зависеть ее успех и ваше здоровье. В книге «Веганы против мясоедов. В поисках золотой середины» кандидат медицинских наук Юрий Гичев рассказывает о подводных камнях системы питания, при которой все продукты животного происхождения исключены из рациона.
Можно ли полностью полагаться на растительный белок?
В обществе широко распространено мнение о том, что растительный белок является неполноценным и не обеспечивает организм человека всеми необходимыми аминокислотами. На первый взгляд действительно может показаться, что раз уж человек относится к царству животных, то животный белок должен иметь гораздо большее сходство с белками нашего организма по сравнению с любыми белковыми продуктами растительного происхождения. И если сравнивать молоко, яйца или мясо с одной стороны и бобы, овес и пшеницу с другой, первые будут содержать, конечно же, гораздо более полноценный белок по сравнению со вторыми.
Но что значит «более полноценный»? Дело в том, что все белки состоят из отдельных «кирпичиков» — аминокислот. Часть из этих аминокислот мы можем синтезировать сами, а часть — так называемые незаменимые аминокислоты —мы должны получать из пищи. Соответственно, чем больше в составе пищевого белка незаменимых аминокислот, тем он более полноценный. Так вот, животные белки в массе своей содержат больший процент незаменимых аминокислот по сравнению с растительными белками. Однако на самом деле разница совсем небольшая. Так, в молочном белке незаменимые аминокислоты составляют 49 %, а в чечевице — 40 %. В мясе и яйце — 44 %, а в бобах и киноа — 39 %. А вот рыба и соя вовсе не различаются по этому показателю — и там и там по 38 %. Соответственно, если мы будем употреблять растительного белка чуть больше рекомендуемой суточной нормы (на 10-20 %), мы сможем легко получить такое же количество незаменимых аминокислот, как те, кто употребляет животный белок.
Соответственно, чем больше в составе пищевого белка незаменимых аминокислот, тем он более полноценный. Так вот, животные белки в массе своей содержат больший процент незаменимых аминокислот по сравнению с растительными белками. Однако на самом деле разница совсем небольшая. Так, в молочном белке незаменимые аминокислоты составляют 49 %, а в чечевице — 40 %. В мясе и яйце — 44 %, а в бобах и киноа — 39 %. А вот рыба и соя вовсе не различаются по этому показателю — и там и там по 38 %. Соответственно, если мы будем употреблять растительного белка чуть больше рекомендуемой суточной нормы (на 10-20 %), мы сможем легко получить такое же количество незаменимых аминокислот, как те, кто употребляет животный белок.
Впрочем, мы уже говорили, что на самом деле все не так просто. Нам важно получить достаточное количество каждой из восьми незаменимых аминокислот, а этого большинство растительных белков не могут обеспечить. Несколько упрощая, можно сказать, что бобовым для того, чтобы быть полноценным источником белка, не хватает необходимого количества метионина, а злакам — лизина. Само собой напрашивающееся решение: смешать в равных пропорциях бобовые и злаковые, что даст нам полный набор незаменимых аминокислот в необходимом объеме. И действительно, смесь, скажем, овса и чечевицы по своему аминокислотному профилю вплотную приближается к говядине.
Само собой напрашивающееся решение: смешать в равных пропорциях бобовые и злаковые, что даст нам полный набор незаменимых аминокислот в необходимом объеме. И действительно, смесь, скажем, овса и чечевицы по своему аминокислотному профилю вплотную приближается к говядине.
Правда, здесь есть еще один подводный камень. Дело в том, что очень многие источники растительного белка одновременно содержат естественные факторы, которые значительно ухудшают усвоение белка. Например, фитиновая кислота, о которой мы говорили выше, или танины, которые в очень больших количествах содержатся в растениях (особенно в недозрелых) и могут связывать белки, образуя нерастворимые комплексы. Кроме того, почти во всех бобовых (которые по праву считаются богатейшим источником растительного белка), а также в картофеле и томатах есть особые вещества, которые блокируют протеолитические ферменты нашей пищеварительной системы и существенно затрудняют усвоение белка.
Кстати, именно поэтому всем известная соя существенно уступает мясу, яйцам или молоку по питательной ценности белка, хотя, если брать чисто химический состав, она должна была бы как минимум им не уступать. Впрочем, и эту проблему можно легко обойти. Во-первых, то же проращивание бобов сокращает концентрацию антибелковых факторов почти до нуля, и, возможно именно поэтому проращенные семена и бобы стали важной частью веганского рациона. Во-вторых, долгая температурная обработка также снижает активность этих веществ. В-третьих, нужно всегда помнить о том, что веганы должны употреблять в 1,2–1,5 раза больше белка по сравнению со стандартными нормами, рекомендованными для смешанных рационов, что позволяет обойти в том числе и эту проблему.
Kальций и кости
Почему-то априори считается, что веганы не способны поддерживать оптимальное состояние костной системы. Якобы кальций в составе растительной пищи очень плохо усваивается, а витамин Д вообще там отсутствует. И многие исследования действительно свидетельствуют о том, что уровень потребления кальция веганами в среднем чуть ниже, чем у людей, придерживающихся обычного рациона. Однако тут упускается из виду очень важный момент, а именно то, что преимущественно растительный рацион способствует повышению эффективности обмена кальция. Это происходит за счет того, что ионы магния и калия, которых очень много в растительной пище, способствуют ощелачиванию крови, что значительно уменьшает активность естественной резорбции (вымывания) кальция из костей и тем самым снижает потребность в этом минерале. У людей же, предпочитающих белково-мясной рацион, кровь, наоборот, имеет более кислую реакцию, что увеличивает активность вымывания кальция из костей и в итоге повышает потребность в нем. Кроме того, почти все смешанные рационы содержат гораздо больше соли по сравнению с веганскими диетами, а натрий, как известно, также повышает уровень выведения кальция с мочой.
Якобы кальций в составе растительной пищи очень плохо усваивается, а витамин Д вообще там отсутствует. И многие исследования действительно свидетельствуют о том, что уровень потребления кальция веганами в среднем чуть ниже, чем у людей, придерживающихся обычного рациона. Однако тут упускается из виду очень важный момент, а именно то, что преимущественно растительный рацион способствует повышению эффективности обмена кальция. Это происходит за счет того, что ионы магния и калия, которых очень много в растительной пище, способствуют ощелачиванию крови, что значительно уменьшает активность естественной резорбции (вымывания) кальция из костей и тем самым снижает потребность в этом минерале. У людей же, предпочитающих белково-мясной рацион, кровь, наоборот, имеет более кислую реакцию, что увеличивает активность вымывания кальция из костей и в итоге повышает потребность в нем. Кроме того, почти все смешанные рационы содержат гораздо больше соли по сравнению с веганскими диетами, а натрий, как известно, также повышает уровень выведения кальция с мочой.
Это показывают и эпидемиологические исследования, не выявившие никакой разницы в показателях минеральной плотности костей и риска переломов между веганами и традиционно питающимися людьми. Причем не только в молодом, но и в среднем и пожилом возрасте. Хотя тут, конечно, нельзя исключать и влияния на минеральную плотность костей физической активности: веганы в силу их гораздо большей приверженности здоро-вому образу жизни обычно ведут гораздо более активный образ жизни.
Витамин Д также критически важен для здоровья костей, однако его можно получать не только из животной пищи. Полностью компенсировать дефицит этого витамина можно с помощью солнечных ванн (естественных летом и искусственных зимой): организм синтезирует витамин Д под влиянием ультрафиолетовых лучей. Наконец, ничто не ме-шает веганам принимать добавки с витамином Д2 (одна из форм природного витамина, существующая наряду с самой распространенной его формой — витамином Д3), который имеет неживотное происхождение и таким образом не противоречит принципам этой диеты.
Витамины животного происхождения
Как известно, витамины — это незаменимые жизненно важные вещества, которые должны регулярно и в нужном объеме поступать в наш организм. Но при этом часть этих витаминов имеет исключительно животное происхождение, что, казалось бы, окончательно ставит под сомнение адекватность веганства. Тем не менее и тут очень быстро выясняется, что максимально разнообразный растительный рацион или здоровый образ жизни могут во многом решить эту проблему.
Про решение проблемы дефицита витамина Д3 мы уже поговорили в предыдущем разделе. Или, например, витамин А — незаменимое вещество исключительно животного происхождения — легко заменяется бета-каротином и другими каротиноидами, которые в очень большом количестве содержатся в растениях. Аналогичным образом можно заменить и омега-3 полиненасыщенные жирные кислоты (витамин F), которые ассоциируются у большинства из нас исключительно с морской рыбой и морепродуктами (морские водоросли не могут считаться надежным источником омега-3 жирных кислот из-за очень высокого содержания йода).
В частности, альфа-линоленовая кислота, которая в большом количестве содержится в них (или в маслах, полученных из этих семян), может полностью компенсировать дефицит морских омега-3 жирных кислот, так как превращается в организме в аналоги эйкозапентаеновой и докозагексаеновой кислот, которые и являются главными представителями омега-3 полиненасыщенных жирных кислот. Правда, очень важно понимать, что скорость биохимических реакций синтеза омега-3 жиров в этом случае будет довольно медленной и, главное, очень сильно зависит от количества белка, а также многих витаминов и минералов в пище (витамин В6, биотин, кальций, магний, цинк, медь). И это еще один аргумент в пользу утверждения о том, что веганский рацион может считаться абсолютно полноценным только при условии максимального разнообразия пищи.
Таким образом, получается, что единственным жизненно важным веществом, которое будет всегда дефицитным в организме веганов, является витамин В12. Существующее мнение о том, что некоторые виды морских водорослей содержат достаточное количество витамина В12, пока является лишь предположением, не имеющим достоверной доказательной базы. Однако проблема дефицита витамина В12 легко решается приемом препаратов этого витамина, тем более что сегодня витамин В12 получают не из печени животных (как это было еще 30 лет назад), а путем бактериального синтеза.
Существующее мнение о том, что некоторые виды морских водорослей содержат достаточное количество витамина В12, пока является лишь предположением, не имеющим достоверной доказательной базы. Однако проблема дефицита витамина В12 легко решается приемом препаратов этого витамина, тем более что сегодня витамин В12 получают не из печени животных (как это было еще 30 лет назад), а путем бактериального синтеза.
В то же время уникальная (в отличие от всех других витаминов и минералов) способность витамина В12 накапливаться в печени на несколько лет вперед говорит о том, что животная пища никогда не была регулярным и уж тем более базовым элементом нашего рациона.
Но как же тогда обходятся без этого важнейшего витамина растительноядные животные? Могут ли веганы научиться у них решению этой проблемы? У жвачных животных витамин В12 синтезируется бактериями, которые обитают в желудке и помогают переваривать грубую растительную пищу. Поступая вместе с пищей в тонкий кишечник, этот витамин прекрасно там усваивается. К сожалению, у человека кислотность желудка слишком велика, чтобы в нем могли выживать эти бактерии, и поэтому мы не можем полагаться на такой источник витамина В12. Впрочем, у нас и у других растительноядных животных, не относящихся к классу жвачных, витамин В12 тоже синтезируется бактериями, но только не теми, что обитают в желудке, а микроорганизмами, населяющими толстый кишечник.
Поступая вместе с пищей в тонкий кишечник, этот витамин прекрасно там усваивается. К сожалению, у человека кислотность желудка слишком велика, чтобы в нем могли выживать эти бактерии, и поэтому мы не можем полагаться на такой источник витамина В12. Впрочем, у нас и у других растительноядных животных, не относящихся к классу жвачных, витамин В12 тоже синтезируется бактериями, но только не теми, что обитают в желудке, а микроорганизмами, населяющими толстый кишечник.
Однако не стоит раньше времени радоваться, так как здесь есть кое-какие деликатные подробности. Так как витамин В12 может усваиваться только в верхних отделах кишечника, смысла в его синтезе в толстой кишке, на первый взгляд, никакого нет. Он там банально не сможет усвоиться и попасть в кровь, так как в толстой кишке нет каналов для усвоения витамина В12. Однако животные (и скорее всего, и наши далекие предки) научились легко обходить это препятствие, поедая — простите за необходимые подробности — свои или чужие экскременты, и именно последние являются для них главным источником витамина В12 (а также многих других полезных веществ, синтезируемых кишечной флорой). Разумеется, точно так же могли бы поступать и веганы, и тогда бы это было веганство в чистом виде, но, согласитесь, прием синтетического витамина В12 выглядит, мягко говоря, гораздо более предпочтительным.
Разумеется, точно так же могли бы поступать и веганы, и тогда бы это было веганство в чистом виде, но, согласитесь, прием синтетического витамина В12 выглядит, мягко говоря, гораздо более предпочтительным.
При всей комичности предыдущего абзаца мы хотим еще раз подчеркнуть, что дефицит витамина В12 — совсем не пустяк. Данный жизненно важный витамин участвует в очень многих процессах в нашем организме и в том числе играет важнейшую роль в обезвреживании гомоцистеина, который не менее опасен для сосудов, чем всем известный холестерин (см. более подробно в третьей части данного издания).
И, кстати, одним из парадоксальных выводов многих исследований состояния здоровья адвентистов, о которых мы так много говорили выше, было то, что веганы зачастую гораздо более подвержены риску смертности от сердечно-сосудистых болезней по сравнению не только с лактоововегетарианцами, но даже по сравнению с невегетарианцами. И объяснением этого парадокса, скорее всего, служит именно скрытый и очень длительный дефицит витамина В12. Получается, что несбалансированный веганский рацион, с одной стороны, полностью защищает нас от избытка холестерина, но с другой — обрекает нас на не менее опасное хроническое поражение сосудов вследствие совсем другой причины.
И объяснением этого парадокса, скорее всего, служит именно скрытый и очень длительный дефицит витамина В12. Получается, что несбалансированный веганский рацион, с одной стороны, полностью защищает нас от избытка холестерина, но с другой — обрекает нас на не менее опасное хроническое поражение сосудов вследствие совсем другой причины.
Отрывок предоставлен для публикации издательским домом «Питер».
Растения-биофабрики
Развитие биотехнологий открыло новые возможности использования живых организмов на благо человечества. Методы генетической инженерии позволяют производить различные вещества в живых объектах, следовательно, мы можем использовать эти объекты в качестве природных «фабрик». Центральная догма молекулярной биологии в общем случае гласит: ДНК → РНК → белок. Именно белок часто является конечным продуктом биотехнологического производства: это может быть инсулин, интерфероны, антитела, ферменты, вакцины. .. Нам лишь нужно задать программу и «записать» ее в ДНК, а живой объект всё сделает сам. В качестве «фабрик» используют клетки дрожжей, бактерий, растений, а также культуры клеток насекомых и млекопитающих. В этой статье речь пойдет о растительных биофабриках.
.. Нам лишь нужно задать программу и «записать» ее в ДНК, а живой объект всё сделает сам. В качестве «фабрик» используют клетки дрожжей, бактерий, растений, а также культуры клеток насекомых и млекопитающих. В этой статье речь пойдет о растительных биофабриках.
Что такое растение-биофабрика?
Как объяснить понятие «растение-биофабрика»? Можно сказать, что это природное предприятие, которое будет изготавливать нужный нам биопродукт. В отличие от обычной фабрики, на таком предприятии будут трудиться не рабочие, а компоненты клеток: полимеразы нуклеиновых кислот, рибосомы, тРНК и многие другие. А производить они будут белок.
Почему именно растения?
Рисунок 1. Сравнение систем продукции рекомбинантных белков (от самых привлекательных «+» до наименее привлекательных «—»).
В настоящее время для наработки белков чаще всего используют бактерий, дрожжи, культуры клеток насекомых и млекопитающих. Очень привлекательной системой синтеза и накопления рекомбинантных белков (экспрессионной системой) являются и растения, и тому есть несколько причин. Прежде всего, в растительных тканях нет риска загрязнения рекомбинантного белка вирусами животных и прионами — инфекционными белками [1]. Растительные клетки обеспечивают правильную модификацию рекомбинантного белка, характерную для эукариотических клеток [2, 3]. Также большое значение имеют стоимость, простота и время. На рисунке 1 сравнивается несколько основных экспрессионных систем.
Прежде всего, в растительных тканях нет риска загрязнения рекомбинантного белка вирусами животных и прионами — инфекционными белками [1]. Растительные клетки обеспечивают правильную модификацию рекомбинантного белка, характерную для эукариотических клеток [2, 3]. Также большое значение имеют стоимость, простота и время. На рисунке 1 сравнивается несколько основных экспрессионных систем.
Из таблицы видно, что идеальной системы экспрессии не существует. Сегодня в России шире всего распространены бактериальные системы с E. coli в качестве самой популярной «рабочей лошадки». Еще в 2009 г. на долю этого микроорганизма приходилось 85% от всех систем экспрессии, несмотря на ряд существенных недостатков.
У каждой биофабрики есть свои плюсы и свои минусы. Но растительная система для многих ситуаций оказывается наиболее привлекательной.
Как заставить растение производить белок?
Для того чтобы растение производило нужный белок, в клетки этого растения необходимо внести чужеродный генетический материал — последовательность ДНК, кодирующую аминокислотную последовательность нужного белка.
Первый этап модификации растений с применением методов генетической инженерии включает поиск и выделение (или синтез) генов, которые будут перенесены в растительный геном. Гены, представляющие интерес для биотехнологов (целевые гены), могут быть «выращены» химическим путем, а также наработаны с помощью ПЦР (полимеразной цепной реакции). Затем целевой ген встраивается в подходящий вектор*, который и доставляет его к месту производства белка — подобно тому, как вагон с сырьём прицепляется к паровозу, направляющемуся к фабрике.
Как перенести в растительную клетку необходимую последовательность ДНК?
В настоящее время чаще используют два способа.
Первый связан с использованием природных генно-инженерных «навыков» почвенной агробактерии Agrobacterium tumefaciens, способной переносить фрагменты ДНК в растительную клетку, то есть модифицировать ее генетически. Этот процесс в природе происходит повсеместно и регулярно. В природной A. tumefaciens помимо хромосомы содержится Ti-плазмида, в состав которой входит так называемая Т-ДНК (transferred DNA) длиной 12–22 т.п.н., встраивающаяся в ДНК растительной хромосомы. Она кодирует ферменты синтеза фитогормонов и опинов — производных аминокислот, которые используются бактерией как источник углерода, азота и энергии.
tumefaciens помимо хромосомы содержится Ti-плазмида, в состав которой входит так называемая Т-ДНК (transferred DNA) длиной 12–22 т.п.н., встраивающаяся в ДНК растительной хромосомы. Она кодирует ферменты синтеза фитогормонов и опинов — производных аминокислот, которые используются бактерией как источник углерода, азота и энергии.
Т-ДНК Ti-плазмид обладает двумя свойствами, делающими ее почти идеальным вектором для введения чужеродных генов в клетки растений. Во-первых, круг хозяев агробактерий очень широк: они трансформируют клетки практически всех двудольных растений (а при некоторых стараниях можно добиться заражения и однодольных, в том числе злаков). Во-вторых, интегрированная в геном растения Т-ДНК наследуется как простой доминантный признак в соответствии с законами Менделя. Простейший способ введения Т-ДНК в клетки растения — заражение его A. tumefaciens, содержащей подходящую Ti-плазмиду, дальнейшее же предоставляется естественному ходу событий. Необходимо только уметь встраивать нужные гены в Т-сегмент плазмидной ДНК.
После проникновения агробактерий в межклеточное пространство Т-ДНК переносится из агробактерии в ядро растительной клетки и встраивается в хромосомную ДНК. Далее происходят транскрипция и трансляция — синтезируется целевой белок. Сама бактерия в клетку при этом не проникает, а остается в межклеточном пространстве.
Второй способ — баллистическая трансформация с использованием генной пушки. Маленькие золотые или вольфрамовые частицы покрывают чужеродной ДНК и «выстреливают» в молодые растительные клетки. Этот метод позволяет встраивать нужные гены не только в хромосомы растений, но и в геном их органелл — пластид. Это очень полезно в первую очередь для получения растений, защищенных от вредителей, но при этом безопасных для опылителей: ведь трансгены не экспрессируются в не имеющих пластид цветках. Недавно таким способом создали трансгенный (а именно — транспластомный) картофель, в хлоропластах которого образуется и сохраняется неповрежденной двухцепочечная РНК, блокирующая синтез жизненно важного белка колорадского жука — β-актина. Поедая листья такого картофеля, личинки жуков погибают в считанные дни [6].
Поедая листья такого картофеля, личинки жуков погибают в считанные дни [6].
Менее распространенные, но всё же действенные способы трансформации — электропорация и трансформация с помощью вирусов.
Постоянная и временная экспрессия гена
Рисунок 2. Транзиентная экспрессия чужеродных генов в растениях с помощью агроинфильтрации. А — общий механизм процесса, Б — визуализация синтезируемого в растении репортера — GFP (зеленого флуоресцентного белка) — освещением листа ультрафиолетом.
В генетической инженерии растений можно встретить такие понятия: генетически модифицированное (ГМ, или трансгенное) растение и растение, обеспечивающее транзиентную (временную) экспрессию гена. В чем же разница?
Если речь идет о трансгенном растении, то подразумевается, что чужеродная ДНК интегрирована в хромосому. К настоящему времени получены десятки видов трансгенных растений, в геном которых перенесена ДНК, кодирующая различные белки медицинского назначения, такие как антигены различных возбудителей инфекционных заболеваний, терапевтические белки и моноклональные антитела [7, 8, 9]. Однако количество синтезируемого целевого белка в таких растениях обычно небольшое (менее 1% от общего растворимого белка).
Однако количество синтезируемого целевого белка в таких растениях обычно небольшое (менее 1% от общего растворимого белка).
При транзиентной экспрессии ДНК обычно не включается в ядерный геном, не реплицируется и не передается по наследству. Этот вид экспрессии не постоянный, однако некоторое время в одной клетке может присутствовать большое количество копий чужеродной ДНК, что обеспечивает высокий уровень синтеза конечного продукта. При наработке белков в растениях данный вариант наиболее эффективен. Мы как бы арендуем фабрику, и это оказывается более рентабельным, чем ее покупка. На рисунке 2 представлена модель переноса в растительную клетку ДНК для транзиентной экспрессии (в роли курьера — Agrobacterium tumefaciens).
Что может производить растение-биофабрика?
Использование растений в биотехнологии развивается в нескольких направлениях (рис. 3).
Рисунок 3. Возможности использования растений в биотехнологических целях.
Первое направление включает в себя создание растений с новыми свойствами. О несомненных плюсах трансгенных растений сказано немало [10]. Так, ведется разработка сортов, устойчивых одновременно к насекомым-вредителям и болезням, вызываемым вирусами, плесневыми грибками и бактериями. Идут исследования, которые позволят вывести сорта сельскохозяйственных культур, переносящих неблагоприятные климатические и химические условия, например, засуху и засоленность почвы [11]. Создаются продукты, в которых значительно увеличена доля полезных и питательных веществ, снижено содержание насыщенных жиров и аллергенов. Особое внимание уделяется разнонаправленным модификациям риса — ценного и относительно недорогого продукта питания, который можно было бы производить во всех беднейших регионах мира, включая засушливые [12].
О несомненных плюсах трансгенных растений сказано немало [10]. Так, ведется разработка сортов, устойчивых одновременно к насекомым-вредителям и болезням, вызываемым вирусами, плесневыми грибками и бактериями. Идут исследования, которые позволят вывести сорта сельскохозяйственных культур, переносящих неблагоприятные климатические и химические условия, например, засуху и засоленность почвы [11]. Создаются продукты, в которых значительно увеличена доля полезных и питательных веществ, снижено содержание насыщенных жиров и аллергенов. Особое внимание уделяется разнонаправленным модификациям риса — ценного и относительно недорогого продукта питания, который можно было бы производить во всех беднейших регионах мира, включая засушливые [12].
В эту же группу можно отнести трансгенные растения, которые используются в качестве модельных объектов для изучения фундаментальных проблем функционирования генов.
Многие ГМ-растения сейчас находятся в массовом производстве. Это соя, кукуруза, картофель, маслянистые растения (рапс и подсолнух) и многие другие (рис. 4). Странами-лидерами в производстве таких растений являются США, Канада, Аргентина и Бразилия. Догоняют их Китай и Япония. С рядом растений работают некоторые страны ЕС и Австралия.
4). Странами-лидерами в производстве таких растений являются США, Канада, Аргентина и Бразилия. Догоняют их Китай и Япония. С рядом растений работают некоторые страны ЕС и Австралия.
Среди компаний, разрабатывающих трансгенные растения, можно отметить Calgen, Monsanto, Ciba Seeds. Несмотря на то, что ГМ-растения продаются на многих рынках мира, дискуссии о безопасности их использовании еще не закончены. Больше всего слухов и скандалов разворачивается вокруг компании «Монсанто». Основная продукция этой фирмы — генетически модифицированные семена кукурузы, сои, хлопка, а также самый распространенный в мире гербицид «Раундап» (непатентованное название — глифосат).
Основанная Джоном Фрэнсисом Куини в 1901 году как чисто химическая компания, «Монсанто» эволюционировала в концерн, специализирующийся на высоких технологиях в области сельского хозяйства. Ключевым моментом в этой трансформации стал 1996 год, когда «Монсанто» выпустила на рынок первые генно-модифицированные сельскохозяйственные культуры: сою «Раундап Рэди» (Roundup Ready, RR), устойчивую к глифосату, и хлопок «Боллгард» (Bollgard), устойчивый к насекомым-вредителям (гусеницам)./nginx/o/2020/06/18/13158381t1h6844.jpg)
Рисунок 4. Примеры трансгенных растений.
В марте 2005 года «Монсанто» приобрела крупнейшую семеноводческую компанию Seminis, специализирующуюся на производстве семян овощей и фруктов, в 2007–2008 годах поглотила 50 компаний — производителей семян по всему миру, после чего подверглась жесткой критике со стороны общества. В знак протеста против генетических манипуляций биотехнологического гиганта 25 мая 2013 года прошел «Марш против „Монсанто“», в котором приняли участие более 2 млн человек на шести континентах, в 52 странах мира.
В Центре «Биоинженерия» Российской академии наук на протяжении двух десятилетий ведутся работы по генетической инженерии растений — как для фундаментальных исследований, так и для сельского хозяйства. Были созданы генетически модифицированные сорта картофеля, устойчивые к колорадскому жуку, сорта свёклы, устойчивые к гербицидам и вирусам и др. Эти культуры могли бы решить ряд задач сельского хозяйства, но из-за до сих пор действующего в России законодательного ограничения они не выращиваются в открытом грунте. Само собой, этот запрет более чем странен, ведь ввоз ГМ-продукции в страну разрешен.
Само собой, этот запрет более чем странен, ведь ввоз ГМ-продукции в страну разрешен.
Второе направление представляет собой создание съедобных вакцин. В данном случае получают генно-модифицированное растение, синтезирующее вакцину. Такой привлекательной кажется идея: лежишь под пальмой, ешь банан, и ни одна тропическая зараза не берет!
Рисунок 5. Препарат трипсина, полученного в растениях (Sigma).
Концепцию производства вакцин в растениях впервые сформулировал Xью Мэйсон с соавторами [13]. Они предприняли попытку получения съедобной вакцины против вируса гепатита В на основе трансгенного табака. На следующем этапе был создан ГМ-картофель, продуцирующий поверхностный антиген вируса гепатита В. При скармливании мышам клубней такого картофеля наблюдали развитие специфического иммунного ответа. В 1999 г. были начаты эксперименты на добровольцах, и у людей, употреблявших в пищу сырые клубни картофеля, наблюдали формирование специфического иммунитета. Также были получены съедобные вакцины против вируса гепатита В на основе люпина и салата.
Также были получены съедобные вакцины против вируса гепатита В на основе люпина и салата.
Созданы трансгенные растения картофеля и табака, производящие белок нуклеокапсида вируса Норфолк, вызывающего у людей острый гастроэнтерит и устойчивого к спиртовым антисептикам. Появился и трансгенный картофель, синтезирующий полипептид LT-B — субъединицу термолабильного токсина Е. coli, вызывающего диарею. Однако, несмотря на активные исследования в этой области, коммерческих препаратов на сегодняшний день нет.
Третье направление связано с наработкой в растениях определенных продуктов, которые затем выделяются из растений и могут быть использованы, например, в качестве лекарственных препаратов. Биотехнологическими компаниями по всему миру уже создано большое количество ГМ-растений для получения белков, в том числе и медицинского назначения [14]. Среди компаний, деятельность которых основана на использовании трансгенных растений, следует отметить фирмы Рrotalix (Израиль), Medicago (Канада), LemnaGene (Франция), Planet Biotechnology (США), ProgyGene (Люксембург), Сhlorogen Inc. (США), SemBioSys Genetics (Канада) и Bayer AG (Германия). Из белков медицинского назначения у производителей наиболее популярны инсулин, лизоцим, лактоферрин, коллаген, липаза, антитела, вакцины и др. Многие из этих препаратов уже проходят клинические испытания. А вот трипсин уже можно купить у компании Sigma (рис. 5).
(США), SemBioSys Genetics (Канада) и Bayer AG (Германия). Из белков медицинского назначения у производителей наиболее популярны инсулин, лизоцим, лактоферрин, коллаген, липаза, антитела, вакцины и др. Многие из этих препаратов уже проходят клинические испытания. А вот трипсин уже можно купить у компании Sigma (рис. 5).
При наработке в растительных клетках продуктов медицинского назначения тоже используют метод агробактериальной трансформации, обеспечивающей транзиентную экспрессию генов на высоком уровне. Очевидными преимуществами этих систем являются простота манипуляций, скорость, низкая стоимость и высокий выход конечного продукта. Кроме того, в данном случае возможен синтез сложных белков, состоящих из нескольких субъединиц. Этот способ позволяет получать в течение нескольких дней белок в больших количествах (до нескольких граммов белка на килограмм массы растения). Выход продукта начинается уже через три часа (!) после проникновения агробактерий в клетку и переноса ДНК, а экспрессия сохраняется до 10 дней. Максимум наработки определяется для каждого белка индивидуально, но в среднем это 3–4 суток. Суммарно на получение белков в растениях уходит 2–3 недели (рис. 6).
Максимум наработки определяется для каждого белка индивидуально, но в среднем это 3–4 суток. Суммарно на получение белков в растениях уходит 2–3 недели (рис. 6).
Рисунок 6. Принципиальная схема экспрессии генов целевых белков в растениях. Весь процесс получения белка занимает 2–3 недели.
В растениях уже нарабатываются вакцины от вирусов папилломы человека, гепатита В [15], гриппа, папилломы крупного рогатого скота [16], африканской катаральной лихорадки, герпеса рогатого скота [17], ящура [18] и др.
В Центре «Биоинженерия» также ведутся работы по экспрессии терапевтических белков в растениях. Так, в клетках Nicotiana benthamiana (вид табака) были произведены вакцинные препараты против вируса гриппа [19, 20]. Основой препарата служит высококонсервативный вирусный белок M2, который присоединен к белку-носителю для увеличения иммуногенности. Носителем может быть кóровый белок вируса гепатита В или бактериальный флагеллин. В случае флагеллина вакцинный препарат применяют интраназально, что является явным преимуществом. А использование высококонсервативной последовательности белка M2 делает вакцину универсальной, что исключает необходимость изготовления каждый год всё новых и новых ее вариантов. Эти вакцинные препараты показали хорошие результаты по иммуногенности и протективности в экспериментах с лабораторными животными; следующим этапом должно стать клиническое тестирование.
А использование высококонсервативной последовательности белка M2 делает вакцину универсальной, что исключает необходимость изготовления каждый год всё новых и новых ее вариантов. Эти вакцинные препараты показали хорошие результаты по иммуногенности и протективности в экспериментах с лабораторными животными; следующим этапом должно стать клиническое тестирование.
Об успехах в мире
Персонифицированная терапевтическая вакцина для лечения лимфомы, полученная с помощью транзиентной экспрессии в растении Nicotiana benthamiana, уже прошла I и II фазы клинических испытаний [21]. На данный момент (2015 год) ожидается старт III фазы. Растительная вакцина против пандемического гриппа H5N1 проходит II фазу клинических испытаний, результаты будут опубликованы в июне 2015 г. [22, 23]. Вакцина была разработана компанией Medicago. Стандартный процесс получения этой компанией вакцинных белков в растениях показан на видео.
youtube.com/embed/lAk_HkFi9-s»/>
Клинические испытания вакцинных препаратов занимают продолжительное время (около 10 лет). Невольно возникает вопрос с вакциной от гриппа, так как каждый год появляются новые штаммы, и будет ли прошедшая клинические испытания вакцина актуальной? Здесь большее значение имеет технология получения препарата. Новый тип вакцины проходит полный цикл клинических испытаний, а затем уже по отработанной методике может быть получена вакцина с учетом циркулирующих штаммов вируса. Так, сейчас сезонные профилактические прививки от гриппа получают в куриных яйцах, и такие вакцины уже не проходят клинических испытаний. Как будут обстоять дела с производством в растениях рекомбинантных вакцин для массового применения, покажет время.
* * *
Подводя итог, можно сказать, что растения дали возможность получения жизненно важных белков методами биотехнологии. Человек научился брать от природы всё лучшее и избегать худшего. Как Уильям Шекспир в «Ромео и Джульетте» написал про растение:
В его цветах — целебный аромат,
А в листьях и корнях — сильнейший яд.
Так и человечество научилось брать целебный аромат, но не смертельный яд у растений. У растений-биофабрик — большое будущее!
Работа выполнена при поддержке гранта Президента Российской Федерации для государственной поддержки ведущих научных школ РФ НШ-6150.2014.4.
- Прионы: исследования таинственных молекул продолжаются;
- Fischer R., Schilberg S., Helliwig S., Twyman R.M., Drossard J. (2012). GMP issues for recombinant plant-derived pharmaceutical proteins. Biotechnol. Adv. 30, 434–439;
- Martinez C.A., Guilietti A.M., Talou R. (2012). Research advances in plant-made flavivirus antigens. Biotechnol. Adv. 30, 1493–505;
- Молекулярное клонирование, или как засунуть в клетку чужеродный генетический материал;
- А не замахнуться ли нам на… изменение генома?;
- Двухцепочечная РНК защищает трансгенные растения только от нежелательных насекомых;
- Sourrouille C.
 , Marshall B., Lienard D., Faye L. (2009). From Neanderthal to nanobiotech: from plant potions to pharming with plant factories. Methods Mol. Biol. 483, 1–23;
, Marshall B., Lienard D., Faye L. (2009). From Neanderthal to nanobiotech: from plant potions to pharming with plant factories. Methods Mol. Biol. 483, 1–23; - Rybiski E.P. (2008). Plant-produced vaccines: promise and reality. Drug Discov. Today. 14, 16–24;
- Yusibov V., Rabindran S. (2008). Recent progress in the development of plant derived vaccines. Expert Rev. Vaccines. 7, 1173–1183;
- Трансгенные растения — спасители планеты или бомбы замедленного действия?;
- Лекарству от голода — средство от засухи;
- Готовим ГМ-рис вместе;
- Mason H.S., Lam D.M., Arntzen C.J. (1992). Expression of hepatitis B surface antigen in transgenic plants. Proc. Natl. Acad. Sci. USA. 89, 11745–11749;
- Paul M., Ma J.K-C. (2011). Plant-made pharmaceuticals: Leading products and production platforms.
 Biotechnol. Appl. Biochem. 58, 58–67;
Biotechnol. Appl. Biochem. 58, 58–67; - Thuenemann E.C., Lenzi P., Love A.J., Taliansky M., Becares M., Zuniga S. et al. (2013). The use of transient expression systems for the rapid production of viruslike particles in plants. Curr. Pharm. Des. 19, 5564–5573;
- Love A., Chapman S., Matic S., Noris E., Lomonosoff G., Taliansky M. (2012). In planta production of a candidate vaccine against bovine papillomavirus type 1. Planta. 236, 1305–1313;
- Pérez Filgueira D.M., Zamorano P.I., Domínguez M.G., Taboga O., Del Médico Zajac M.P., Puntel M. et al. (2003). Bovine herpes virus gD protein produced in plants using a recombinant tobacco mosaic virus (TMV) vector possesses authentic antigenicity. Vaccine. 21, 4201–4209;
- Wigdorovitz A., Pérez Filgueira D.M., Robertson N., Carrillo C., Sadir A.M., Morris T.
 J., Borca M.V. (1999). Protection of mice against challenge with foot and mouth disease virus (FMDV) by immunization with foliar extracts from plants infected with recombinant tobacco mosaic virus expressing the FMDV structural protein. Virology. 264, 85–91;
J., Borca M.V. (1999). Protection of mice against challenge with foot and mouth disease virus (FMDV) by immunization with foliar extracts from plants infected with recombinant tobacco mosaic virus expressing the FMDV structural protein. Virology. 264, 85–91; - Равин Н.В., Котляров Р.Ю., Марданова Е.С., Куприянов В.В., Мигунов А.И., Степанова Л.А. и др. (2012). Продукция в растениях рекомбинантной противогриппозной вакцины на основе вирусоподобных HBc-частиц, несущих внеклеточный домен М2-белка. Биохимия. 77, 33–40;
- Mardanova E.S., Kotlyarov R.Y., Kuprianov V.V., Stepanova L.A., Tsybalova L.M., Lomonosoff G., Ravin N.V. (2015). Rapid high-yield expression of a candidate influenza vaccine based on M2 protein linked to flagellin in plants using viral vectors. BMC Biotechnology. В печати;
- McCormick A.A., Reddy S., Reinl S.J., Cameron T.I., Czerwinkski D.K.
 , Vojdani F. et al. (2008). Plant-produced idiotype vaccines for the treatment of non-Hodgkin’s lymphoma: safety and immunogenicity in a Phase I clinical study. Proc. Natl. Acad. Sci. USA. 105, 10131–10136;
, Vojdani F. et al. (2008). Plant-produced idiotype vaccines for the treatment of non-Hodgkin’s lymphoma: safety and immunogenicity in a Phase I clinical study. Proc. Natl. Acad. Sci. USA. 105, 10131–10136; - D’Aoust M.A., Couture M.M., Charland N., Trépanier S., Landry N., Ors F., Vézina L.P. (2010). The production of hemagglutinin-based virus-like particles in plants: a rapid, efficient and safe response to pandemic influenza. Plant Biotechnol. J. 8, 607–619;
- Sheldon E., Seiden D.J. (2014). Immunogenicity, safety and tolerability of a plant-derived seasonal virus-like-particle quadrivalent influenza vaccine in adults. ClinicalTrials.gov. (сервис Национальных институтов здоровья США)..
Белок из растений — Vegan lifestyle — LiveJournal
Исследователи, изучающие питание, более тридцати лет назад заявили, что растительная пища может обеспечить нас достаточным количеством белка (1). Тем не менее, “откуда вы берёте белок?” это тот вопрос, который большинство веганов слышало гораздо чаще, чем они рассчитывали. Многие вопросы о белке в растительных диетах возникают из неразберихи вокруг “полноценных” белков.
Тем не менее, “откуда вы берёте белок?” это тот вопрос, который большинство веганов слышало гораздо чаще, чем они рассчитывали. Многие вопросы о белке в растительных диетах возникают из неразберихи вокруг “полноценных” белков.Полноценные и неполноценные белки
Белки в организме человека, как правило, имеют постоянное соотношение незаменимых аминокислот. Так как процент незаменимых аминокислот в продуктах животного происхождения и соевых бобах примерно соответствует ему в человеческом теле, белки этих продуктов считаются “полноценными”. Растительная пища, такая как злаки, бобовые и орехи содержат низкий процент, по крайней мере, одной незаменимой аминокислоты, что делает их “неполноценными”. Например, бобовые (кроме соевых бобов) имеют низкое содержание незаменимой аминокислоты метионина, а злаки, низкое содержание лизина. Но, когда злаки и бобовые употребляются вместе, их аминокислотные профили дополняют друг друга и производят смесь, которая является “полноценной”, и потому, хорошо подходящей для потребностей организма.
Но, когда злаки и бобовые употребляются вместе, их аминокислотные профили дополняют друг друга и производят смесь, которая является “полноценной”, и потому, хорошо подходящей для потребностей организма.
В начале 1970-х, идея о том, что вегетарианское питание должно содержать эти конкретные взаимодополняющие пары популяризировала Франс Мур Лаппе в своей книге «Диета для маленькой планеты» (2). Как мы сегодня знаем, теория о том, что происходит, когда белковые продукты сочетаются таким образом, не была неправильной; она просто оказалась ненужной. Новейшие исследования показали, что организм хранит запасы незаменимых аминокислот (3). Нам необходимо пополнять запасы этого хранилища всеми аминокислотами, поэтому так важно есть разнообразную растительную пищу. Но старая идея о том, что некоторые комбинации растительных продуктов — взаимодополняющие пары, должны потребляться вместе, неправдива.
Хотя фрукты содержат очень мало белка и масел, все другие растительные продукты содержат белок. Существует расхожее заблуждение, что в растительных продуктах полностью отсутствует одна или несколько аминокислот. Это неправда. Все растительные источники белка содержат хотя бы немного каждой незаменимой аминокислоты. На самом деле, Вы могли бы получить достаточное количество белка и все незаменимые аминокислоты, употребляя в пищу только один тип пищи, к примеру, фасоль пинто. Вам следовало бы съедать её довольно много — около четырёх чашек в день. Это непрактично, отчасти потому, что скучно, но и потому, что вся эта фасоль, вероятно, вытесняла бы продукты, необходимые для удовлетворения других пищевых потребностей. Так что употребление различных источников белка приносит больше пользы в диетическом смысле.
Существует расхожее заблуждение, что в растительных продуктах полностью отсутствует одна или несколько аминокислот. Это неправда. Все растительные источники белка содержат хотя бы немного каждой незаменимой аминокислоты. На самом деле, Вы могли бы получить достаточное количество белка и все незаменимые аминокислоты, употребляя в пищу только один тип пищи, к примеру, фасоль пинто. Вам следовало бы съедать её довольно много — около четырёх чашек в день. Это непрактично, отчасти потому, что скучно, но и потому, что вся эта фасоль, вероятно, вытесняла бы продукты, необходимые для удовлетворения других пищевых потребностей. Так что употребление различных источников белка приносит больше пользы в диетическом смысле.
Рекомендуемая норма потребления белка для веганов
Потребности в белке рассчитываются на основе здорового (или “идеального”) веса тела, то есть веса человека со здоровым количеством жира в организме. Ученые используют метрическую систему, поэтому американские потребности в белке определяются с помощью здорового веса в килограммах.
РСН белка для взрослых составляет 0,8 грамм белка на килограмм идеальной массы тела, но наряду с большинством другими веганами-диетологами, мы рекомендуем веганам употреблять немного больше белка. Это потому, что растительные белки не усваиваются так же хорошо как животные белки (4). Так как обработка и приготовление пищи зачастую улучшает усвояемость белка, это может быть не так актуально для веганов, употребляющих много таких продуктов как тофу или вегетарианское мясо из обработанного соевого белка. Для тех, кто полагается на цельные продукты, такие как бобовые, орехи и злаки, в качестве основного источника белка, фактор усвояемости играет роль.
Это небольшая разница, но веганам следует стремиться употреблять от 0,9 грамм белка на килограмм массы тела. Для удобства расчета, это означает примерно 0,4 грамма белка на фунт здорового веса тела. Так веганам, здоровый вес которых составляет 150 фунтов необходимо 60 граммов белка (150 х 0,4) в день.
Так как потребности в белке значительно различаются между людьми, а РСН предназначена для покрытия потребностей 97 процентов населения, она несколько больше потребностей многих людей. Поскольку нет какого-либо способа узнать попадаете ли Вы в диапазон необходимого Вам количества белка, и потому что последние исследования показывают, что рекомендованные нормы потребления белка могут быть слишком низкими (5), хорошо бы не рисковать и стремиться к РСН.
Поскольку нет какого-либо способа узнать попадаете ли Вы в диапазон необходимого Вам количества белка, и потому что последние исследования показывают, что рекомендованные нормы потребления белка могут быть слишком низкими (5), хорошо бы не рисковать и стремиться к РСН.
Для детей и подростков, мы хотели бы использовать РСН, направленные на потребности различных возрастных групп и рассчитанные специально для веганов.
Рекомендации по употреблению белка для молодых веганов
Возраст (годы) | Девочки (грамм/день) | Мальчики (грамм/день) |
|---|---|---|
1–2 | 18–19 | 18–19 |
2–3 | 18–21 | 18–21 |
4–6 | 26–28 | 26–28 |
7–10 | 31–34 | 31–34 |
11–14 | 51–55 | 50–54 |
15–18 | 50–55 | 66–73 |
Удовлетворение потребностей в белке на веганской диете: Значение бобовых
 19 показывает, что многие растительные продукты являются хорошим источником белка, бобовые особенно богаты белком. Бобовые включают фасоль, горох, чечевицу, соевые продукты (например, тофу, соевое молоко и вегетарианское мясо) и арахис. (Большинство людей думает, что арахис это орех, но это бобовое растение, а с точки зрения питания, он имеет больше общего с фасолью пинто и чечевицей, чем с грецкими орехами и орехами пекан.) Наше руководство по питанию рекомендует употреблять как минимум три-четыре порции этих продуктов в день. Порция довольно скромная: ½ стакана вареной фасоли, ½ чашки тофу или темпе, одна унция вегетарианского бургера, одна чашка соевого молока или две столовые ложки арахисовой пасты. Спланировать меню, включающее эти продукты несложно, и мы дадим вам несколько советов для этого в главе 7.
19 показывает, что многие растительные продукты являются хорошим источником белка, бобовые особенно богаты белком. Бобовые включают фасоль, горох, чечевицу, соевые продукты (например, тофу, соевое молоко и вегетарианское мясо) и арахис. (Большинство людей думает, что арахис это орех, но это бобовое растение, а с точки зрения питания, он имеет больше общего с фасолью пинто и чечевицей, чем с грецкими орехами и орехами пекан.) Наше руководство по питанию рекомендует употреблять как минимум три-четыре порции этих продуктов в день. Порция довольно скромная: ½ стакана вареной фасоли, ½ чашки тофу или темпе, одна унция вегетарианского бургера, одна чашка соевого молока или две столовые ложки арахисовой пасты. Спланировать меню, включающее эти продукты несложно, и мы дадим вам несколько советов для этого в главе 7.В дополнение к тому, что они богаты белком, эти продукты единственные хорошие растительные источники — за немногими исключениями — незаменимой аминокислоты лизин. Диета, которая получает большую часть белка из злаков, орехов и овощей, вероятно, будет содержать слишком мало лизина. И хотя некоторые популярные ресурсы предполагают, что очень низкое потребление белка — всего 5-6 процентов от общего количества калорий, может удовлетворить наши пищевые потребности, в действительности трудно получить достаточное количество лизина на диете с низкой полнотой белка.
И хотя некоторые популярные ресурсы предполагают, что очень низкое потребление белка — всего 5-6 процентов от общего количества калорий, может удовлетворить наши пищевые потребности, в действительности трудно получить достаточное количество лизина на диете с низкой полнотой белка.
Вы можете получить примерное представление о необходимом Вам количестве лизина, умножив свой вес (в фунтах) на 19. Этот расчёт учитывает немного более низкую усвояемость белка из цельной растительной пищи. Например, человеку весом 140 фунтов необходимо 2660 мг лизина в день.Таблица на стр. 21 показывает, что лучшими источниками лизина являются бобовые, киноа, фисташки, и кешью.
Если Вы будете следовать нашим рекомендациям и употреблять как минимум три-четыре порции бобовых в день, Вы удовлетворите свои потребности в лизине. Это не означает, что бобы, арахис и соевые продукты абсолютно необходимы в веганской диете. Хотя без них трудно удовлетворить потребности в белке и лизине, это возможно, и мы дадим представление об этом в главе 7, когда рассмотрим принципы планирования рациона для веганов.
Содержание лизина в некоторых растительных продуктах
Продукт | Количество лизина (в миллиграммах) |
|---|---|
Белковые порошки | |
Белковый порошок Naturade, без сои, ⅓ чашки | 1,455 |
Белковый порошок Naturade, соевый, ⅓ чашки | 1,552 |
Соевые продукты | |
Зелёные соевые бобы, ½ чашки | 577.5 |
Соевое молоко, 1 чашка | 439 |
Тофу, твёрдый, ½ чашки | 582 |
Бобовые | |
Чёрная фасоль, ½ чашки | 523 |
Турецкий горох (нут), ½ чашки | 486. |
Фасоль кинди, ½ чашки | 526.5 |
Чечевица, ½ чашки | 623.5 |
Арахисовая паста, 2 столовые ложки | 290 |
Арахис, ¼ чашки | 310 |
Пережаренная фасоль кинди, ½ чашки | 475 |
Орехи и семечки | |
Миндаль, ¼ чашки | 205 |
Кешью, ¼ чашки | 280 |
Пекан, ¼ чашки | 78 |
Фисташки, ¼ чашки | 367 |
Грецкий орех, ¼ чашки | 124 |
Злаки | |
Хлеб, белый, 1 кусок | 56 |
Хлеб, цельнозерновой, 1 кусок | 85 |
Овсяные хлопья, ½ чашки, приготовленные | 158 |
Картофель (белый), средний, ½ часть | 131. |
Киноа, ½ чашки | 221 |
Рис, коричневый, ½ чашки | 86 |
Рис, белый, ½ чашки | 80 |
Спагетти, белые, ½ чашки | 63.5 |
Спагетти, цельнозерновые, ½ чашки | 82.5 |
Пшеничная тортилья, 1 средняя | 98 |
Овощи | |
Брокколи, ½ чашки | 117 |
Кукуруза, ½ чашки | 116 |
Римский салат, сырой, нарезанный, 1 чашка | 58 |
Шпинат, приготовленный, ½ чашки | 164 |
Фрукты | |
Банан, 1 средний | 59 |
Апельсин, 1 средний | 62 |
Клубника, целая, 1 чашка | 37 |
Растительный белок и блюда, которые им богаты
Довольно просто составить блюдо, содержащие значительное количество белка.
 Каждое из этих блюд содержит, по меньшей мере, 20 граммов белка.
Каждое из этих блюд содержит, по меньшей мере, 20 граммов белка.Лёгкий овсянный завтрак
- 1 стакан овсянных хлопьев с ½ стакана соевого молока
- 1 ломтик цельнозернового хлеба с 2 столовыми ложками миндальной пасты
Всего белка: 20.5 грамм
Индонезийский темпе с арахисовым соусом
- ¼ чашки кунжутного соуса тахини
- 1½ чашки свареной на пару брокколи
Всего белка: 35 грамм
Фасолевый тако-ужин
- 2 ракушки тако
- ½ чашки пережаренной фасоли
- ¼ стакана вегетарианского фарша, приготовленного в томатном соусе
- Рубленные томаты и салат-латук
- 1 чашка сваренного на пару шпината
Всего белка: 20 грамм
Паста с овощным соусом
- 1 стакан пасты
- 2 столовые ложки кедровых орехов
- 1 чашка нарезанной брокколи
- ½ стакана обжаренных платинок кайенского перца
Всего белка: 23 грамма
Ланч «на ходу»
- Быстрорастворимый чечевичный суп с 2-мя столовыми ложками тыквенных семечек
- 1 ломтик цельнозернового хлеба с пюре из авокадо
Всего белка: 21 грамм
Недостаточное потребление
Выраженный дефицит белка большая редкость среди американцев и встречается в других частях света, там, где у людей нет достаточного количества пищи. Многие сторонники веганства отмечают, что люди не попадают в больницы из-за недостатка белка. Это правда, что в странах, где пища имеется в изобилии, острого дефицита белка не возникает. Но диеты, имеющие критическое содержание белка — не совсем отсутствующие, но и не вполне оптимальное — могут привести к потере мышечной массы, слабому здоровью костей, и нарушению иммунитета. А эти виды расстройств встречаются в Соединенных Штатах.
Многие сторонники веганства отмечают, что люди не попадают в больницы из-за недостатка белка. Это правда, что в странах, где пища имеется в изобилии, острого дефицита белка не возникает. Но диеты, имеющие критическое содержание белка — не совсем отсутствующие, но и не вполне оптимальное — могут привести к потере мышечной массы, слабому здоровью костей, и нарушению иммунитета. А эти виды расстройств встречаются в Соединенных Штатах.
Нам хотелось бы сказать, что веганам не нужно беспокоиться о белке, но это несовсем верно. Есть некоторые ситуации, когда веганы могут не удовлетворить свои потребности в белке.
Веганская диета с низким содержанием продуктов, богатых белком, таких как бобовых, вероятно, будет иметь низкое содержание белка. А поскольку низкокалорийные диеты увеличивают потребности в белке, люди, которые соблюдают диету или просто не едят достаточно пищи по другим причинам (например, хронические заболевания), возможно, потребуется увеличить потребление богатых белком продуктов, например, бобовых или соевых продуктов.
Очевидно, веганская джанк-фуд диета, основанная на картофельных чипсах, картофеле фри и прохладительных напитках, может иметь слишком низкое содержание белка (и слишком низкое содержание почти всего остального, необходимого вам для того, чтобы быть здоровым).
Экстремальные версии веганских диет, такие как сыроедение или фрукторианство, зачастую содержат мало (или вообще не содержат) богатых белком растительных продуктов, вроде бобовых и соевых продуктов, что может привести к критическому потреблению белка. Это одна из причин, почему эти типы диет не рекомендуются для детей.
Получают ли веганы достаточно триптофана?
Одно из распространенных мнений, часто высказываемых критиками веганской диеты, полагает, что растительная пища не содержит достаточного количества триптофана. Это незаменимая аминокислота необходима для производства нейромедиатора серотонина, а низкий уровень серотонина связан с депрессией. Мясо содержит больше триптофана, чем растения, но правильно сбалансированная веганская диета едва ли ни гарантированно предоставит более чем достаточно этой аминокислоты. Совет по продовольствию и питанию института медицины рекомендует употреблять 5 мг триптофана на каждый килограмм нормального веса тела. Учитывая особенность усвоения растительного белка, РСН для веганов составляет 5,5 мг на килограмм массы тела, или 2,5 мг триптофана за фунт.
Совет по продовольствию и питанию института медицины рекомендует употреблять 5 мг триптофана на каждый килограмм нормального веса тела. Учитывая особенность усвоения растительного белка, РСН для веганов составляет 5,5 мг на килограмм массы тела, или 2,5 мг триптофана за фунт.
Например, вегану, который весит 130 фунтов следует употреблять 325 мг триптофана, что легко может быть получено на веганской диете. Рацион, состоящий из одной чашки черной фасоли, ½ стакана тофу и одной чашки коричневого риса даст почти 400 миллиграмм триптофана.
Известно, что употребление продуктов, имеющих очень высокое содержание белка, например, мяса, не обязательно увеличивает количество триптофана в мозге. Это потому, что высокие уровни других аминокислот в этих продуктах блокируют поглощение триптофана из крови в мозг. Употребление в пищу таких продуктов, как бобовые, содержащих как белки и так и углеводы может даже увеличить прохождение триптофана в мозг (6).
Содержание триптофана в некоторых растительных продуктах
Продукт | Триптофан (в миллиграммах) |
|---|---|
Тофу, ½ чашки | 155 |
Овсяные хлопья, ½ чашки | 118 |
Соевое молоко, 1 стакан | 105 |
Чёрная фасоль, отварная, ½ чашки | 90 |
Арахисовая паста, 2 столовые ложки | 78 |
Нут, отварной, ½ чашки | 70 |
Киноа, отварная, ½ чашки | 29 |
Брокколи, отварная, ½ чашки | 24 |
Советы для удовлетворения потребностей веганов в белке
- Потребляйте адекватное число калорий для поддержания здоровой веса.
 Если потребление калорий является низким, поскольку Вы сидите на диете или по любой другой причине, Вам, возможно, потребуется добавить несколько дополнительных богатых белком продуктов питания в ваше меню.
Если потребление калорий является низким, поскольку Вы сидите на диете или по любой другой причине, Вам, возможно, потребуется добавить несколько дополнительных богатых белком продуктов питания в ваше меню.
- Ешьте разнообразную растительную пищу каждый день.
- Следуйте инструкциям в руководстве о питании из главы 7 и стремитесь иметь как минимум три-четыре порции бобовых в вашем ежедневном меню. Порция, это ½ стакана вареной фасоли, ½ чашки тофу или темпе, ¼ чашки арахиса, одна чашка соевого молока или 2 столовые ложки арахисовой пасты.
- Если фасоль доставляет Вам дискомфорт из-за газообразования, ешьте больше чечевицы и гороха (они менее способствуют газообразованию) и включите в свой рацион вегетарианское мясо, тофу, темпе.
- Если в Ваш рацион входит растительное молоко, старайтесь хотя бы иногда пить соевое. Молоко из миндаля, конопли, и риса имеет низкое содержание белка.
Список литературы
- V.
 R. Young and P. L. Pellett, “Plant Proteins in Relation to Human Protein and Amino Acid Nutrition,” American Journal of Clinical Nutrition 59, suppl. no. 5 (1994): S1203–S1212.
R. Young and P. L. Pellett, “Plant Proteins in Relation to Human Protein and Amino Acid Nutrition,” American Journal of Clinical Nutrition 59, suppl. no. 5 (1994): S1203–S1212. - F. M. Lappé, Diet for a Small Planet (New York: Ballantine, 1971), 72–94.
- M. F. Fuller and P. J. Reeds, “Nitrogen Cycling in the Gut,” Annual Review of Nutrition 18 (1998): 385–411.
- G. Sarwar, “Digestibility of Protein and Bioavailability of Amino Acids in Foods: Effects on Protein Quality Assessment,” World Review of Nutrition and Dietetics 54 (1987): 26–70.
- R. Elango, M. A. Humayun, R. O. Ball, and P. B. Pencharz, “Evidence that Protein Requirements Have Been Significantly Underestimated,” Current Opinion in Clinical Nutrition & Metabolic Care 13, no. 1 (2010): 52–57.
- C. Hudson, S. Hudson, and J. MacKenzie, “Protein-Source Tryptophan as an Efficacious Treatment for Social Anxiety Disorder: A Pilot Study,” Canadian Journal of Physiology and Pharmacology 85, no. 9 (2007): 928–32.

_________
Источник: CHAPTER 2 — PROTEIN FROM PLANTS, Vegan for Life: Everything You Need to Know to Be Healthy and Fit on a Plant-Based Diet (2011), Jack Norris, RD & Virginia Messina, MPH, RD.
Защитные белки растений. PR-белки » Строительный онлайн-ресурс
18.01.2014 Белки, связанные с патогенезом (PR-белки), образуются в растениях в ответ на заражение грибными, бактериальными, вирусными болезнями, а также в ответ на обработку некоторыми химикатами. Все эти белки обладают широким антигрибным спектром действия. Среди них большой интерес представляют следующие.
— Ферменты β-1,3-глюканазы и хитиназы (группы PR-2 и PR-3 соответственно), разлагающие полисахариды β-1,3-глюкан и хитин. Поскольку глюканы содержатся в клеточных стенках растений, наличие у них глюканаз как регуляторов процессов синтеза и деградации элементов клеточной стенки неудивительно. Но хитина у растений нет, а это означает, что хитиназа несет главным образом защитные функции. Синтез этих ферментов в ответ на заражение также свидетельствует об их связях с защитными реакциями. Хитин и β-глюкан — основные компоненты клеточных оболочек грибов, из хитина построены стилеты сосущих насекомых и нематод. В настоящее время гены, ответственные за синтез хитиназы и β-глюканазы, широко используются в генно-инженерных конструкциях с целью создания трансгенных растений, устойчивых к болезням и вредителям.
Синтез этих ферментов в ответ на заражение также свидетельствует об их связях с защитными реакциями. Хитин и β-глюкан — основные компоненты клеточных оболочек грибов, из хитина построены стилеты сосущих насекомых и нематод. В настоящее время гены, ответственные за синтез хитиназы и β-глюканазы, широко используются в генно-инженерных конструкциях с целью создания трансгенных растений, устойчивых к болезням и вредителям.
— Белки, связывающие хитин (группа PR-4). Они относятся к большой группе связывающих хитин белков — лектинов.
— Тауматиноподобные белки (группа PR-5), которые имеют структурное сходство со сладким белком тауматином из южноафриканского кустарника Taumatococcus. Они вызывают лизис грибного мицелия вследствие связывания β-1,3-глюкана в клеточных стенках грибов (обладают β-1,3-глюканазной активностью), ингибируют осамилазу насекомых и человеческий трипсин (обладают свойствами ингибиторов ферментов).
Ингибиторы протеиназ. Ингибиторы протеиназ (ИП) — это белки, образующие комплексы с протеиназами и ингибирующие их каталитическую активность. Известно несколько классов ИП, отличающихся ингибированием разных типов протеиназ. Некоторые ИП накапливаются в незараженных растениях, синтез других индуцируется в ответ на заражение или повреждение насекомыми. ИП подавляют активность протеиназ, выделяемых в растение фитопатогенными грибами и насекомыми, и нарушают способность патогенов поглощать растительные белки, то есть снижают их пищевую активность. ИП не только выполняют защитные функции, они могут служить запасающими белками (накапливаются в покоящихся органах растений— семенах, клубнях) и регуляторами протеиназной активности самих растений.
Известно несколько классов ИП, отличающихся ингибированием разных типов протеиназ. Некоторые ИП накапливаются в незараженных растениях, синтез других индуцируется в ответ на заражение или повреждение насекомыми. ИП подавляют активность протеиназ, выделяемых в растение фитопатогенными грибами и насекомыми, и нарушают способность патогенов поглощать растительные белки, то есть снижают их пищевую активность. ИП не только выполняют защитные функции, они могут служить запасающими белками (накапливаются в покоящихся органах растений— семенах, клубнях) и регуляторами протеиназной активности самих растений.
Антивирусные белки. У многих растений (фитоляки, дурмана, табака и др.) обнаружены белки, ингибирующие вирусную инфекцию. Эти белки разделяют на две большие группы: эндогенные, присутствующие в клетках независимо от заражения, и индуцированные, возникающие при заражении вирусами. Первые ингибируют главным образом ранние фазы вирусной инфекции путем агрегации ингибиторного белка с вирионом и ингибирования репликации вирусных белков вследствие инактивации рибосом. Индуцированные антивирусные белки ингибируют репликацию вирусов. Некоторые из них имеют много общего с интерферонами человека (интерфероны ингибируют репликацию некоторых вирусов растений). Большинство антивирусных белков синтезируется в растении в очень низких концентрациях, что затрудняет их исследование.
Дефензины. Это низкомолекулярные (45…54 аминокислоты) белки, богатые цистеином. Дефензины продуцируются как защитные белки млекопитающими, насекомыми, грибами и растениями. Растительные дефензины могут вызывать морфологические изменения у восприимчивых видов грибов (морфогенные дефензины), ингибировать рост мицелия без морфологических изменений (неморфогенные дефензины), ингибировать осамилазу грибов. Они связываются с рецепторами на мембранах грибов и вызывают усиление потери К и поступления Са в клетки.
Другие защитные белки растений. Помимодефензинов факторами устойчивости к патогенам могут быть и другие низкомолекулярные антимикробные белки, богатые цистеином. Это белки, осуществляющие трансмембранный транспорт липидов, белки, подавляющие синтез белка на чужеродных рибосомах на стадии элонгации (RIP-белки), и богатые серой тионины, накапливающиеся в семенах и проростках растений. Последние взаимодействуют с мембранными фосфолипидами и вызывают образование пор в мембранах. Эти белки обнаружены в семенах, листьях, цветках и клубнях разных растений, часто накапливаются в клеточных стенках, осуществляя защитную функцию.
структура, функции и практическое применение – тема научной статьи по биологическим наукам читайте бесплатно текст научно-исследовательской работы в электронной библиотеке КиберЛенинка
УДК 577.1 12
Белки системы врожденного иммунитета растений, осуществляющие транспорт липидов: структура, функции и практическое применение
Е. И. Финкина, Д. Н. Мельникова, И. В. Богданов, Т. В. Овчинникова*
Институт биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова РАН,
117997, Москва, ул. Миклухо-Маклая, 16/10
*E-mail: [email protected]
Поступила в редакцию 05.08.2015
Принята к печати 18.12.2015
РЕФЕРАТ Среди множества молекулярных факторов системы врожденного иммунитета растений особый интерес представляют небольшие белки, осуществляющие транспорт липидов и обладающие широким спектром биологической активности. Эти белки называют липид-переносящими или липид-транспорти-рующими (ЛТБ). Можно выделить три основных аспекта, в контексте которых ЛТБ привлекают интерес исследователей. Первый из них — способность растительных ЛТБ связывать и переносить липиды, благодаря чему эти белки получили свое название и были объединены в один класс. Во-вторых, ЛТБ относятся к защитным белкам, являющихся факторами врожденного иммунитета растений. Кроме того, ЛТБ составляют один из наиболее клинически значимых классов растительных аллергенов. Цель настоящего обзора состоит в обобщении имеющихся данных о структуре, свойствах, функциях, механизмах действия и практическом применении ЛТБ для углубления понимания роли этих белков в физиологии растений и их значения в жизни человека.
КЛЮЧЕВЫЕ СЛОВА аллергены, антимикробная активность, защита растений, липид-транспортирующие белки растений, перекрестная реактивность, связывание и перенос липидов.
СПИСОК СОКРАЩЕНИЙ ЛТБ — липид-транспортирующие белки; ЖК — жирные кислоты; ФХ — фосфа-тидилхолины; ФИ — фосфатидилинозиты; ФГ — фосфатидилглицерины; PRP (Pathogenesis-Related Proteins) — белки, связанные с патогенезом; AMP (Antimicrobial Peptides) — антимикробные пептиды; PAMP (Pathogen Associated Molecular Patterns) — ассоциированные с патогенами молекулярные структуры; DAMP (Damage Associated Molecular Patterns) — молекулярные структуры, ассоциированные с повреждением; ГФИ-якорь — гликозилфосфатидилинозитный якорь; АФК — активные формы кислорода; SAR (Systemic Acquired Resistance) — системная приобретенная резистентность; HR (Hypersensitive Response) — гиперчувствительный ответ; АСИТ — аллерген-специфическая иммунотерапия.
ВВЕДЕНИЕ
Липиды и их производные принимают участие в самых разнообразных процессах, включая биогенез мембран, дифференцировку клеток, межклеточную и внутриклеточную передачу сигналов, образование водоотталкивающих и термоизоляционных покровов, защищающих растение от воздействия неблагоприятных факторов окружающей среды, а также выполняют запасающую и энергетическую функции. В клетках про- и эукариот важную роль в метаболизме липидов играют белки, осуществляющие их внутри- и внеклеточный транспорт. В растениях
обнаружено несколько классов белков, обладающих способностью связывать и транспортировать липиды и их производные: ацил-КоА-связывающие белки (Acyl-CoA-Binding Proteins), гликолипид-транс-портирующие белки (Glycolipid Transfer Proteins), стерин-переносящие белки (Sterol Carrier Proteins), гомологи основного пыльцевого аллергена березы Betula verrucosa, зарегистрированного в базе данных аллергенов IUIS под аббревиатурой Bet v 1, белки, связывающие жирные кислоты (Fatty Acid Binding Proteins), пуроиндолины (Puroindolines) и липид-транспортирующие белки (Lipid Transfer Proteins).
Сравнительная характеристика двух подклассов растительных ЛТБ
Характеристика ЛТБ1 ЛТБ2
Мг, кДа 9-10 6-7
Число аминокислотных остатков, а.о. 90-95 65-70
Консервативные а.о. С, G, Р, R, Y(F) C, Q, P, Y(F)
Мотив -С¥ХС™- X — гидрофильный а.о. (как правило, экспонирован на поверхности молекулы белка X — гидрофобный а.о. (чаще всего F), обращен внутрь молекулы белка
Организация дисульфидных связей С:-С¥1 Сп-Сш С1¥-Сш1 С¥-Ста1 CI-CV С11-Сш CIV-CVI1 Cvl-cvm
Пространственная структура 4 а-спирали, фрагмент 310-спирали и неструктурированный С-концевой фрагмент 3 a-спирали и область, содержащая одиночные повороты спирали
Форма гидрофобной впадины Туннель с большим и малым входом, в его формировании принимают участие спирали Н1, Н2 и Н3, расположенные параллельно друг другу Трехгранный полый бокс, спирали h2 и h3 располагаются параллельно друг другу, а спираль h4 направлена под углом 90° относительно h3
Способность связывать стерины Нет Есть
Взаимодействующие с лигандом а.44 и Туг79 (нумерация для ЛТБ1 риса) Phe36, Tyr45 и Tyr48 (нумерация для ЛТБ2 риса)
Сигнальный пептид, а.о. 21-27 27-35
Локализация Органы, покрытые слоем кутина (листья, стебли, цветки) Органы, покрытые слоем суберина (подземные органы)
Одна из предполагаемых функций Биосинтез кутина Биосинтез суберина
Активация иммунного ответа Элиситоры в комплексе с жасмоновой кислотой Элиситоры в комплексе со стерином
Аллергены, зарегистрированные в ШК ЛТБ1 42 растений (не считая изоаллерге-нов и вариантов) Sola l 6 томата, Api g 6 сельдерея, Ara h 16 арахиса
Сопоставление аминокислотных последовательностей белков перечисленных классов выявило отсутствие значительной структурной гомологии между ними. Эти белки имеют внутри- или внеклеточную локализацию, относительно небольшую молекулярную массу (7-30 кДа), высокое значение изоэлек-трической точки (р1 ~9-11) и компактную структуру, стабилизированную дисульфидными связями. Для пространственной структуры белков, осуществляющих транспорт липидов, характерно наличие гидрофобной впадины, внутри которой располагается сайт связывания лигандов. Эти белки обратимо связывают липиды и доставляют их к месту назначения. Белки некоторых из перечисленных классов имеют высокоспецифичные лиганды, другие белки связывают и переносят широкий спектр липидов.
К функционально наиболее значимым классам белков растений, связывающих и переносящих липи-ды, относятся ЛТБ. Эти белки были открыты в 1970 г. и первоначально названы фосфолипид-обмениваю-щими белками [1], а позднее переименованы в фос-фолипид-транспортирующие белки [2]. Дальнейшие исследования показали, что лигандами данных белков могут быть не только фосфолипиды, но и другие гидрофобные молекулы, в связи с чем ЛТБ получили
свое нынешнее название — неспецифические липид-транспортирующие белки [3].
СТРУКТУРНАЯ ХАРАКТЕРИСТИКА ЛТБ РАСТЕНИЙ
На основании особенностей структурной организации растительные ЛТБ подразделяются на два подкласса: ЛТБ1 с молекулярной массой 9-10 кДа и ЛТБ2 с молекулярной массой около 7 кДа (таблица). Гомология аминокислотных последовательностей у представителей двух подклассов не превышает 30% (рис. 1). Все ЛТБ являются основными белками (р1 ~9-10). Подавляющее большинство ЛТБ содержат восемь консервативных остатков цистеина (..С1…СП…СШС1У… С¥ХС¥1…С¥П…С¥Ш..), образующих четыре дисульфид-ные связи, которые стабилизируют структуру и тем самым обуславливают устойчивость ЛТБ к действию высоких температур и протеолитических ферментов. Некоторые представители белков этого класса сохраняют нативную конформацию и биологическую активность даже после прогревания при температуре около 100°С [4]. Пространственная структура ЛТБ представлена в основном а-спиральными участками.—
10 20 30 40 50 60 70 80 90
CAA69949
— LTCGQVTGAIAP CLGYIATAGSVPVPLT-CCHGVaGLHHAARTTI I1RRTACHCLKQTAHAIAD — LH LH — AAAGLP AKC G- -VHIPÏKI5 PSTDCHKW———AEG79730
VLTCGOVTGALAP CLÜÍVbE SQVHVPVPLT- С CMWUGLHH AAETTLDKRTAC GCLKÜTAMAVTG -LH LH — AAAGLP ARCG— VU IPYKI £ PTT DCN KW————P27631
— -TCGdVSSAIAÍ CI fYUlAGG—PIPV£- С CHGVRS LKAAAHTTP DRQTAC HCLKQSAGSI PH — LH PH — HAVGLPRACG—VSIPYKÏSISTDCSKV————-BAH03575
P85894
-VTCGÛWGAVAP CLGYLRHGG—TPPQP-С CTGVKG LR» SSETTS DRÍ7TIС MCLKSASS SYRG -‘VS GH-YASS LP GKCG- — VWL PYKISPSTDCHEIQ————ABK96813
AI SCGäVASAI AP CI SYASGQG- -SGPÊAGC CSGVUS LBH AAETTADRRAAC MC LKKAAAGVS G — LH AO- HAAS IPSHCÖ—VSIPYTISTSTDCS KVK————P19656
Q42952 P07597 P24296
ALSCGTVSGyVAE CI GYLAQGAP -ALPRA- С CSGVTSLNH LSRTTODRa 9K®dVGSAHArET — LH SA- RAAGLP KACG- — VHIPYKIS KTT HCH SVK————ABM69132
P27056
AAA33876
P82007
AAX35807
CAB43522
QHICPKVHHIVTP CVAYGLGRA—-PI APC CRA1H DLR-FVMTRH LRKAAC KCL VGWMEH PG-LRRH PRFQ MIP EDCSUtT FVRPFWWRPRIBCGRIHLTDKLIYLDAEE Q41258
AAV40850
AAA iHt iHHt it 1 AMA
h2
h3
ш-шт-
10 20 30 40 50 60
O.6Н) [10] риса. Звездочками отмечены остатки, составляющие конформационные эпитопы Рги р 3 (GenBank: AAV40850) [98]
Б
тенциальный сайт связывания гидрофобных и амфи-фильных молекул, таких, как липиды.
ЛТБ1 состоят из 90-95 аминокислотных остатков и имеют следующий порядок образования дисульфидных связей: CLCVI, Сп-Сш, CIV-CVI1, CV-CVI11 (рис. 1А, 2А). Фрагмент -CVXCVI- в структуре ЛТБ1 содержит гидрофильную аминокислоту (чаще всего аспара-гин), боковая группа которой экспонирована на поверхности молекулы. Пространственная структура этих белков сформирована четырьмя а-спиралями, фрагментом 310-спирали и протяженным неструктурированным С-концевым участком (рис. 2А) [5, 6]. В структуре некоторых ЛТБ1, например, выделенных из кукурузы (Zea mays) и табака (Nicotiana tabacum), спирали Н1 и Н4 разделены остатками пролина на два фрагмента (Н1а и Н1Ь, Н4а и Н4Ь соответственно). Гидрофобная впадина ЛТБ1 имеет форму вытянутого туннеля, в формировании которого принимают
участие спирали Н1, Н2 и Н3, расположенные параллельно друг другу. Гидрофобный характер поверхности туннеля обусловлен боковыми радикалами таких аминокислотных остатков, как Ile, Val, Leu, Ala, но наряду с этим в формировании впадины участвуют гидрофильные остатки Arg, Lys, Ser [7]. Туннель в молекулах белков ЛТБ1 имеет два входа, различающихся по размеру. У большинства ЛТБ1 около большого входа располагается основный остаток Arg44 (нумерация относительно ЛТБ1 риса Oryza sativa), который взаимодействует с полярными головками липидов [8]. У ЛТБ1 риса в этом взаимодействии принимает участие еще один основный остаток — Lys35. Кроме остатков цистеина в молекуле большинства ЛТБ1 присутствуют консервативные остатки глицина и про-лина, обеспечивающие повороты между спиралями; два остатка тирозина, один из которых находится в N-концевой области на внешней стороне а-спирали,
А
N-ter
С-С
N49
h4
Су-СУш
С»-Сш
cV—cV
C-CV
h3
С»-Сш
CIV-C
Рис. 2. Пространственные структуры (А) ЛТБ1 (PDB Ю: 1RZL) и (Б) ЛТБ2 (PDB ID: 1L6H) из риса в ленточном представлении. Указаны номера а-спиралей (Н1-Н4). Фиолетовым цветом показаны гидрофобные остатки, красным — остатки, взаимодействующие с липидным лигандом [5, 10], желтым — дисульфидные связи, зеленым -остаток во фрагменте -СУХСУ’-, обращенный наружу или внутрь молекулы белка
а второй расположен в С-концевой области у большого входа в гидрофобный туннель и участвует во взаимодействии с лигандами [7, 9].
ЛТБ2, состоящие из 65-70 аминокислотных остатков, изучены в меньшей степени, чем ЛТБ1. ЛТБ2 во фрагменте -CVXCVI- в качестве центрального остатка чаще всего содержат фенилаланин, обращенный внутрь молекулы, и имеют иную организацию дисульфидных связей: CI-CV, Сп-Сш, CIV-CVI1, CVI-CV111 (рис. 1Б, 2Б) [10]. Пространственная структура белков этого подкласса включает три а-спирали и область, содержащую одиночные витки спирали (рис. 2Б). В структуре ЛТБ2 спирали h2 и h3 располагаются параллельно друг другу, а спираль h4 направлена под углом 90° относительно h3. Гидрофобная впадина ЛТБ2 по форме напоминает трехгранный полый бокс с расположенными внутри боковыми радикалами остатков Ala, Ile, Leu, Phe и Val. Трехгранный бокс ЛТБ2 по объему меньше гидрофобной полости ЛТБ1, однако его более выраженная пластичность позволяет белкам этого подкласса связывать крупные лиганды с жесткой структурой, например стерины [10-12]. Боковые радикалы Phe39, Tyr45 и Tyr48 (нумерация относительно ЛТБ2 риса) повернуты внутрь полости и контактируют с ли-пидным лигандом [13]. Помимо остатков цистеина в структуре ЛТБ2 присутствуют консервативные остатки Gln, Tyr и Pro.
Объем гидрофобной впадины у ЛТБ обоих подклассов может значительно изменяться. Например, размер гидрофобной впадины у ЛТБ1 риса равен 249 А3, однако при связывании белка с пальмитиновой кислотой ее объем увеличивается до 1354 А3. Такая пластичность молекул ЛТБ может быть причиной их низкой специфичности к липидному лиганду.
СВЯЗЫВАНИЕ И ТРАНСПОРТ ЛИПИДОВ
Наличие в структуре молекул ЛТБ гидрофобной впадины позволяет этим белкам связывать и переносить различные лиганды. Образование комплексов ЛТБ с лигандами in vitro зависит от размера гидрофобной полости и формирующих ее аминокислотных остатков, пространственной структуры лиганда, а также от условий эксперимента (рН, состав буфера, температура). Показано, что ЛТБ, выделенные из различных растительных источников, способны связывать липиды. Однако стоит отметить, что существуют и исключения из этого правила. Так, белок из семян лука (Allium cepa), названный Ace-AMP1, обладает выраженной гомологией с растительными ЛТБ, но не взаимодействует с липидами, возможно, из-за отсутствия единой полости внутри молекулы белка
[14].ис-конфигурации [18], две из которых — линолевая и олеиновая кислоты — являются предшественниками мономеров кути-на и суберина.
ЛТБ1, в отличие от ЛТБ2, не связывают стерины. Установлено, что в зависимости от пространственной организации молекул ЛТБ1 и лиганда ориентация последнего в гидрофобной впадине может быть различной. Например, в комплексах ЛТБ1 кукурузы с 1-пальмитоиллизофосфатидилхолином [9] и ЛТБ1 пшеницы (Triticum aestivum) с димиристоилфосфа-тидилглицерином [18] лиганды размещаются в полости белка в «прямой» ориентации, т.е. полярные головки липидов расположены вблизи большого входа в гидрофобную впадину. В то же время в комплексе ЛТБ1 ячменя (Hordeum vulgare) с пальмитоил-КоА лиганд имеет «обратную» ориентацию, его алифатические цепи сильно изогнуты и полярная головка направлена в сторону меньшего входа впадины [19].
ЛТБ1 растений могут связывать одну или две молекулы лизофосфолипида [20]. Предполагается, что ЛТБ этого подкласса взаимодействуют с лиган-дами согласно кооперативной модели связывания. Если в гидрофобной полости находятся две молекулы лиганда, то их ориентация и прочность связывания с белком не одинаковы. Так, в комплексе ЛТБ1 пшеницы с лизомиристоилфосфатидилхолином две молекулы этого лиганда ориентированы в гидрофобной полости по принципу «голова к хвосту» [19, 21]. Высказывается предположение, что второй сайт связывания в ЛТБ активируется только тогда, когда первый уже занят лигандом.
Показано, что в регуляции связывания липи-дов растительными ЛТБ принимает участие каль-ций-кальмодулиновая система. Растительные ЛТБ связываются с кальмодулином вне зависимости от присутствия ионов кальция. Потенциальный сайт связывания кальмодулина с Zm-LTP кукурузы и Ace-AMP1 лука лежит в средней части полипептидной цепи ЛТБ (аминокислотные остатки
46-60) и имеет структуру, сходную с ВАА-доменом (Basic Amphiphilic a-helix) кальмодулин-связыва-ющих белков [22]. Отличительной особенностью ВАА-подобного домена у растительных ЛТБ является отсутствие Trp, имеющего решающее значение для кальций-зависимого связывания кальмодулина. В присутствии кальмодулина у Zm-LTP кукурузы снижается способность связывать липиды, что объясняется локализацией в кальмодулин-связываю-щем центре этого белка остатка Arg46, участвующего в связывании липидов. В то же время сайт связывания кальмодулина у белка репы (Brassica rapa), названного BP-10, и ЛТБ1 арабидопсиса (Ärabidopsis thaliana) находится в С-концевой области (аминокислотные остатки 69-81) и не имеет структурного сходства ни с одним из известных кальмодулин-связы-вающих центров [23]. Образование комплекса BP-10 с кальмодулином приводит к повышению эффективности связывания липидов. Причиной этого эффекта считается расположение в кальмодулин-связываю-щем центре данного ЛТБ остатка Tyr81, играющего важную роль во взаимодействии с липидным лиган-дом.
ЛТБ растений не только связывают липиды, но и осуществляют их перенос между мембранами в опытах in vitro. Они переносят фосфолипиды, например, фосфатидилхолины (ФХ), фосфатидилино-зиты (ФИ), фосфатидилглицерины (ФГ) и их производные, а также ацил-КоА [24-26]. На примере ЛТБ пшеницы показано, что липид-транспортирующая активность ЛТБ2 в несколько раз выше, чем у ЛТБ1 [27].
Механизм транспортировки липидов с участием ЛТБ до сих пор неизвестен. Предполагается, что растительные ЛТБ, так же как и фосфатидил-холин-специфичные ЛТБ млекопитающих, переносят липиды по челночному механизму. Комплекс ЛТБ-фосфолипид взаимодействует с мембраной, в результате чего происходит обмен фосфолипидами между комплексом и мембраной [3].
Прямые доказательства участия ЛТБ растений в связывании и переносе липидов in vivo до сих пор отсутствуют. Единственным комплексом ЛТБ c ли-гандом, обнаруженным в растительных клетках, является ковалентный аддукт LTP1 ячменя с окси-липином, образующийся при взаимодействии карбоксильной группы Asp7 с оксидом аллена в молекуле 9(£),10-эпокси-10,12(2)-октадекадиеновой кислоты [28, 29]. В результате реакции образуется a-кетол — 9-гидрокси-10-оксо-12(2)-октадеценовая кислота. Необходимо отметить, что образование этого ковалентного комплекса, получившего название LTP1b, приводит к увеличению пластичности гидрофобной впадины белка и его способности переносить липиды.
Некоторые ЛТБ способны не только связывать и переносить липиды, но и разрушать модельные мембраны. В качестве примера можно привести белок подсолнечника (Helianthus annuus), названный Ha-AP10, который разрушает липосомы, состоящие из ФХ и ФГ [30]. Интересно отметить отсутствие корреляции между липид-связывающей и ли-пид-переносящей активностью и способностью ЛТБ разрушать мембраны. Например, ЛТБ ячменя связывает широкий спектр липидов, однако слабо влияет на свойства модельных мембран [31]. Ace-AMP1 лука не связывает липиды, но нарушает целостность двухслойных везикул, состоящих из анионных ли-пидов [14].
БИОСИНТЕЗ И ЛОКАЛИЗАЦИЯ
Класс ЛТБ относится к большому семейству белков, связанных с патогенезом (Pathogenesis-Related Proteins, или PRP). Индукция синтеза данных белков происходит при воздействии на растение абиотических и биотических стрессорных факторов и лежит в основе одного из ключевых защитных механизмов, имеющихся в арсенале растений. PRP присутствуют во всех органах растений, накапливаются в вакуолях и апопласте, а также в первичной и вторичной клеточной стенке. Такая локализация согласуется с защитной функцией PRP, которые, наряду с антимикробными пептидами (AMP), создают своеобразный барьер на пути проникновения патогена [32].
Семейство белков, связанных с патогенезом, помимо ЛТБ (PRP-14), включает белки еще 16 классов: глюканазы (PRP-2), хитиназы (PRP-3,4,8), ингибиторы протеиназ (PRP-6), гомологи основного пыльцевого аллергена березы Bet v 1 (PRP-10), дефенсины (PRP-12), тионины (PRP-13) и др. [33]. Абиотическими индукторами синтеза PRP являются УФ-излучение, осмотический шок, дефицит влаги, низкие температуры, засоление почвы. Синтез PRP при инфицировании растения индуцируется как первичными, так и вторичными элиситорами — неспецифичными патоген-ассоциированными молекулярными структурами (Pathogen Associated Molecular Patterns, или PAMP), и структурами, ассоциированными с повреждением (Damage-Associated Molecular Patterns, или DAMP), а также специфичными эф-фекторными белками патогенов. Индукторами синтеза PRP являются такие фитогормоны, как этилен, ауксины, абсцизовая, жасмоновая и салициловая кислоты. На определенных стадиях онтогенеза активация синтеза и тканеспецифичная аккумуляция PRP происходят также в отсутствие факторов стресса [34].
ЛТБ обнаружены в различных органах растений -семенах, листьях, стеблях, корнях, цветках и плодах.
Чаще всего ЛТБ локализуются в покрытых кутикулой клетках эпидермиса, но обнаруживаются также в эмбриональных и сосудистых тканях. ЛТБ синтезируются в растительных клетках в виде пребелков, содержащих гидрофобную сигнальную последовательность (21-27 или 27-35 аминокислотных остатков у ЛТБ1 или ЛТБ2 соответственно), и являются секреторными белками с преимущественно внеклеточной локализацией [35, 36]. Некоторые ЛТБ имеют нехарактерную внутриклеточную локализацию. Так, ЛТБ из семян клещевины (Ricinus communis) обнаружен в глиоксисомах [37], ЛТБ из семян виг-ны (Vigna unguiculata) — в вакуолях [38], Ca-LTP(1) из семян перца (Capsicum annuum) — в везикулах [39]. Особый интерес представляет вопрос о том, каким образом ЛТБ, синтезируемые в виде пребелков и не имеющие соответствующих сигнальных последовательностей, попадают в эти клеточные органел-лы. Установлено, что ЛТБ подсолнечника Ha-AP10 изменяет свою локализацию. В покоящихся семенах Ha-AP10 находится в апопласте, но при набухании и прорастании семени, возможно, с помощью эндо-цитоза, поступает внутрь клеток и переходит в ор-ганеллы, участвующие в метаболизме липидов [40].
В некоторых растениях обнаружены ЛТБ, названные LTPG (GPI-anchored Lipid Transfer Proteins), которые синтезируются в виде предшественников, содержащих помимо N-концевого сигнального пептида С-концевую сигнальную последовательность. Эта последовательность обеспечивает посттрансляционное присоединение к белку гликозилфосфатиди-линозитного якоря (ГФИ), благодаря которому LTPG могут локализоваться на внешней стороне плазматической мембраны или секретироваться в апопласт после отщепления ГФИ-якоря [41]. Еще одну группу необычных ЛТБ, имеющих внеклеточную локализацию, составляют ксилоген из циннии (Zinnia elegans) и ксилоген-подобные белки других растений [42]. В структуре генов ксилоген-подобных белков, которые относятся к большому семейству арабинога-лактановых белков (АГБ), присутствует сигнальный пептид, домен ЛТБ, несколько доменов АГБ и ГФИ-якорь. В процессе созревания эти белки претерпевают ряд посттрансляционных превращений, включая удаление N-концевого сигнального пептида, присоединение ГФИ-якоря, гидроксилирование остатков пролина и О-гликозилирование [42].
ЛТБ растений кодируются мультигенными семействами и в геноме растений, как правило, представлены набором генов, кодирующих различные изоформы. Экспрессия генов различных изоформ ЛТБ отличается ярко выраженной тканевой специфичностью и происходит на определенных стадиях онтогенеза [36]. Предполагается, что это связано
с тем, что разные изоформы ЛТБ выполняют различные функции [43]. Дифференциальная экспрессия генов множественных изоформ ЛТБ происходит также при воздействии на растение различных абиотических и биотических факторов окружающей среды и может рассматриваться как один из элементов защитной стратегии в условиях стресса [44]. Дифференциальная экспрессия генов изоформ показана на примерах ЛТБ кунжута (Sesamum indicum) [45], арабидопсиса [43, 46], перца [47], клещевины [37], винограда (Vitis vinifera) [48], тамарикса жестковоло-систого (Tamarix hispida) [49] и томата (Lycopersicon pennellii) [50].
БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ
ЛТБ, как уже упоминалось, составляют один из классов защитных PRP, многие из которых обладают антимикробной и ферментативной активностями или являются ингибиторами ферментов. Различные представители класса ЛТБ проявляют антибактериальную, противогрибковую, противовирусную, антипролиферативную активности, обладают способностью влиять на активность разнообразных ферментов [36].
Антимикробная активность
Многие ЛТБ обладают антимикробной активностью и ингибируют рост таких фитопатогенных бактерий и грибов, как Clavibacter michiganensis, Pseudomonas solanacearum, P. syringae, Alternaria brassicola, Ascochyta pisi, Colletotrichum lindemuthianum, Fusarium solani, F. graminearum, F. culmorum, F. oxysporum, Botrytis cinerea, Sclerotinia sclerotiorum, Verticillium dahliae и др. ЛТБ из перца и кофе (Coffea canephora) активны также в отношении патогенных для человека штаммов грибков рода Candida [39, 51]. Антимикробное действие большинства растительных ЛТБ характеризуется специфичностью и проявляется в отношении определенного спектра микроорганизмов. Выраженной антимикробной активностью в микромолярных концентрациях обладают ЛТБ из лука [52], редиса (Raphanus sativus) [52] и арабидопсиса [53]. Основная же масса ЛТБ умеренно или слабо влияет на рост микроорганизмов, в некоторых случаях это влияние вообще отсутствует [54]. Антимикробная активность ЛТБ растений снижается в растворах с высокой концентрацией соли и в присутствии ионов кальция, что сближает данные белки с другими классами растительных AMP и PRP [52]. Как и растительные дефенсины, ЛТБ обладают способностью действовать в синергизме с тионинами [55], не оказывают токсического действия на растительные клетки и клетки млекопитающих, включая фибробласты и эритроциты [30, 52].
Разрушение дисульфидных связей, стабилизирующих структуру растительных ЛТБ, приводит к тому, что эти белки теряют способность ингиби-ровать рост микроорганизмов и связывать липиды [56]. В то же время другие аминокислотные остатки, необходимые для проявления антимикробной активности, остаются неизвестными. Для LTP110 из риса показано, что для проявления антимикробной активности этого белка важны консервативные остатки Tyr17, Arg46 и Pro72, которые у большинства ЛТБ1 играют существенную роль в стабилизации структуры белка [57]. При изучении изоформ ЛТБ пшеницы показано, что отличие всего в один аминокислотный остаток (Pro3Ser в изоформах TaLt10B6 и TaLt710h34, Asn24Ser в TaLt10F9 и TaBs116G9) существенно влияет на антимикробную активность белков. Предполагается, что замена даже одного аминокислотного остатка может приводить к изменению пространственной структуры ЛТБ и влиять на распределение положительного заряда на поверхности его молекулы [56].
На сегодняшний день установлено, что антимикробная активность растительных ЛТБ не связана с их способностью взаимодействовать с липидами. Так, на примере восьми изоформ ЛТБ пшеницы показано отсутствие корреляции между способностью этих белков ингибировать рост патогенных микроорганизмов и связывать липиды [56]. На примере Ace-AMP1 лука [52] и мутантной изоформы ЛТБ риса [57] также показано, что белки данного класса могут обладать антимикробной активностью, но не связывать при этом молекулы липидов и наоборот.
Растительные ЛТБ оказывают не только фунги-статическое, но и фунгицидное действие и подобно другим AMP вызывают нарушение проницаемости модельных мембран [30] и цитоплазматических мембран фитопатогенных грибов [30, 56]. Так, ЛТБ лука [14], подсолнечника [30] и в меньшей степени ячменя [31] обладают способностью нарушать проницаемость липосом, состоящих только из анионных фосфоли-пидов или из смеси анионных и нейтральных фосфо-липидов, вызывая утечку из них флуоресцентного красителя. Однако стоит отметить, что этот эффект выражен гораздо слабее, чем у других AMP растений, и наблюдается только в растворах с низкой ионной силой.
Механизм антимикробного действия представителей класса ЛТБ до сих пор неизвестен. Тем не менее возможной мишенью антимикробного действия ЛТБ считается цитоплазматическая мембрана. Предполагается, что растительные ЛТБ, как и другие катионные мембранотропные AMP, связываются посредством электростатических взаимодействий с цитоплазматической мембраной фитопатогена,
вызывая ее дестабилизацию и нарушение проницаемости. Ослаблением электростатического взаимодействия с клеточной мембраной фитопатоге-на объясняется менее выраженная антимикробная активность изоформ ЛТБ, содержащих меньше основных аминокислотных остатков [56]. Считается, что возможной причиной избирательной токсичности ЛТБ растений могут быть различия в липидном составе мембран клеток бактерий, грибов, растений и млекопитающих.
Противовирусная, антипролиферативная активность
Показано, что ЛТБ нарцисса (Narcissus tazetta) и капусты полевой (Brassica campestris), называемой также сурепицей, обладают противовирусной активностью и способностью ингибировать пролиферацию опухолевых клеток человека. ЛТБ нарцисса, обозначенный как NTP, в экспериментах in vitro значительно ингибировал образование бляшек респираторного синцитиального вируса (RSV) и цитопатический эффект вируса гриппа A (h2N1), а также пролиферацию линии клеток промиелоцитарного лейкоза человека (HL-60). ЛТБ капусты полевой подавлял активность обратной транскриптазы вируса иммунодефицита человека типа 1 (HIV-1), а также пролиферацию клеток злокачественной гепатомы HepG2 и рака молочной железы MCF7. Механизм противоопухолевой активности ЛТБ пока не установлен [58, 59].
Ингибирование активности ферментов
Отдельные представители класса ЛТБ, как и ингибиторы протеаз (PRP-6), и некоторые дефенсины (PRP-12) [60, 61], обладают способностью подавлять активность протеолитических ферментов и а-амилаз. Так, обнаружено, что ЛТБ обоих подклассов из семян ячменя ингибируют активность цистеиновых эндопро-теаз [62]. Также показано, что ЛТБ1 из семян гинкго двулопастного (Ginkgo biloba) подавляет активность цистеиновой (папаин), аспартатной (пепсин) и сери-новой (трипсин) протеаз [63]. ЛТБ1 из семян кофе и перца ингибируют активность а-амилазы человека [39, 51]. Как полагают, ЛТБ, способные ингибировать активность собственных и чужеродных ферментов, могут принимать участие как в развитии и прорастании семян, так и в защите растения от насекомых и травоядных животных.
ВОЗМОЖНЫЕ ФУНКЦИИ ЛТБ
Известно, что ЛТБ играют важную роль в растениях. Выключение генов, кодирующих данные белки, приводит к нарушению вегетативного и репродуктивного развития растений, снижению их устойчивости
к инфекциям [43, 64, 65]. На основании результатов исследований по подавлению экспрессии генов ЛТБ высказан ряд предположений о возможном участии представителей данного класса белков в адаптации растений к стрессу, метаболизме липидов, эмбриогенезе, росте и размножении растений, симбиозе и других процессах. Считается, что многие из этих функций обусловлены способностью ЛТБ связывать и переносить молекулы липидов (рис. 3).
Участие в метаболизме липидов
В связи с тем, что растительные ЛТБ обладают способностью связывать и переносить молекулы липи-дов, считается, что эти белки принимают участие в целом ряде процессов, сопровождающихся изменениями липидного состава. Для ЛТБ, имеющих внеклеточную локализацию, предполагается участие в формировании защитного слоя кутикулы, мономерные компоненты которой образуются в эпи-дермальных клетках и доставляются к месту биосинтеза. Активация биосинтеза кутикулы, которая играет важную роль в поддержании водного баланса и защите растений от проникновения патогенов, происходит в условиях действия разнообразных стрес-сорных факторов и является одним из защитных механизмов растений. Прямых доказательств причастности ЛТБ к этому процессу пока не найдено, однако показано, что растительные ЛТБ присутствуют в высоких концентрациях в эпидермальных тканях и способны связывать жирные кислоты, необходимые для синтеза кутина и суберина. Кроме того, индукция синтеза ЛТБ сопровождается утолщением слоя кутикулы [66], а выключение генов ЛТБ приводит к изменению липидного состава и плотности кутикулярного слоя [67]. Предложено два возможных механизма доставки компонентов кутикулы с участием ЛТБ. В соответствии с первым из них ЛТБ поступают в клетку посредством рецептор-опосредованного эндоцитоза, осуществляемого при слиянии везикул, содержащих ЛТБ и мономеры кутина. Второй механизм предполагает функционирование ЛТБ между плазматической мембраной и клеточной стенкой растения и существование молекулы-переносчика, действующего с внутренней стороны плазматической мембраны [68]. Интересен тот факт, что ЛТБ1 присутствуют в органах, покрытых слоем кутина (листья, стебли, цветки), в то время как ЛТБ2 обнаруживаются в покрытых суберином подземных органах. Это свидетельствует в пользу дифференциального участия белков первого и второго подклассов в формировании кутинового и суберинового слоев [35]. Показано также, что LTPG, имеющие ГФИ-якорь, возможно, принимают участие в биосинтезе и накоплении суберина [41].
апопласт
антимикробное действие
ингибирование
активности экзоферментов
размягчение и созревание плодов
цитоплазматическая мембрана
оплодотворение цветковых растений
секреция липидов
формирование кутикулы
межклеточные взаимодействия
активация защитных механизмов в растении
внутриклеточный транспорт липидов
регуляция сигнальных путей
апоптоз
цитоплазма
липидная молекула
Рис.КК как в свободной форме, так и в виде ацил-КоА. Этот белок увеличивает также активность ацил-КоА-ок-сидазы, которая участвует в реакции Р-окисления ЖК [37]. Предполагается, что ЛТБ подсолнечника Ha-AP10, поступающий в клетки при прорастании семян, переносит в глиоксисомы ЖК, высвободившиеся при расщеплении триацилглицеринов, для их дальнейшего Р-окисления [40].
Показано, что индукция экспрессии генов, кодирующих ЛТБ моркови (Daucus carota), наблюдается на ранних стадиях эмбриогенеза, когда происходит разрушение одних и биосинтез других липидов, а также формирование защитного липидного слоя вокруг зародыша [69]. Роль этого белка в процессе эмбриогенеза предположительно заключается в уча-
стии в этих процессах посредством переноса соответствующих липидных молекул.
Участие в оплодотворении цветковых растений
Считается, что растительные ЛТБ играют важную роль в репродукции цветковых растений. Так, ЛТБ1 лилии (Lilium longiflorum) является компонентом, необходимым для адгезии пыльцы, формирования и роста пыльцевой трубки [70]. Предполагается, что ЛТБ1 может действовать непосредственно как адгезивный компонент либо как переносчик гидрофобного адгезивного компонента. Показано также, что одна из изоформ липид-транспортирующего белка арабидопсиса, LTP5, участвует в росте пыльцевой трубки и формировании семян [64].
Выявлена роль ЛТБ риса OsC6 в постмейотиче-ском развитии пыльцы. Установлено, что данный белок присутствует в тканях пыльника и обладает способностью связывать ЖК. Полагают, что OsC6 участвует в формировании липидных орбикул
и пыльцевой экзины, осуществляя перенос необходимых липидов из клеток тапетума к микроспорам [65].
Участие в защите и адаптации растений в условиях стресса
Утверждение, что ЛТБ участвуют в защите и адаптации растений к воздействию стрессорных факторов, основано, в основном, на повышении уровня синтеза этих белков. Так, синтез ЛТБ, как и других PRP, индуцируется при механическом повреждении, дефиците влаги, низких температурах, засолении почвы, инфицировании, а также при обработке растения химическими агентами [43, 45, 47, 50, 71, 72]. Индукция экспрессии генов ЛТБ в условиях стресса, возможно, связана с наличием в их промоторной области регуляторных элементов, характерных также для генов других PRP. В регуляции экспрессии генов ЛТБ участвуют такие фитогормоны, как абсцизовая и салициловая кислоты, этилен и метилжасмонат [36].
Считается, что одной из возможных причин индукции экспрессии генов ЛТБ в условиях стресса является вовлеченность этих белков в биосинтез ку-тикулярного слоя [50]. Защитная функция ЛТБ в растениях обусловлена их антимикробной активностью, криопротекторным действием и свойствами ингибиторов экзогенных ферментов, а также возможным участием в секреции других компонентов иммунной системы растений.
Железистые волоски (трихомы) растений вырабатывают эфирные масла, которые принимают участие в обмене веществ, защищают растение от вредителей, оказывают ранозаживляющее действие, служат для привлечения насекомых и предохраняют от перегревания. Обнаружено, что NtLTP1 табака (N. tabacum) специфически экспрессируется в длинных железистых волосках и участвует в секреции из головок трихом компонентов эфирных масел (дитерпе-нов, алифатических углеводородов и ароматических кислот), которые являются защитными факторами растений [73]. Транскрипты генов ЛТБ обнаружены в железистых волосках и других растений, например, мяты (Mentha piperita), люцерны (Medicago sativa), полыни (Artemisia annua), хмеля (Humulus lupulus), шалфея (Salvia fruticosa) и томата [73].
Известно, что устойчивость растений к холоду связана со стабилизацией клеточных мембран и предотвращением снижения растворимости белков при понижении температуры. В листьях акклиматизированной к холоду капусты (Brassica oleracea) обнаружены белки класса WAX9, имеющие высокую степень гомологии аминокислотных последовательностей с ЛТБ. Данные белки не обладают способностью связывать липиды, но подобно ß-1,3-
глюканазам, осмотинам и лектинам, способны в условиях холода стабилизировать мембраны тилакоидов [72]. Предполагается, что механизм криопротектор-ного действия этих белков связан с уменьшением подвижности мембранных липидов и проницаемости бислоя при взаимодействии ЛТБ с мембраной тила-коидов [74].
Участие в активации и регуляции сигнальных каскадов
Предполагается, что ЛТБ, образуя комплексы с различными молекулами липидов, могут принимать участие в активации и регуляции различных сигнальных каскадов в растениях. Одним из классов сигнальных медиаторов растений являются оксилипины, которые образуются из ненасыщенных ЖК под действием активных форм кислорода (АФК) или ферментов и участвуют в регуляции роста и развития растения, а также в запуске ответных защитных реакций в условиях стресса. Помимо этого, оксилипины регулируют процессы обезвреживания токсичных компонентов, образующихся во время стресса. Как уже упоминалось, ЛТБ1 ячменя в процессе прорастания семян формирует ковалентные комплексы с оксили-пином — 9(£),10-эпокси-10,12(2)-октадекадиеновой кислотой, содержащей нестабильный алленоксид, образующийся в результате последовательного действия липоксигеназы и алленоксидсинтазы [28, 29]. Такое взаимодействие может свидетельствовать о совместном участии ЛТБ и оксилипинов в регуляции сигнальных путей, запускающих механизм предотвращения повреждения клеток растения в условиях стресса [29].
ЛТБ в комплексе с молекулами липидов действуют как эндогенные элиситоры, взаимодействующие со специфическими рецепторами на цитоплазма-тической мембране растительных клеток и обеспечивающие развитие иммунного ответа в условиях инфицирования (рис. 4). Так, показано, что ЛТБ риса и табака обладают способностью взаимодействовать с элиситиновыми рецепторами [21, 75, 76]. Элиситины — хорошо изученные РАМР растений, которые имеют молекулярную массу около 10 кДа и продуцируются фитопатогенными оомице-тами (Phytophthora и РуШшт), паразитирующими на высших растениях. Данные белки, благодаря наличию в их структуре гидрофобной впадины, обладают способностью связывать стерины и обеспечивают фитопатогенные микроорганизмы необходимыми для их жизнедеятельности липидами, источником которых служат растения. Все элиситины имеют а-спиральную структуру, стабилизированную тремя дисульфидными связями, и в комплексе со стерином распознаются растением посредством
клеточная стенка
апопласт
мембрана
цитоплазма
киназный каскад
I
стерины, ЖК, жасмоновая кислота
изменение экспрессии генов
i
SAR
I
ЛТБ
липазы,кутиназы фитопатогенов
Рис. 4. Возможный механизм участия ЛТБ в активации иммунного ответа в растениях. ЛТБ секретируются в апопласт и связываются с молекулами липидов, которые так же секретируются растением, как, например, жасмоновая кислота, или образуются в результате действия ферментов, выделяемых фитопатогенными микроорганизмами. В комплексе с липидами ЛТБ взаимодействуют с расположенными на цитоплазматической мембране рецепторами, например, с рецептор-подобными серин-треониновыми протеинкиназами, которые содержат внеклеточный обогащенный лейциновыми повторами LRR-домен, а также трансмембранный и цитоплазмати-ческий протеинкиназный (PK) домены. Результатом этого взаимодействия может быть передача сигнала, опосредованная универсальными вторичными мессенджерами и каскадом митоген-активируемых протеинкиназ, активация ряда транскрипционных факторов, индукция синтеза защитных факторов, в том числе AMP и PRP (возможно также и изоформ ЛТБ с выраженной антимикробной активностью), и, в конечном итоге, развитие SAR
рецептор-подобных киназ, расположенных на цитоплазматической мембране. В результате распознавания происходит активация в растениях защитных механизмов, таких, как образование фитоалексинов и АФК, развитие гиперчувствительного ответа (HR) и системной приобретенной резистентности (SAR) [77, 78]. Аминокислотные последовательности ЛТБ и элиситинов имеют низкую степень гомологии, тогда как пространственные структуры этих белков обладают выраженным сходством [79]. Растительные ЛТБ в комплексе с молекулой липида выступают в роли агонистов элиситинов и DAMP, связываются с рецепторами элиситинов и вызывают развитие иммунного ответа. Интересным фактом, говорящим о возможности существования различных путей ак-
тивации защитного ответа в растениях с участием представителей двух подклассов ЛТБ, является отличие в структуре гидрофобного лиганда, в роли которого для ЛТБ2 выступают молекулы стеринов [75], а для обладающих менее гибкой гидрофобной впадиной ЛТБ1 — жасмоновая кислота [21, 76].
Показано также, что необычный представитель ЛТБ2 из арабидопсиса, имеющий изоэлектрическую точку в кислой области pH и названный DIR1, играет ключевую роль в развитии SAR [80]. Предполагается, что данный белок в процессе инфицирования растения связывается с молекулами липидов (оксили-пинами, жирными кислотами или моноацильными фосфолипидами), которые образуются в результате работы секретируемых патогеном липаз, после чего
образованный комплекс взаимодействует с гипотетическим рецептором, запуская сигнальный каскад, приводящий к развитию SAR [81].
Установлено, что ксилоген из циннии, содержащий ГФИ-якорь и связывающий растительные стерины, стимулирует превращение недифференцированных клеток в элементы трахеи и, возможно, участвует в межклеточных взаимодействиях и передаче сигнала. Предполагается, что ксилогено-подобные белки других растений, ЛТБ-домены которых имеют большее сходство с ЛТБ2, также могут участвовать в межклеточных взаимодействиях и передаче сигнала, функционируя в комплексе с липидной молекулой [42].
Участие в апоптозе
Предположение о возможном участии ЛТБ в апоп-тозе выдвинуто на основании сходства между ЛТБ кукурузы и проапоптотическим белком Bid млекопитающих, который тоже имеет в своей структуре внутреннюю впадину, связывает и переносит липиды [82]. Bid находится в цитозоле и в присутствии лизо-фосфолипидов, образующихся в процессе программируемой клеточной смерти, действует на митохондрии, вызывая высвобождение факторов индукции апоптоза, в том числе цитохрома с. ЛТБ кукурузы в присутствии лизофосфолипидов также вызывает высвобождение цитохрома с из митохондрий. В качестве возможного механизма дестабилизирующего действия обоих белков рассматривают перенос лизо-фосфолипидов на наружную мембрану митохондрий, которые изменяют ее свойства, облегчая тем самым действие других проапоптотических белков [83].
Участие в симбиозе
Известно, что симбиотические ризобактерии стимулируют рост растений и защищают их от почвенных фитопатогенов, вызывая развитие так называемой индуцированной системной резистентности, которая фенотипически и функционально сходна с SAR [84]. Показано, что ЛТБ MtN5 люцерны играет важную роль в развитии симбиотических отношений между растением и клубеньковыми бактериями, а именно, вовлечен в процессы проникновения бактерий в ткани корня и формирования клубеньков [85].абилизированная дисульфидными связями структура этих белков придает им повышенную устойчивость к расщеплению пищеварительными ферментами, позволяет достигать кишечника человека в нативной иммуногенной форме и вызывать сенсибилизацию организма [88]. Аллергизирующая способность ЛTБ в различных прошедших обработку пищевых продуктах (соках, джемах, пиве, вине и др.) объясняется их высокостабильной структурой, практически не подверженной тепловой денатурации, химической деградации и ферментативному расщеплению [89]. Необходимо отметить, что охарактеризованными аллергенами являются в основном представители первого подкласса растительных ЛTБ. Tак, в настоящий момент в базе данных аллергенов IUIS зарегистрированы всего три ЛTБ2 (из томата, арахиса и сельдерея) и 42 ЛTБ1 из различных растений, не считая их изоформ. Высокая структурная гомология ЛTБ1 обуславливает развитие перекрестных аллергических реакций.
ЛTБ1, широко распространенные в царстве растений, являются основными аллергенами, выделенными из фруктов и ягод, — Pru p 3 персика (Prunus persica), Pru av 3 вишни (P. avium), Mal d 3 яблока (Malus domestica), Pru d 3 сливы (P. domestica), Cit s 3 апельсина (Citrus sinensis), Vit v 1 винограда, Fra a 3 клубники (Fragaria ananassa), орехов — Cor a 8 фундука (Corylus avellana), Jug r 3 грецкого ореха (Juglans regia), Ara h 9 арахиса (Arachis hypogaea), Cas s 8 каштана (Castanea sativa), овощей — Aspa o 1 салата-латука (Asparagus officinalis), Lec s 1 спаржи (Lactuca sativa), Bra o 3 капусты, Lyc e 3 томата (Lycopersicon esculentum), Api g 2 сельдерея (Apium graveolens), злаковых — Zea m 14 кукурузы, Ory s 14 риса, Tri a 14 пшеницы, Hor v 14 ячменя и бобовых культур Len c 3 чечевицы, Pha v 3 фасоли [90-92]. Важно отметить, что ЛTБ накапливаются в основном в кожице плодов, а не в их мякоти [93], что может быть причиной развития анафилактических реакций при кожном контакте человека с плодами [94]. Cущественный вклад в первичную сенсибилизацию вносят и пыльцевые аллергены класса ЛTБ (Par j 2 постенницы иудейской (Parietaria judaica), Ole e 7 оливкового дерева (Olea europoea), Pla a 3 платана (Platanus acerifolia), Art v 3 полыни (Artimisia vulgar-is) и др.44 [100]. В роли Т-клеточного эпитопа Рги р 3 выступает участок полипептидной цепи, соответствующий аминокислотным остаткам 61-80 [101]. Также показано, что развитие Т-клеточного ответа на Рги р 3 сопровождается увеличением экспрессии интегрина а4Р7, обеспечивающего миграцию лимфоцитов в стенку кишечника, где происходит их первичная активация [102].
ЭВОЛЮЦИЯ ГЕНОВ
Гены ЛТБ повсеместно присутствуют в геномах высших растений — от наиболее примитивных мохообразных до сосудистых, включая папоротникообразные, плауновидные, покрытосеменные и голосеменные, но не обнаружены в таких низших растениях, как водоросли. В связи с этим высказывается предположение о том, что ЛТБ, принимающие участие в защите растений от воздействия разнообразных стрессорных факторов окружающей среды, могли появиться в период выхода растений на сушу, т.е. около 400 млн лет тому назад [103].
Как упоминалось выше, ЛТБ одного растения кодируются обычно десятками родственных генов, образующих мультигенное семейство. Считается, что появление в процессе эволюции множественных изоформ ЛТБ, выполняющих различные функции в растениях, связано с рядом последовательных дупликаций гена-предшественника и последующих мутаций [104]. Известно, что большинство покрытосеменных подверглись в процессе эволюции одному или нескольким удвоениям целого генома. Филогенетический анализ множественных изоформ ЛТБ риса, арабидопсиса и пшеницы свидетельствует о том, что процесс дупликации генов и фрагментов
хромосом продолжается и в настоящее время [105]. Мутации в дуплицированных генах ЛТБ в процессе эволюции могли приводить к псевдогенизации гена, субфункционализации с сохранением части функций гена-предшественника или неофункционализации, т.е. приобретению геном совершенно новых функций [106]. Последние два варианта могли привести к появлению новых изоформ ЛТБ, обладающих иным спектром и степенью выраженности биологической активности, а также ЛТБ-подобных белков, значительно отличающихся от представителей класса ЛТБ по структуре и выполняющих другие функции.
ПРАКТИЧЕСКОЕ ПРИМЕНЕНИЕ
ЛТБ как переносчики лекарственных средств
Способность ЛТБ связывать и переносить липиды создает предпосылки для их возможного применения в качестве лиганд-связывающих белков для создания систем доставки лекарственных и косметических средств с целью защиты от преждевременной биодеградации или снижения побочных эффектов при системном применении. Возможность создания систем доставки на основе ЛТБ определяется рядом их свойств: а) устойчивостью к тепловой денатурации и действию протеаз; б) гидрофильной поверхностью, обеспечивающей биосовместимость комплекса с лигандом и снижение риска развития побочных реакций; в) защитой лекарственного вещества, расположенного внутри гидрофобной полости ЛТБ, от преждевременной биодеградации; г) небольшим размером комплекса с лигадом, обеспечивающим его эффективное проникновение в ткани; д) увеличением аффинности и специфичности при образовании комплексов ЛТБ с лигандами, которое может быть достигнуто посредством модификации аминокислотной последовательности белка.
В ряде работ показано, что растительные ЛТБ образуют комплексы не только с ЖК и фосфолипида-ми, но и с другими гидрофобными и амфифильны-ми лигандами, включая некоторые лекарственные вещества. Так, ЛТБ1 пшеницы образует комплексы с простагландином В2 (PGB2). Установлено, что при взаимодействии с ЛТБ1 PGB2 полностью погружается в гидрофобную полость белка, оказываясь при этом изолированным от окружающей среды [17]. Показано, что ЛТБ1 пшеницы связывает некоторые компоненты липидного слоя кожи (сфин-гозины, сфингомиелины и цереброзиды), которые входят в состав косметических средств. Таким образом, ЛТБ1 пшеницы может быть использован в косметологии как средство доставки эпидермальных липидов. С другой стороны, ЛТБ1 пшеницы способен связывать лекарственные средства, которые актив-
ны в отношении возбудителей лейшманиоза и HIV-1, а также обладают антинеопластическими свойствами, но имеют серьезные побочные эффекты при системном применении (например, эделфозин, илмо-фозин и их аналоги). Использование ЛТБ1 пшеницы в качестве средства доставки может значительно снизить токсичность этих препаратов. Кроме того, ЛТБ1 пшеницы способен осуществлять доставку таких противогрибковых средств, как коназол BD56 и амфотерицин В [16]. Следует отметить, что белок связывает все перечисленные соединения с низкой аффинностью, что является обязательным условием транспорта и контролируемого высвобождения лиганда.
В результате скрининга с использованием библиотеки CMC (Comprehensive Medicinal Chemistry), содержащей информацию о ~7300 биологически активных соединениях, показано, что ЛТБ1 кукурузы и ЛТБ2 риса содержат не один, а два потенциальных центра связывания лекарственных веществ — один в гидрофобной полости, второй — на гидрофильной поверхности молекулы белка. У ЛТБ2 риса вблизи гидрофобной полости располагается центр связывания стеринов, например Р-ситостерина или холестерина, а на поверхности белка вблизи С-концевого участка находится область связывания трифенилме-тановых производных, например дифенил(пиридил-4)-метана [15].
ЛТБ в пищевой промышленности
Поверхностно-активные свойства ЛТБ растений делают возможным их применение в пищевой промышленности в качестве стабилизаторов пен и эмульсий. Пивоварение — одна из отраслей пищевой промышленности, где широко используются эти свойства ЛТБ. Известно, что образование и стабильность пены являются важными показателями качества пива. В многочисленных работах показано, что ЛТБ являются основными белковыми компонентами ячменного пива и играют ключевую роль в формировании и стабилизации пивной пены [35, 75]. В число основных белковых компонентов пива входит LTP1 ячменя, который связывает липиды и тем самым снижает их негативное влияние на формирование и стабильность пены. В процессе пивоварения происходит гликозилиро-вание и ацилирование LTP1, что увеличивает ам-фифильность и поверхностно-активные свойства этого белка [75]. При ферментации происходит образование LTPlb — ковалентного комплекса этого белка с 9(£),10-эпокси-10,12(2)-октадекадиеновой кислотой, о котором упоминалось выше [107]. LTP1 и LTPlb устойчивы к действию высоких температур, и в процессе нагревания при пастеризации
пива сохраняют свою структуру и способность взаимодействовать с липидами. Необходимо отметить, что LTP1, в отличие от LTP1b, обладает противогрибковой активностью, ингибирует рост дрожжей и тем самым может негативно влиять на процесс ферментации, поэтому образование LTP1b и установление равновесия между содержанием в пиве свободной и связанной с липидом форм LTP1 важны для получения ячменного пива высокого качества.
Создание жизнестойких трансгенных растений
Большой интерес представляет возможность использования ЛTБ для создания трансгенных растений, устойчивых к действию разнообразных абиотических и биотических стрессорных факторов. Tрансгенные растения, несущие гены ЛTБ, обладают повышенной устойчивостью к фитопатогенным микроорганизмам [108], поражению вредителями [73], действию высоких температур [109], засолению почвы [108], засухе [110] и др.временное направление развития аллергодиаг-ностики основано на замене суммарных экстрактов на индивидуальные белковые аллергокомпоненты, которые могут быть использованы для составления молекулярного профиля чувствительности пациента и изучения перекрестной реактивности аллергенов [111]. В современных тест-системах в формате микрочипов, предназначенных для компонент-разрешающей диагностики, на сегодняшний день уже используются несколько природных и рекомбинант-ных пыльцевых (Art v 3 полыни, Pla a 3 платана, Par j 2 постенницы и Ole e 7 маслины) и пищевых (Pru p 3 персика, Cor a 8 фундука, Jug r 3 грецкого ореха, Ara h 9 арахиса и Tri a 14 пшеницы) аллергенных ЛTБ.
Современный метод снижения реактивности организма — аллерген-специфическая иммунотерапия (АСИТ), при которой пациенту вводятся постепенно повышающиеся дозы аллергена [112]. Однако традиционно при АСИТ используют неочищенные экстракты или аллергоиды, которые характеризуются низкой эффективностью и высоким риском развития системных аллергических реакций. Наиболее безопасное и перспективное направление АСИТ предполагает разработку и создание вакцин на основе индивидуальных природных и рекомбинантных аллергенов, а также их гипоаллергенных аналогов. Эти аналоги должны обладать низкой аллергенно-стью, но достаточно высокой иммуногенностью, чтобы не вызывать побочных аллергических реакций и надолго снижать гиперчувствительность организма [113]. Гипоаллергенные формы создаются в основном с помощью методов рационального дизайна и сайт-направленного мутагенеза путем замены аминокислотных остатков, входящих в состав В-клеточных эпитопов. На сегодняшний день несколько гипоал-лергенных аналогов основных пыльцевых и пищевых аллергенов различных классов проходят клинические испытания в качестве лекарственных препаратов для проведения АСИТ [114]. К настоящему времени получены гипоаллергенные формы ряда растительных ЛТБ, например, Par j 2 постенницы [115] и Pru p 3 персика [116], но среди препаратов, проходящих клинические испытания, пока отсутствуют вакцины на основе гипоаллергенных форм растительных ЛТБ.
ЗАКЛЮЧЕНИЕ
ЛТБ широко распространены в царстве растений, присутствуют практически во всех растительных органах и тканях, имеют внутри- или внеклеточную локализацию и играют важную физиологическую роль. ЛТБ, кодируемые мультигенным семейством, в растениях представлены набором множественных изоформ, дифференциально экспрессирующихся в различных органах и тканях в условиях воздействия различных стрессогенных факторов окружающей среды. Помимо этого, в растениях обнаружены разнообразные ЛТБ-подобные белки, которые имеют сильно отличающуюся структуру и функциональную
СПИСОК ЛИТЕРАТУРЫ
1. Abdelkader A.B., Mazliak P. // Eur. J. Biochem. 1970. V. 15. P. 250-262.
2. Vergnolle C., Arondel V., Jolliot A., Kader J. // Methods Enzy-mol. 1992. V. 209. P. 522-530.
3. Kader J.-C. // Annu. Rev. Plant. Physiol. Plant. Mol. Biol. 1996. V. 47. P. 627-654.
4. Perrocheau L., Bakan B., Boivin P., Marion D. // J. Agricult. Food Chem. 2006. V. 54. № 8. P. 3108-3113.
активность. Предполагается, что появление в ходе эволюции множественных изоформ ЛТБ и ЛТБ-подобных белков обусловлено необходимостью расширения спектра функций, выполняемых этими белками.
Биологическая роль ЛТБ в растениях изучена не до конца. Показано, что ЛТБ принимают участие во многих процессах, что, вероятно, во многом обусловлено их способностью связывать и переносить разнообразные молекулы липидов.
Достоверно установлено, что ЛТБ относятся к молекулярным факторам системы врожденного иммунитета растений. Являясь компонентами семейства РИР — белков, связанных с патогенезом, ЛТБ принадлежат к защитной системе растений, позволяющей им быстро адаптироваться и выживать в условиях стресса. Защитная функция ЛТБ обусловлена их антимикробной активностью и способностью ингиби-ровать чужеродные ферменты, участием в переносе сигнальных медиаторов, защитных и строительных липидов, а также свойствами эндогенных элисито-ров, которые в комплексе с молекулой липида распознаются специфическими рецепторами и запускают иммунный ответ.
ЛТБ играют важную роль в жизни человека. Широкое распространение и сходная пространственная организация делают эти белки одним из важнейших классов перекрестных растительных аллергенов, являющихся частой причиной развития аллергических реакций различной степени тяжести. Поверхностно-активные и аллергенные свойства, а также способность ЛТБ связывать и переносить гидрофобные лиганды делают возможным применение этих белков в фармации для конструирования систем доставки лекарственных и косметических средств, в аллергологии для создания современных диагностических тест-систем и препаратов для аллерговак-цинации, в пищевой промышленности для производства высококачественных сортов пива и в сельском хозяйстве для получения растений, устойчивых к стрессу. •
Исследование выполнено за счет гранта Российского научного фонда (проект № 14-50-00131).
5. Lee J.Y., Min K., Cha H., Hwang D.H.S.K.Y., Suh S.W. // J. Mol. Biol. 1998. V. 276. P. 437-448.
6. Gizatullina A.K., Finkina E.I., Mineev K.S., Melnikova D.N., Bogdanov I.V., Telezhinskaya I.N., Balandin S.V., Shenkarev Z.O., Arseniev A.S., Ovchinnikova T.V. // Biochem. Biophys. Res. Commun. 2013. V. 439. № 4. P. 427-432.
7. Simorre J., Caille A., Dominique M., Didier M., Ptak M. // Biochemistry. 1991. V. 30. P. 11600-11608.
8. Yeasts T.H., Rose J.K.C. // Protein Sci. 2007. V. 17. P. 191-198.
9. Gomar J., Petit M.-C., Sodano P., Sy D., Marion D., Kader J.-C., Vovelle F., Ptak M. // Protein Sci. 1996. V. 5. № 4. P. 565-577.
10. Samuel D., Liu Y.J., Cheng C.S., Lyu P.C. // J. Biol. Chem. 2002. V. 277. P. 35267-35273.
11. Hoh F., Pons J.L., Gautier M.F., de Lamotte F., Dumas C. // Acta Crystallogr. D. Biol. Crystallogr. 2005. V. 61. P. 397-406.
12. Pons J.L., de Lamotte F., Gautier M.F., Delsuc M.A. // J. Biol. Chem. 2003. V. 278. P. 14249-14256.
13. Cheng C.S., Chen M.N., Lai Y.T., Chen T., Lin K.F., Liu Y.J., Lyu P.C. // Proteins. 2008. V. 70. № 3. P. 695-706.
14. Tassin S., Broekaert W.F., Marion D., Acland D.P., Ptak M., Vovelle F., Sodano P. // Biochem. 1998. V. 37. P. 3623-3637.
15. Cheng C.S., Chen M.N., Liu Y.J., Huang L.Y., Lin K.F., Lyu P.Ch. // Enzyme Microb. Technol. 2004. V. 35. P. 532-539.
16. Pato C., Borgne M., Baut G., Papec P., Marion D., Douliez J.-P. // Biochem. Pharmacol. 2001. V. 62. P. 555-560.
17. Tassin-Moindrot S., Caille A., Douliez J.P., Marion D., Vovelle F. // Eur. J. Biochem. 2000. V. 267. P. 1117-1124.
18. Douliez J.-P., Michon T., Marion D. // Biochim. Biophys. Acta. 2000. V. 1467. P. 65-72.
19. Charvolin D., Douliez J.-P., Marion D., Cohen-Addad C., Pebay-Peyroula E. // Eur. J. Biochem. 1999. V. 264. P. 562-568.
20. Cheng H., Cheng P., Peng P., Lyu P., Sun Y. // Protein Sci. 2004. V. 13. P. 2304-2315.
21. Buhot N., Gomes E., Milat M.L., Ponchet M., Marion D., Lequeu J., Delrot S., Coutos-Thévenot P., Blein J.P. // Mol. Biol. Cell. 2004. V. 15. № 11. P. 5047-5052.
22. Li C., Xie W., Bai W., Li Z., Zhao Y., Liu H. // FEBS J. 2008. V. 275. № 21. P. 5298-5308.
23. Wang Z., Xie W., Chi F., Li C. // FEBS Lett. 2005. V. 579. № 7. P. 1683-1687.
24. Guerbette F., Grosbois M., Jolliot-Croquin A. // Mol. Cell. Biochem. 1999. V. 192. P. 157-161.
25. Guerbette F., Grosbois M., Jolliot-Croquin A., Kader J.-C., Zachowski A. // Biochemistry. 1999. V. 38. P. 14131-14137.
26. Ostergaard J., Vergnolle C., Schoentgen F., Kader J.-C. // Biochim. Biophys. Acta. 1993. V. 1170. P. 109-117.
27. Douliez J.-P., Pato C., Rabesona H., Molle D., Marion D. // Eur. J. Biochem. 2001. V. 268. P. 1400-1403.
28. Bakan B., Hamberg M., Larue V., Prangé T., Marion D., Las-combe M.B. // Biochem. Biophys. Res. Commun. 2009. V. 390. P. 780-785.
29. Bakan B., Hamberg M., Perrocheau L., Maume D., Rogniaux H., Tranquet O., Rondeau C., Blein J.P., Ponchet M., Marion D. // J. Biol. Chem. 2006. V. 281. № 51. P. 38981-38988.
30. Regente M.C., Giudici A.M., Villalaín J., de la Canal L. // Lett. Appl. Microbiol. 2005. V. 40. P. 183-189.
31. Caaveiro J.M.M., Molina A., González-Mañas J.M., Rodrí-guez-Palenzuela P., García-Olmedo F., Goñi F.M. // FEBS Lett. 1997. V. 410. P. 338-342.
32. Hoffmann-Sommergruber K. // Biochem. Society Transactions. 2002. V. 30. P. 930-935.
33. van Loon L.C., Rep M., Pieterse C.M. // Annu. Rev. Phyto-pathol. 2006. V. 44. P. 135-162.
34. Edreva A. // Gen. Appl. Plant Physiol. 2005. V. 31. P. 105-124.
35. Douliez J., Michon T., Elmorjani K., Marion D. // J. Cereal Sci. 2000. V. 32. P. 1-20.
36. Carvalho A.O., Gomes V.M. // Peptides. 2007. V. 28. P. 11441153.
37. Tsuboi S., Osafune T., Tsugeki R., Nishimura M., Yamada M. // Biochem. 1992. V. 3. P. 500-508.
38. Carvalho A.O., Teodoro C.E.S., Da Cunha M., Okorokova-Facanha A.L., Okorokov L.A., Fernandes K.V.S., Gomes V.M. // Physiol. Plant. 2004. V. 122. P. 328-336.
39. Diz M.S., Carvalho A.O., Ribeiro S.F., Da Cunha M., Beltra-
mini L., Rodrigues R., Nascimento V.V., Machado O.L., Gomes V.M. // Physiol. Plant. 2011. V. 142. № 3. P. 233-246.
40. Pagnussat L., Burbach C., Baluska F., de la Canal L. // J. Exp. Bot. 2012. V. 63. № 18. P. 6555-6563.
41. Edstam M.M., Edqvist J. // Physiol Plant. 2014. V. 152. № 1. P. 32-42.
42. Kobayashi Y., Motose H., Iwamoto K., Fukuda H. // Plant Cell Physiol. 2011. V. 52. № 6. P. 1095-1106.
43. Chae K., Gonong B.J., Kim S.C., Kieslich C.A., Morikis D., Balasubramanian S., Lord E.M. // J. Exp. Bot. 2010. V. 61. № 15. P. 4277-4290.
44. Garcia-Olmedo F., Molina A., Segura A., Moreno M. // Trends in Microbiology. 1995. V. 3. № 2. P. 72-74.
45. Choi A.M., Lee S.B., Cho S.H., Hwang I., Hur C.-G., Suh M.C. // Plant Physiol. Biochem. 2008. V. 46. P. 127-139.
46. Thoma S., Hecht U., Kippers A., Botella J., De Vries S., Somerville C. // Plant Physiol. 1994. V. 105. P. 35-45.
47. Jung H.W., Kim W., Hwang B.K. // Plant Cell Environ. 2003. V. 26. № 6. P. 915-928.
48. Gomes E., Sagot E., Gaillard C., Laquitaine L., Poinssot B., Sanejouand Y.H., Delrot S., Coutos-Thévenot P. // Mol. Plant Microbe Interact. 2003. V. 16. № 5. P. 456-464.
49. Wang C., Yang C., Gao C., Wang Y. // Tree Physiol. 2009. V. 29. № 12. P. 1607-1619.
50. Trevino M.B., O’Conell M.A. // Plant Physiol. 1998. V. 116. P. 1461-1468.
51. Zottich U., Da Cunha M., Carvalho A.O., Dias G.B., Silva N.C., Santos I.S., do Nacimento V.V., Miguel E.C., Machado O.L., Gomes V.M. // Biochim. Biophys. Acta. 2011. V. 1810. № 4. P. 375-383.
52. Cammue B.P.A., Thevissen K., Hendriks M., Eggermont K., Goderis L.J., Proost P., Damme J.V., Osborn R.W., Guerbette F., Kader J., Broekaert W.F. // Plant Physiol. 1995. V. 109.
P. 445-455.
53. Segura A., Moreno M., García-Olmedo F. // FEBS Lett. 1993. V. 332. № 3. P. 243-246.
54. Dubreil L., Gaborit T., Bouchet B., Gallant D.J., Broekaert W.F., Quillien L., Quillien L., Marion D. // Plant Sci. 1998.
V. 138. P. 121-135.
55. Molina A., Segura A., Garcia-Olmedo F. // FEBS. 1993. V. 316. P. 119-122.
56. Sun J.Y., Gaudet D.A., Lu Z.X., Frick M., Puchalski B., Laroche A. // Mol. Plant Microbe Interact. 2008. V. 21. № 3. P. 346-360.
57. Ge X., Chen J., Sun C., Cao K. // Prot. Eng. 2003. V. 16. P. 387-390.
58. Ooi L.S., Tian L., Su M., Ho W.S., Sun S.S., Chung H.Y., Wong H.N., Ooi V.E. // Peptides. 2008. V. 29. № 12. P. 2101-2109.
59. Lin P., Xia L., Wong J.H., Ng T.B., Ye X., Wang S., Shi X. // J. Pept. Sci. 2007. V. 13. № 10. P. 642-648.
60. Zhang N., Jonnes B.L., Tao H.P. // Cereal Chem. 1997. V. 74. № 2. P. 119-122.
61. Melo F.R., Rigden D.J., Franco O.L., Mello L.V., Ary M.B., Grossi de Sa M.F., Bloch C. // Proteins. 2002. V. 48. № 2. P. 311-319.
62. Jones B.L., Marinac L.A. // J. Agric. Food Chem. 2000. V. 48. P. 257-264.
63. Sawano Y., Hatano K., Miyakawa T., Komagata H., Miyauchi Y., Yamazaki H., Tanokura M. // Plant Physiol. 2008. V. 146. № 4. P. 1909-1919.
64. Chae K., Kieslich C., Morikis D., Kim S., Lord E.M. // Plant Cell. 2009. V. 21. P. 3902-3914.
65. Zhang D., Liang W., Yin C., Zong J., Gu F., Zhang D. // Plant Physiol. 2010. V. 154. № 1. P. 149-162.
66. Cameron K.D., Teece M.A., Smart L.B. // Plant Physiol. 2006. V. 140. P. 176-183.
67. Lee S.B., Go Y.S., Bae H.J., Park J.H., Cho S.H., Cho H.J., Lee
D.S., Park O.K., Hwang I., Suh M.C. // Plant Physiol. 2009. V. 150. № 1. P. 42-54.
68. Kader J.-C. // Trends Plant Science. 1997. V. 2. № 2. P. 66-70.
69. Sterk P., Booij H., Schellekens G.A., van Kammen A., De Vries S.C. // Plant Cell. 1991. V. 3. P. 907-921.
70. Park S.Y., Jauh G.Y., Mollet J.C., Eckard K.J., Nothnagel E.A., Walling L.L., Lord E.M. // Plant Cell. 2000. V. 12. P. 151-163.
71. Ouvard O., Cellier F., Ferrare K., Tousch D., Lamaze T., Dupuis J.M., Casse-Delbart F. // Plant Mol. Biol. 1996. V. 31. P. 819-829.
72. Hincha D.K. // Phil. Trans. R. Soc. Lond. 2002. V. 357. P. 909-916.
73. Choi Y.E., Lim S., Kim H.J., Han J.Y., Lee M.H., Yang Y., Kim J.A., Kim Y.S. // Plant J. 2012. V. 70. № 3. P. 480-491.
74. Sror H.A., Tischendorf G., Sieg F., Schmitt J.M., Hincha D.K. // Cryobiology. 2003. V. 47. № 3. P. 191-203.
75. Cheng C.S., Samuel D., Liu Y.J., Shyu J.C., Lai S.M., Lin K.F., Lyu P.C. // Biochemistry. 2004. V. 43. P. 13628-13636.
76. Wang X., Wang H., Cao K., Ge X. // Mol. Biol. Rep. 2009. V. 36. P. 745-750.
77. Osman H., Vauthrin S., Mikes V., Milat M.L., Panabieres F., Marais A., Brunie S., Maume B., Ponchet M., Blein J.P. // Mol. Biol. Cell. 2001. V. 12. P. 2825-2834.
78. Kim Y.T., Oh J., Kim K.H., Uhm J.Y., Lee B.M. // Mol. Biol. Rep. 2010. V. 37. № 2. P. 717-727.
79. Douliez N., Jacquemard A., Marion D., Tran V., Maume B., Milat M., Ponchet M., Mikes V., Kader J.-C., Blein J. // FEBS Lett. 2001. V. 509. № 1. P. 27-30.
80. Maldonado A.M., Doerner P., Dixon R.A., Lamb C.J., Cameron R.K. // Nature. 2002. V. 419. № 6905. P. 399-403.
81. Lascombe M.B., Bakan B., Buhot N., Marion D., Blein J.P., Larue V., Lamb C., Prangé T. // Protein Sci. 2008. V. 17. № 9. P. 1522-1530.
82. Degli Esposti M. // Biochim. Biophys. Acta. 2002. V. 1553. № 3. P. 331-340.
83. Crimi M., Astegno A., Zoccatelli G., Esposti M.D. // Arch. Biochem. Biophys. 2006. V. 445. № 1. P. 65-71.
84. Rudrappa T., Biedrzycki M.L., Kunjeti S.G., Donofrio N.M., Czymmek K.J., Paré P.W., Bais H.P. // Commun. Integr. Biol. 2010. V. 3. № 2. P. 130-138.
85. Pii Y., Astegno A., Peroni E., Zaccardelli M., Pandolfini T., Crimi M. // Mol. Plant Microbe Interact. 2009. V. 22. № 12. P. 1577-1587.
86. Pii Y., Molesini B., Pandolfini T. // Plant Signal Behav. 2013. V. 8. № 7. e24836.
87. Tomassen M.M., Barrett D.M., van der Valk H.C., Woltering
E.J. // J. Exp. Bot. 2007. V. 58. № 5. P. 1151-1160.
88. Palacin A., Varelaw J., Quirce S., del Pozo V. // Clin. Exp. Allergy. 2009. V. 39. P. 1267-1276.
89. Salcedo G., Sanchez-Monge R., Diaz-Perales A., Garcia-Casado G., Barber D. // Clin. Exp. Allergy. 2004. V. 34. № 9. P. 1336-1341.
90. Hauser M., Roulias A., Ferreira F., Egger M. // Allergy Asthma Clin. Immunol. 2010. V. 6. № 1. P. 1-14.
91. Borges J.P., Barre A., Culerrier R., Granier C., Didier A., Rougé P // Biochem. Biophys. Res. Commun. 2008. V. 365. № 4. P. 685-690.
92. Akkerdaas J., Finkina E.I., Balandin S.V., Santos Magadán S., Knulst A., Fernandez- Rivas M., Asero R., van Ree R., Ovchin-nikova T.V. // Int. Arch. Allergy Immunol. 2012. V. 157. P. 51-57.
93. Borges J.P., Jauneau A., Brule C., Culerrier R., Barre A., Didier A., Rougé P. // Plant Physiol. Biochem. 2006. V. 44. P. 535-542.
94. Fernandez-Rivas M., Gonzalez-Mancebo E., Rodriguez-Perez R., Benito C., Sanchez-Monge R., Salcedo G., Alonso M.D., Rosado A., Tejedor M.A., Vila C., et al. // J. Allergy Clin. Immunol. 2003. V. 112. P. 789-795.
95. Egger M., Hauser M., Mari A., Ferreira F., Gadermaier G. // Curr. Allergy Asthma Rep. 2010. V. 10. № 5. P. 326-335.
96. Marzban G., Mansfeld A., Herndl A., Jäger S., Stoyanova M. E., Hemmer W., Katinger H., Laimer M. // Aerobiologia. 2006. V. 22. P. 237-245.
97. Fernández-Rivas M., Bolhaar S., González-Mancebo E., Asero R., van Leeuwen A., Bohle B., Ma Y., Ebner C., Rigby N., Sancho A.I., et al. // J. Allergy Clin. Immunol. 2006. V. 118. P. 481-488.
98. Pacios L.F., Tordesillas L., Cuesta-Herranz J., Compes E., Sánchez-Monge R., Palacín A., Salcedo G., Díaz-Perales A. // Mol. Immunol. 2008. V. 45. № 8. P. 2269-2276.
99. García-Casado G., Pacios L.F., Díaz-Perales A., Sánchez-Monge R., Lombardero M., García-Selles F.J., Polo F., Barber D., Salcedo G. // J. Allergy Clin. Immunol. 2003. V. 112. P. 599-605.
100. Salcedo G., Sanchez-Monge R., Barber D., Diaz-Perales A. // Biochim. Biophys. Acta. 2007. V. 1771. P. 781-791.
101. Tordesillas L., Cuesta-Herranz J., Gonzalez-Muñoz M., Pacios L.F., Compés E., Garcia-Carrasco B., Sanchez-Monge R., Salcedo G., Diaz-Perales A. // Mol. Immunol. 2009. V. 46. P. 722-728.
102. Schulten V., Radakovics A., Hartz C., Mari A., Vazquez-Cortes S., Fernandez-Rivas M., Lauer I., Jahn-Schmid B., Eiwegger T., Scheurer S., et al. // J. Allergy Clin. Immunol. 2009. V. 124. № 1. P. 100-107.
103. Edstam M.M., Viitanen L., Salminen T.A., Edqvist J. // Mol. Plant. 2011. V. 4. № 6. P. 947-964.
104. Boutrot F., Chantret N. Gautier M.-F. // BMC Genomics.
2008. V. 9. № 86. P. 1-19.
105. Jang C.S., Jung J.H., Yim W.C., Lee B.M., Seo Y.W., Kim W. // Mol. Cell. 2007. V. 24. № 2. P. 215-223.
106. Moore R.C., Purugganan M.D. // Curr. Opin. Plant Biol. 2005. V. 8. P. 122-128.
107. Nieuwoudt M., Lombard N., Rautenbach M. // Food Chem. 2014. V. 157. P. 559-567.
108. Safi H., Saibi W., Alaoui M.M., Hmyene A., Masmoudi K., Hanin M., Brini F. // Plant Physiol Biochem. 2015. V. 89. P. 64-75.
109. Wang F., Zang X.S., Kabir M.R., Liu K.L., Liu Z.S., Ni Z.F., Yao Y.Y., Hu Z.R., Sun Q.X., Peng H.R. // Gene. 2014. V. 550. № 1. P. 18-26.
110. Guo C., Ge X., Ma H. // Plant Mol. Biol. 2013. V. 82. № 3. P. 239-253.
111. Van Winkle R.C., Chang C. // Clin. Rev. Allergy Immunol. 2014. V. 46. № 3. P. 211-224.
112. Bidad K., Nicknam M.H., Farid R. // Iran J. Allergy Asthma Immunol. 2011. V. 10. № 1. P. 1-9.
113. Mutschlechner S., Deifl S., Bohle B. // Clin. Exp. Allergy.
2009. V. 39. № 11. P. 1635-1642.
114. Cromwell O., Häfner D., Nandy A. // J. Allergy Clin. Immunol. 2011. V. 127. № 4. P. 865-872.
115. Bonura A., Passantino R., Costa M.A., Montana G., Melis M., Bondi M.L., Butteroni C., Barletta B., Corinti S., Di Felice G., et al. // Clin. Exp. Allergy. 2012. V. 42. № 3. P. 471-480.
116. Gómez-Casado C., Garrido-Arandia M., Gamboa P., Blanca-López N., Canto G., Varela J., Cuesta-Herranz J., Pacios L.F., Díaz-Perales A., Tordesillas L. // Clin. Dev. Immunol. 2013.
V. 2013. P. 1-12.
10 лучших источников белка на основе растений
Когда вы слышите слово «белок», вы, вероятно, думаете о куриной грудке или куске стейка. В этом есть смысл — по данным Heart Foundation, мясо является одним из лучших источников этого макроэлемента. Но это не , а только источник . Фактически, вполне возможно получать необходимый вам белок каждый день, не употребляя в пищу мясо птицы, говядины и свинины. «Когда все сделано вдумчиво, люди могут удовлетворить свои потребности в белке исключительно из растительных источников», — говорит Натали Сешнс, доктор медицинских наук, из методистской больницы Хьюстона в Техасе.
Возможные преимущества обмена мясного протеина на растительный протеинОдним из преимуществ употребления в пищу животного протеина является то, что эти источники являются полноценными, то есть содержат девять незаменимых аминокислот, которые наш организм не может вырабатывать, согласно Cedars-Sinai Блог. Но есть свои преимущества в торговле или сокращении потребления мяса и восполнении растительных белков, в том числе:
Похудение При правильном соблюдении растительные диеты, такие как вегетарианская диета, могут помочь вам похудеть. обзор 12 рандомизированных контролируемых испытаний, опубликованных в январе 2016 г. в журнале Journal of General Internal Medicine .
Помогая окружающей среде Замена мяса растениями для получения протеина может также принести пользу окружающей среде, отмечается в статье, опубликованной в декабре 2018 года в Nutrients .
Укрепление здоровья сердца Когда дело доходит до красного мяса, преимущества растительной альтернативы белку, возможно, становятся еще более впечатляющими. «Некоторые исследования связывают красное мясо с повышенным риском сердечных заболеваний и диабета 2 типа, отчасти из-за содержания насыщенных жиров», — говорит Сешнс.
Фактически, рандомизированное контролируемое исследование, опубликованное в июне 2019 года в American Journal of Clinical Nutrition , показало, что среди диет с красным мясом, диет с белым мясом и диет с растениями наиболее положительные эффекты имели растительные диеты. на уровень ЛПНП или «плохого» холестерина. Согласно Американской кардиологической ассоциации, замена насыщенных жиров более здоровыми жирами, такими как полиненасыщенные и мононенасыщенные жиры, может улучшить уровень липидов и холестерина.
Между тем, другие исследования, такие как метаанализ, опубликованный в апреле 2014 года в JAMA Internal Medicine , показывают, что по сравнению с всеядными людьми, сидящими на диете (теми, кто ест и растительный, и животный белки), у вегетарианцев показатели диастолического и систолического артериального давления ниже.По данным Центров по контролю и профилактике заболеваний, эти преимущества могут привести к более здоровому тикеру и снизить риск сердечных заболеваний.
Продление жизни Национальный институт здоровья сообщает, что потребление красного мяса может сократить вашу жизнь. Группа рекомендует заменить его из своего рациона на более здоровые источники белка.
Соблюдая диету с разнообразными продуктами, можно получить фиксированное количество аминокислот, необходимых вашему организму для наилучшей работы, отмечает Cedars-Sinai.
«Никому не нужно есть красное мясо, чтобы быть здоровым», — говорит Сешнс.
СВЯЗАННЫЙ: 9 лучших веганских блогов о еде для растительного вдохновения
«Сколько протеина мне нужно?»По данным Harvard Health Publishing, рекомендуемая суточная доза белка составляет 0,8 грамма (г) на килограмм массы тела. Умножьте свой вес в фунтах (фунтах) на 0,36 — это то, сколько граммов белка вы должны получать как минимум каждый день.Таким образом, если вы весите 150 фунтов, вы стремитесь получать 54 г белка в день. Другими словами, белок должен составлять от 10 до 35 процентов ежедневного потребления калорий, говорит Шира Сусси, RDN, основательница Shira Sussi Nutrition в Бруклине, Нью-Йорк.
Это несложный вопрос для большинства американцев. «Нас не очень беспокоит получение достаточного количества белка — большинство американцев соблюдают или превышают рекомендованное потребление», — говорит Сешнс. «Во многих случаях, которые я видел при работе с клиентами и пациентами, они переусердствовали с потреблением белка, а также недооценивали рекомендуемое потребление богатых питательными веществами овощей, фруктов и цельнозерновых продуктов.
Сусси подозревает, что это потому, что «люди воспитаны с идеей, что белок, особенно животный белок, должен быть в центре еды, и что еда без белка не приносит удовлетворения и не приносит удовлетворения». Она оспаривает это мышление и говорит, что за ужином не обязательно должен быть большой кусок мяса. По словам Сусси, вы можете решить проблему, добавляя высококачественный белок в блюда и закуски в течение дня, например, добавляя порцию бобов в салат или укладывая жареные стейки тофу между ломтиками хлеба на обед.
СВЯЗАННЫЕ: 9 инстаграммеров, любящих овощи, которые вдохновят вас на цели растительной диеты
Готовы изучить растительную сторону белка? Вот 10 лучших белков растительного происхождения, которые стоит включать в свой рацион, независимо от того, хотите ли вы полностью отказаться от продуктов животного происхождения или просто хотите разнообразить свои белковые варианты.
Растительные белки — обзор
1.3.3 Тенденции развития продуктов
Растительные белки также могут входить в состав «продуктов свободы», как заявил Кристофер Шанахан, руководитель глобальной программы Frost & Sullivan (Gelski, 2015).В частности, «пища свободы» не ограничивается опасениями, касающимися болезней человека, благополучия животных и безопасности пищевых продуктов, специфичных для белков животного происхождения. Фактически, растительные белки из зернобобовых, семян и злаков играют важную роль в продуктах «свобода», «бесплатные» и «полезные для вас». От пяти до десяти или более граммов растительного белка на порцию часто добавляют во многие продукты, напитки и здоровые закуски. Растительные белки обычно связаны с энергией; а на этикетках могут быть такие слова, как «протеин, получаемый из растений», «питаемый», «заряженный энергией» и «питаемый энергией».«Растительные белки были проданы, чтобы предложить« заряд »белка для энергичных тренировок, а также для хорошего завтрака и наиболее важной части дня, чтобы вы продолжали двигаться. Растительные белки, которые недавно были выделены таким образом, включают горох и другие бобовые, семена подсолнечника и тыквы, кешью, миндаль, амарант, киноа, орехи макадамия, семена кунжута, фундук и грецкие орехи. Прежде всего, соевый белок напрямую связан со здоровьем сердца. Согласно Своду федеральных правил США, раздел 21, 101.82 следующее заявление о пользе для здоровья может быть сделано в отношении пищевого продукта, содержащего не менее 6,25 г соевого белка на эталонное количество этого продукта питания: «В рамках диеты с низким содержанием насыщенных жиров и холестерина 25 г соевого белка в день может снизить риск сердечных заболеваний ». На таком продукте, как этот, можно также найти этикетку, украшенную такими словами, как «здоровье сердца» и «белок, полезный для сердца».
Многие растительные порошки, напитки и заменители еды сегодня имеют рекламу на этикетках, обращенных к потребителю, например, «растительный белок», «органический растительный белок», «веганский», «зеленый протеиновый порошок», «суперпродукты». , »« Полноценный и сбалансированный белок »и / или« здоровая альтернатива ».«Продукты на растительной основе также продаются, чтобы разрушить потенциальные потребительские барьеры для входа на рынок. Например, растительные продукты привлекают особое внимание при сравнении кальция с молочным молоком или уровнями омега-жирных кислот по сравнению с лососем. Кроме того, растительные белки в виде проросших зерен и семян с повышенной ферментативной активностью становятся все более популярными из-за связи с лечением болезней, помощи в пищеварении, усвоении питательных веществ и повышенной плотности белка и питательных веществ. Проросшие семена включают, помимо прочего, тыкву, арбуз, чиа, лен, коноплю и подсолнечник.На веб-сайтах и в средствах массовой информации растительный белок рекламируется как будущее белка. Хотя лидерами этого движения являются чечевица, зерна и орехи в цельных или минимально обработанных формах, есть некоторые соображения, которые тратятся на мясные и молочные аналоги (как правило, аналоги представляют собой сильно переработанные растительные ингредиенты, созданные для имитации продуктов животного происхождения). Часто производители мясных аналогов на растительной основе проводят интенсивные маркетинговые кампании, призывающие мясную промышленность к проблемам благополучия животных и убойного убоя, проблемам безопасности пищевых продуктов, экологическим проблемам с животноводством, изменению климата и нехватке воды, использованию антибиотиков и гормонов роста и негативным последствиям. влияние холестерина и насыщенных жиров на здоровье.
Была обнаружена корреляция между западными диетами с высоким содержанием мяса, рафинированного сахара и жиров, что вредно как для человека, так и для всей планеты (Tilman & Clark, 2014). Экологи Тилман и Кларк подсчитали, что к 2050 году производство продуктов питания для таких рационов приведет к 80% увеличению глобальных выбросов парниковых газов в сельском хозяйстве. Производство продуктов питания по западному образцу уже нанесло ущерб, включая вырубку лесов в слаборазвитых странах. Текущий растущий спрос на западные продукты питания приведет к увеличению расчистки земель для производства мяса и основных масличных культур сои и пальмы.Исследование Тилмана и Кларка быстро разрослось в статьях в СМИ, в которых западные диеты считались вредными для здоровья человека и окружающей среды (Healy, 2014; Skirble, 2014). Следовательно, замена традиционных диет диетами западного типа нецелесообразна. Этот сдвиг в питании сопровождался ростом заболеваемости диабетом 2 типа, ишемической болезнью сердца и другими хроническими западными заболеваниями. Глобальная трилемма плохого питания, здоровья и окружающей среды потребует решений в области питания, политики и бизнеса. Эта трилемма, вероятно, будет усугублена прогнозируемым увеличением мирового населения на 30% в следующие 30 лет и еще на 10% к началу века.Выращивание питательной пищи для этого большого числа людей станет жизненно важным. Ниже мы обсудим, как человечество может справиться с этой ситуацией и подготовиться к критическому выбору.
Моделирование для понимания взаимосвязей между структурой и функцией растительного белка — значение для белков-хранилищ семян
Abstract
Белки являются одними из самых важных молекул на Земле. Их структура и агрегационное поведение являются ключом к их функциональности в живых организмах и в продуктах, богатых белком.Инновации, такие как увеличенный размер и мощность компьютера, вместе с новыми инструментами моделирования, улучшили наше понимание взаимосвязей между структурой белка и функцией. В этом обзоре рассматриваются различные белки, присутствующие в растениях, и инструменты моделирования, которые можно применять для лучшего понимания белковых структур и их взаимосвязи с функциональностью, с особым акцентом на запасных белках растений. Моделирование растительных белков расширяется, но менее 9% депозитов в Исследовательском коллаборации структурной биоинформатики белковых данных поступают из растительных белков.Хотя применяются те же инструменты, что и для других белков, моделирование растительных белков отстает, а инновационные методы используются редко. Молекулярная динамика и молекулярный докинг обычно используются для оценки различий в формах или мутантах и их влияния на функциональность. Инструменты моделирования также использовались для описания фотосинтетического механизма и его реакций переноса электронов. Запасные белки, особенно в больших и изначально неупорядоченных проламинах и глютелинах, были значительно менее хорошо описаны с помощью моделирования.Эти белки агрегируются во время обработки и образуют большие полимеры, которые соотносятся с функциональностью. Полученные в результате взаимосвязи структура-функция важны для обработанных запасных белков, поэтому моделирование и имитационные исследования с использованием современных моделей, алгоритмов и компьютерных инструментов необходимы для лучшего понимания этих взаимосвязей.
Ключевые слова: альбумин, глобулин, глутелин, моделирование Монте-Карло, моделирование молекулярной динамики, проламин
1.Введение — Растительные белки: типы, характеристики и наличие
1.1. Разнообразие растительных белков и их функции
Белки — это биологические макромолекулы, которые отвечают за большинство биологических ролей (иногда вместе с другими биомолекулами) в клетке. Таким образом, белки можно рассматривать как биомолекулярные устройства с естественными структурными и функциональными свойствами, которые часто сложно воссоздать в лаборатории. Некоторыми классическими примерами белков с исключительными функциями являются белки шелка паука, сочетающие в себе очень высокую прочность с превосходной эластичностью [1], и бактериальные жгутики, которые представляют собой микроскопические пропеллеры [2].Белки в форме ферментов катализируют реакции с большой скоростью и высокой селективностью.
Подобно белкам в целом, растительные белки играют различные ферментативные, структурные и функциональные роли (фотосинтез, биосинтез, транспорт, иммунитет и т. Д.). Они также действуют как среда для хранения, чтобы удовлетворить потребности развивающихся сеянцев в росте и питании. Белки выполняют эти функции в своем составе и определенных структурных формах, например, посредством складывания, которое может варьироваться от компактного и хорошо упорядоченного до развернутого и внутренне неупорядоченного.
1.2. Классификация растительных белков — взаимосвязь с запасными белками семян
Первые попытки классифицировать растительные белки были основаны на экстрагируемости и растворимости этих белков, при этом первое систематическое исследование запасных белков семян было проведено T.B. Осборн, применив схему классификации, предложенную Американским комитетом по номенклатуре белков [3]. Эта номенклатура в основном классифицирует белки на три типа; простые, сопряженные и производные. Белки во всех тканях растений классифицируются как простые белки, которые делятся на четыре типа [4] ().Эти четыре типа растительных белков в основном связаны с запасными белками семян и известны как альбумины, глобулины, проламины и глютелины, разделенные на основе фракционирования Осборна водой, солью, спиртом и щелочью соответственно (). Позднее были предприняты попытки более сложных классификаций растительных белков, основанных, например, на их химической структуре, механизме / механизмах действия, биологической функции или местонахождении внутри растения. Несмотря на эти попытки использовать более современные системы классификации, классификация Осборна по-прежнему остается наиболее широко используемой системой, особенно используемой для процедур экстракции и очистки белков [5].Однако на практике классификация Осборна использовалась только для запасных белков семян, тогда как классификация других растительных белков обычно более сложна и иногда неясна.
Таблица 1
Типы, характеристики (на основе фракционирования по Осборну [3,4]) и наличие растительных белков.
| Тип протеина | Растворимость | Характеристики | Примеры в растениях | Ссылки (примеры) |
|---|---|---|---|---|
| Альбумины | Вода | Шаровидный тип 2, коагулянт | е.г., Лейцин, Легумалин, Фазелин, Рицин | [4,5,6] |
| Глобулины | Солевой раствор | Шаровидный, с более высокой молекулярной массой, чем альбумины | 7S вицилинового типа (горох, соя и т. д.) ) 11S бобового типа (капуста, овес, рис) | [4,7] |
| Проламины | Смеси спирт / вода (например, 70% этанол) | Внутримолекулярные дисульфидные связи, высокая доля пролина и глутамин, повторяющиеся мотивы в центральных доменах | Глиадины, зеин, гордеин, секалин | [4,7,8,9,10] |
| Глютелины | Щелочные растворы | Межмолекулярные дисульфидные связи, высокая доля пролин и глутамин, повторяющиеся мотивы в центральных доменах | Глютенины в пшенице | [4,7,8,9,10,11] |
1.3. Характеристика и наличие белков, классифицированных по осборну.
Альбумины определяются как водорастворимые глобулярные белки, коагулирующие при нагревании (). Наиболее известные альбумины — это сывороточный альбумин, основной белок в крови человека, и яичный белок. В растениях альбумин присутствует в семенах в виде запасного белка 2S-альбумина, например, в виде лейцина в ячмене, пшенице и ржи, в виде бобумелина в горохе, сое и вигне, в виде фазелина в фасоли и в виде рицина в клещевине [6 ] (). Многие белки в тканях зеленых растений, в том числе рибулозо-1,5-бисфосфаткарбоксилаза оксигеназа (RuBisCO), фермент, катализирующий первую стадию фиксации углерода и самый распространенный белок на Земле, не определяются как альбумины, несмотря на то, что они водорастворимы. .RuBisCO растворим в воде и коагулирует под действием тепла [12], что, по определению Осборна, должно сделать его белком альбумина. Точно так же большинство ферментативных белков в растениях растворимы в воде и коагулируются под действием тепла, но, кроме того, что они были охарактеризованы как ферменты, они не были далее определены в тип белка.
Глобулины также являются глобулярными белками, которые имеют более высокий молекулярный вес, чем альбумины, и растворимы в разбавленном солевом растворе, но не растворимы в воде (). Самый известный глобулин — это главный белок крови человека (сывороточный гамма-глобулин) [13].У растений глобулины присутствуют в качестве запасных белков как у двудольных, так и у однодольных, что делает их наиболее распространенной группой запасных белков [7]. Основываясь на коэффициенте седиментации, глобулины-накопители растений в основном делятся на две группы: 7S-вицилиновый тип, который был обнаружен и широко изучен в горохе, сое и т. Д., И 11S-бобовый тип, который, например, является основным хранилищем. белок в большинстве бобовых и двудольных растений, таких как капуста, овес и рис [7] (). Некоторые белки листьев растений явно не растворимы в воде и могут быть классифицированы как глобулины в некоторых характеристиках белков листьев [14].Однако причина того, что эти белки листа не растворимы в воде, может заключаться в том, что они связаны с клеточной стенкой, взаимодействуют с пектином или являются гидрофобными [15], и поэтому их, очевидно, нелегко отнести к категории глобулинов или альбуминов.
Два дополнительных типа протеина, проламины и глютелины, обнаруживаются, в частности, в качестве запасных протеинов в семенах семейства злаковых (Triticeae), где они являются доминирующими протеинами, составляющими до 85% от общего протеина [7] (). Проламины, содержащиеся в пшенице, называются глиадинами, тогда как номенклатура проламинов в других злаках основана на их латинских названиях; зеин в кукурузе, гордеин в ячмене, секалин в ржи и т. д.[8] (). Чаще всего глютелин содержится в пшенице (глютенин), хотя глютелин также присутствует в ячмене и ржи [11] (). Проламины и глютелины имеют несколько общих черт, включая высокую долю пролина и глутамина и высокую долю повторяющихся мотивов или последовательностей с неповторяющимися доменами на их N- и C-концах [8]. Хотя эти белки различаются по молярной массе, основное различие между двумя типами белков заключается в образовании внутри- и межмолекулярных дисульфидных связей в нативном состоянии проламинов и глутелинов соответственно [9], что объясняет различия в их экстрагируемости. .
1,4. Запасные белки семян — типы и характеристики
Из предыдущих разделов ясно, что запасные белки семян присутствуют в семенах в различных типах, включая альбумин, глобулин, проламин и глютелин [6,7,8]. Эти белки могут иметь разные характеристики в растительной клетке, а также во время обработки и для различных применений, где запасные белки вносят вклад в функциональность. Однако на сегодняшний день запасные белки семян в основном охарактеризованы на основе их химических свойств во время фракционирования, осаждения и т. Д.[4,6,7,8]
2. Функциональные возможности растительных белков — в растениях, а также в пищевых продуктах и промышленности
2.1. Функция растительных белков в растении
Растительные белки удовлетворяют потребности проростков в питании и росте благодаря своим ферментативным, структурным, функциональным и запасающим функциям [16]. Растения содержат ряд определенных типов белков, которых нет в других живых организмах, и они выполняют определенные функции (). Например, у большинства растений есть какой-либо запасной орган (семена, клубни и т. Д.).) для размножения, где хранятся различные источники питательных веществ, чтобы у нового растения были ресурсы для роста в предстоящий сезон. Белки, углеводы и масла — это различные типы источников питательных веществ, которые накапливаются в органах хранения растений. Такие белки обычно называют запасными белками (). Их основная функция — расщепляться на аминокислоты, чтобы сформировать необходимые строительные блоки для появляющихся белков в растении следующего поколения [17]. Клетка растения содержит ряд органелл, в том числе хлоропласт, ответственных за фотосинтез ().У растений также есть специфический белок, фермент RuBisCO (), который катализирует передачу солнечной энергии в химическую энергию, которая может быть использована растением, посредством фиксации CO 2 [18].
Таблица 2
Примеры растительных белков с их уникальными функциями в растениях, пищевых и непищевых продуктах
| Использование | Тип белка (Примеры) | Возникновение (Примеры) | Функция (Примеры) | Ссылки (Примеры) |
|---|---|---|---|---|
| Живые растения | Запасные белки | Семена, клубни | Рост и питание рассады и проростков | [16,17] |
| Фотосинтез | ||||
| Белки плазматической мембраны e.g., поверхностные белки, глобулярные белки | Клеточная мембрана, Белковые каналы | Транспорт, структурная поддержка, ионная регуляция | [16,18] | |
| Пищевые продукты | Вицилин | Горох | Эмульгирование гелеобразования при нагревании свойства | [19,20,21,22] |
| Биологические материалы | Глютенины | Пшеница | Когезивная матрица, газовый барьер, прочность | [10,23,24,25,26,27, 28,29,30,31,32,33,34] |
| Глиадины | Пшеница | Связная матрица, газовый барьер, гибкость |
2.2. Функции растительных белков в пищевых продуктах
В пищевых продуктах белки часто являются основным функциональным компонентом, особенно в обработанных пищевых продуктах с высоким содержанием белка [19]. В таких продуктах белки вносят свой вклад в питание, а также в качество, текстуру, аромат, вкус, чувство сытости и простоту обработки [20] (). Большинство растительных белков обладают характеристиками, которые делают их интересными при переработке пищевых продуктов, хотя их конкретные характеристики могут отличаться. Например, было показано, что вицилин горохового белка обладает лучшими свойствами гелеобразования и эмульгирования, вызванными нагреванием, чем бобовые гороха, которые, как было обнаружено, более питательны для человека [21].Эффективность различных растительных белков для пищевых продуктов сильно зависит от их структурных особенностей и их способности образовывать определенные трехмерные (3D) конфигурации / конформации, а также их способности к сшиванию [10,22].
2.3. Функции растительных белков в промышленных приложениях
Растительные белки также обладают свойствами, которые делают их интересными для использования в качестве материалов (). Ряд растительных белков, включая в основном запасные белки, например, из пшеницы, сои, картофеля и масличных культур, обладают интересными свойствами для таких применений, как упаковка, огнестойкие и абсорбирующие материалы [23,24,25,26,27,28,29 , 30] ().Способность белков к сшиванию и агрегации важна для хороших свойств материала на основе белка [10,31,32,33].
2.4. Влияние запасных белков семян на функциональность
Приведенные выше описания ясно показывают первостепенное значение запасных белков в растениях как источника аминокислот, которые будут использоваться в качестве строительных блоков для развивающихся молодых проростков при появлении всходов [17]. В пищевых продуктах и в промышленности запасные белки семян играют центральную роль в обеспечении функциональности [19,20,21,22,23,24,25,26,27,28,29,30], поэтому важно понимать, как функционирует подвержены влиянию и могут быть настроены [35,36,37].
3. Моделирование — современное состояние растительных белков
3.1. Основа для моделирования структур белков
Как описано выше, трехмерная (3D) -конформация нативных белков вместе с их способностью сшивать, изменять форму и формировать определенные структурные особенности вносят существенный вклад в функциональные свойства конкретных белков. в растении и в растительных продуктах [31,34,38]. По сути, методы определения структуры белков можно разделить на три типа:е., основанные на различных типах методов микроскопии, основанные на рассеянии / дифракции и спектроскопии (например, методы рентгеновского и ядерного магнитного резонанса (ЯМР)), и основанные на моделировании [39] (). В этом обзоре мы сосредоточимся на возможностях и недостатках использования моделирования для определения структур растительных белков, уделяя особое внимание запасным белкам растений.
Таблица 3
Методы, используемые для определения структур белков и взаимосвязей между структурой и функцией.
| Тип метода | Метод (Примеры) | Используется для / приложений (Примеры) | Ссылки (Примеры) |
|---|---|---|---|
| Микроскопия | Трансмиссионная электронная микроскопия (TEM119) | (3D) структура белков из 2D изображений частиц | [39,48] |
| Крио-электронная микроскопия (Cryo-EM) | 3D-структура биомакромолекул в нативном состоянии | [39,49] | |
| Томография | 3D-изображения высокого разрешения | [50] | |
| Визуализация | Изображения отдельных белков с помощью низкоэлектронной голографии | [50,51] | |
| Рассеяние / дифракция, ядерная магнитная спектроскопия | резонансная спектроскопия (ЯМР)Химические сдвиги, отражающие конформации белков | [52] | |
| Малоугловые рентгеновские лучи рассеяние | Форма, конформация и сборка белков | [53] | |
| Широкоугольное рентгеновское рассеяние | Характеристика структурных моделей, сходства и изменений в атомной упаковке | [54] | |
| Фурье Инфракрасная спектроскопия с преобразованием (FT-IR) | Конформация белка путем подбора пика амидных полос | [39,55] | |
| Рентгеновская кристаллография | Атомное разрешение трехмерных структур белка | [56] | |
| Моделирование-имитация | На основе шаблона | Моделирование на основе гомологии | [34] |
| Ab initio | Моделирование основано только на информации о последовательности | [40,41] | |
| Монте-Карло (MC) | Статистический метод оценки движений белка | [42,43] | |
| Молекулярная динамика (MD) | Решение уравнения Ньютона уравнение движения | [43] | |
| Машинное обучение (AlphaFold) | Искусственная нейронная сеть | [45,46,47] |
3.2. Моделирование на основе шаблонов и Ab Initio
Методы, применяемые для моделирования структур растительных белков, аналогичны тем, которые используются для любого типа белка (). Моделирование на основе шаблонов — это наиболее упрощенный метод моделирования белков. Модели на основе шаблонов построены на сравнении аминокислотных последовательностей белков с известными белковыми структурами (часто идентифицируемыми с помощью кристаллографии) и предположении, что аналогичные последовательности приводят к одинаковым структурам белков [40]. Однако многие белки не имеют сходства последовательностей с другими белками, уже присутствующими в базах данных, и с известными структурами.Для таких белков (не показывающих взаимосвязи с известными белками) моделирование только на основе информации о последовательности, то есть предсказание структуры белка ab initio, является единственным вариантом. В предсказаниях ab initio термодинамические принципы применяются к случаю конформации белка посредством поиска общего минимума энергии [40].
3.3. Монте-Карло, молекулярная динамика и методы машинного обучения
Два более продвинутых / современных метода, Монте-Карло (MC) и молекулярная динамика (MD), были разработаны в последние годы для предсказания и моделирования структуры белков.Оба метода напоминают подход ab initio, поскольку моделирование основано только на информации о последовательности. (). Оба метода можно применять в разных масштабах с разной степенью детализации; от полностью атома и объединенного атома к крупнозернистым моделям [41]. Преимущество вычислений MC состоит в том, что их выполнять быстрее и проще, чем вычисления MD, из-за того, что они свободны от ограничений, связанных с решением уравнения движения Ньютона [42] (). Однако это также влияет на результаты, поскольку из прогона MC не собирается «динамическая» информация [42,43].Таким образом, в нескольких моделированиях белков MC была объединена с MD [44]. Более того, современные методы машинного обучения, такие как алгоритм AlphaFold, позволили значительно продвинуться в предсказании структуры белка на основе информации о последовательностях [45]. В последних экспериментах по критической оценке предсказания структуры белка (CASP) 3D-модели белков AlphaFold были помещены на первое место в категории «Бесплатное моделирование» с точки зрения точности [46]. Алгоритм AlphaFold использует искусственные нейронные сети для создания библиотеки специфичных для белков фрагментов [47].Однако алгоритмы, такие как AlphaFold, еще не применялись для прогнозирования структуры запасных белков семян, вероятно, потому, что эти алгоритмы обычно предсказывают белковые структуры на основе сворачивания, в то время как некоторые из наиболее полезных запасных белков изначально неупорядочены.
3.4. Моделирование растительных белков с особым акцентом на запасных белках семян
Область исследований по моделированию растительных белков сравнительно небольшая и относительно новая, с ограниченным количеством связанных с растениями депозитов в Исследовательском сотрудничестве по структурной биоинформатике банка данных белков (RCSB PDB).Поиск месторождений растений в настоящее время дает 2300 результатов, четверть из которых — от Arabidopsis. Сортировка, основанная на наиболее распространенных организмах, показывает 1382 попадания на Arabidopsis и 15000 попаданий на другие (другие = организмы растительного происхождения, но также и дополнительные организмы) в общей сложности более 160 000 общих отложений (большинство поступает от людей и микроорганизмов) [57]. Одна треть залежей в текущем поиске растений относится к 2015 году и позже. Для запасных белков семян доступно только 47 отложений, большинство из которых составляют глобулины, а остальные — альбумины.Эти отложения указывают на то, что моделирование растительных белков было сосредоточено на определенных областях. Это также отражено в информации в PDB RCSB, где доступно большое количество отложений, например, в белках, связанных с механизмом фотосинтеза, белках, связанных с рибосомами, ферментами, стрессом и защитой, а также для аллергенов и сладких на вкус. белки [57]. Моделирование растительных белков в этих различных областях кратко изложено в Разделе 4.1, Разделе 4.2, Разделе 4.3, Разделе 4.4, Разделе 4.5 и раздел 4.6, чтобы определить возможности, актуальные для моделирования запасных белков семян.
4. Основные области моделирования растительных белков и влияние на моделирование запасных белков семян
Подходы к моделированию шести наиболее распространенных растительных белков в RCSB PDF описаны ниже. Запасные белки семян не входят в их число, хотя знания, полученные из других областей исследований, могут иметь отношение к моделированию запасных белков семян.
4.1. Фотосинтетическое оборудование
Фотосинтетическое оборудование отвечает за передачу солнечной энергии в химическую энергию посредством фиксации CO 2 [18].Таким образом, это одна из наиболее важных и специфических черт растений, которая давно привлекает интерес научного сообщества. Моделирование методом МД, дополненное квантово-механическими описаниями, применялось уже в начале 1990-х годов для описания того, как перенос электронов контролируется движением белка в фотосинтетических реакционных центрах [58]. С тех пор моделирование молекулярной динамики способствовало пониманию того, что движение белка в реакционных центрах является ключом к кинетике первичной реакции переноса электрона [59].Чтобы понять все механизмы фотосинтетического аппарата, был принят ряд как аналитических, так и имитационных методов, как недавно сделал обзор Блумберже [60,61]. Инструменты для оценки перемещений белков в реакционных центрах могут быть полезны для исследования перемещений запасных белков семян во время обработки и передачи динамики / энергии для этих перемещений. Структура RuBisCO, а также дивергентных, мутантных и гибридных форм этого фермента охарактеризована с помощью рентгеновской кристаллографии [62].Моделирование молекулярной динамики также использовалось для объяснения вариаций в функциональности мутантов RuBisCO, где было обнаружено использование структурных контрольных точек, позволяющих точно настроить динамику фермента [63]. Точно так же динамику запасных белков семян, уже охарактеризованную экспериментальными методами, такими как рентгеновская кристаллография, можно понять с помощью методов компьютерного моделирования.
4.2. Белки, ассоциированные с рибосомами
Крио-ЭМ-исследования в сочетании с рентгеновской кристаллографией были применены для определения структуры рибосом, создания статических моделей для различных состояний рибосом.Недавно компьютерные исследования, включающие моделирование, оказались успешными в проливании света на структурные флуктуации и переходы между различными рибосомными конфигурациями [64]. Успехи в моделировании МД, включая крупномасштабное МД, являются одним из объяснений успешного моделирования больших макромолекулярных комплексов, таких как рибосомы [65]. Размер некоторых запасных белков семян создает проблемы при их моделировании, что приводит к сходству с моделированием рибосом. Таким образом, использование крупномасштабных МД может быть альтернативой для моделирования запасных белков семян.
4.3. Ферменты
Подходы к математическому моделированию долгое время были полезным инструментом для исследования сложности метаболических сетей и их ферментативной регуляции, в то время как более современные модели внесли большой вклад в растущую область системной биологии [66]. Чаще всего для изучения регуляции ферментов применялись ферментно-кинетические модели [66], хотя в последнее время для аналогичных целей использовались методы MD и моделирование молекулярной стыковки [67]. Ферментно-кинетическое моделирование метаболических путей существенно отличается от моделирования структур и функций запасных белков семян.
4.4. Стресс и защита
Что касается белков стресса и защитных механизмов, моделирование было использовано для лучшего понимания задействованных механизмов [68,69,70,71]. Опять же, недавнее использование МД-моделирования улучшило наше понимание этих белков. Как моделирование гомологии, так и моделирование методом МД использовались для изучения фона устойчивости растений к гербицидам [72]. Гомологическое моделирование, молекулярная стыковка и моделирование МД использовались для оценки различий в конформациях белков, вносящих вклад в устойчивость, по сравнению с реакциями восприимчивости растений к различным заболеваниям [73].Наибольшее значение для моделирования запасных белков семян имеет методология, описывающая различия в конформации белков, связанные с различными функциями и функциональными возможностями.
4.5. Аллергены
Аллергенами часто являются белки [74], а растения содержат множество аллергенов, на которые чувствительные люди проявляют аллергические реакции [75]. Белки растений, ответственные за аллергические реакции, были структурно смоделированы с использованием кристаллографии, рассеяния рентгеновских лучей и ЯМР, а также стыковочного моделирования моделей белков с аналогичной последовательностью [76,77].Кроме того, была определена трехмерная кристаллическая структура различных белков аллергии растительного происхождения, а моделирование МД было использовано для обнаружения молекулярных конформаций белков, участвующих в аллергических реакциях [78,79,80]. Некоторые аллергены растительного происхождения также являются запасными белками семян в растениях, поэтому моделирование, проведенное на аллергенах, можно напрямую перенести на исследования запасных белков семян и взаимосвязей между структурой и функцией.
4.6. Белки сладкого вкуса
Белки сладкого вкуса — это специфические растительные белки, представляющие большой интерес, поскольку они обладают характеристиками, делающими их в сотни или тысячи раз слаще по вкусу, чем сахар [81,82].Несколько исследований были сосредоточены на изучении этого свойства с использованием таких методов, как кристаллизация белков и определение их структуры с помощью ЯМР и рентгеновской кристаллографии [81,83]. Сравнительное / гомологическое моделирование и методы молекулярного стыковки использовались для предсказания трехмерных структур димерных и тетрамерных форм некоторых сладких белков, в то время как влияние pH на конформацию белков оценивалось с использованием МД-моделирования [82]. МД-моделирование также использовалось в качестве инструмента структурно-ориентированной белковой инженерии для разработки улучшенных низкокалорийных подсластителей на растительной основе для фармацевтического и пищевого применения [84].Методы, применяемые для понимания структурно-функционального поведения, и методы, используемые для структурно-ориентированной инженерии, могут представлять интерес для исследований и приложений семян запасных белков.
5. Понимание взаимосвязи между структурой и функцией запасных белков семян
Запасные белки растений, вероятно, являются второй по распространенности группой белков в растениях (после RuBisCO). У всех растений, содержащих запасные органы, такие как зерна и семена, функция запасных белков заключается в хранении аминокислот, необходимых для роста и развития проростков [85].С этими белками было проведено немного исследований с помощью инструментов моделирования, несмотря на обилие запасных белков растений, их важность как источника питания для формирующегося молодого ростка [85] и их влияние на функциональность продуктов из растительных зерен [10, 22,23,86,87,88,89]. Однако методы биоинформатики все чаще используются для классификации различных белков растений, при этом нейронные сети демонстрируют точность 95,3% при классификации белков риса по различным классам (альбумины, глобулины, проламины, глютелины) [90].Кроме того, алгоритмы машинного обучения успешно использовались для классификации запасных белков семян риса, пшеницы, кукурузы, клещевины и кресс-салата на их классы [91]. Структурно различные классы запасных белков семян можно разделить на два типа: альбумины / глобулины и проламины / глютелины (). Альбумины и глобулины, как правило, сильно структурированы и поэтому способны кристаллизоваться, и их сворачивание можно моделировать с помощью ряда методов, включая машинное обучение и моделирование ab initio [92,93,94,95,96,97,98] ().Большинство проламинов и глютелинов вместо этого по своей природе неупорядочены [99] и, таким образом, создают больше проблем при моделировании. Им потребуются алгоритмы на основе MC и MD для моделирования их структур, хотя методы малоуглового рассеяния в сочетании с инфракрасной спектроскопией (ИК) и высокоэффективной жидкостной хроматографией (ВЭЖХ) также применялись для изучения структурных изменений во время обработки [100,101,102,103,104] .
Отдельные субъединицы и полимеры, полученные из них (слева направо): запасные белки 7S-глобулин в сое, 11S-глобулин в горохе, α-глиадин в пшенице и субъединицы низкомолекулярного глютенина (LMW-GS) в пшенице.Аминокислотные последовательности и инструменты моделирования, применяемые для определения структур, описаны в Yoshizawa et al. [107] и Исследовательское объединение банка данных по структурной биоинформатике (RCSB PDB) (3AUP) [39] для 7S глобулина, а также в Tandang-Silvas et al. [108] и RSCB PDB (3KSC) [39] для 11S глобулина. Последовательности аминокислот для a-глиадина и LMW-GS можно найти по номерам доступа Uniprot {«type»: «entrez-protein», «attrs»: {«text»: «Q9ZP09», «term_id»: «75267695», «term_text»: «Q9ZP09»}} Q9ZP09 и {«type»: «entrez-protein», «attrs»: {«text»: «P10386», «term_id»: «121457», «term_text»: «P10386» }} P10386 и моделирование проводилось с использованием полностью атомной модели с алгоритмами Монте-Карло в программе Profasi [126].Все модели были визуализированы с помощью Visual Molecular Dynamics [127].
Таблица 4
Структурные характеристики некоторых смоделированных запасных белков семян.
| Тип белка | Метод прогнозирования структуры | Экспериментальная форма | Характеристики структуры | Ссылки (примеры) | |
|---|---|---|---|---|---|
| Глобулин | Кристаллическая структура Canavalin 90119 | Кристаллическая дифракция19 с солевыми мостиками и гидрофобными кластерами | [93,94,95,96] | ||
| Вицилин | Гомологическое моделирование | Аминокислотная последовательность | Тример | [97] | |
| Круциферин Аминокислотная последовательность | Гексамер через межпротомерные (IE) дисульфидные связи между двумя тримерами | [98] | |||
| Проламин | Глиадины | Динамическое рассеяние света, криопропускающая электронная микроскопия, малоугловое рассеяние рентгеновских лучей , МД моделирования | Раствор глиадина при pH 3.0 | Димеры 5,72 нм, агрегированные кластеры 30 нм, олигомеры 68 и 103 нм | [103,105] |
| Глютелин | Глютенины | Малоугловое рассеяние рентгеновских лучей | Родное / извлеченное из пшеницы семя | Собственно неупорядоченная структура | [34,104] |
5.1. Альбумины
Кристаллические структуры некоторых запасных белков альбумина были идентифицированы с помощью ЯМР и рентгеновской кристаллографии [92], и две из этих белковых структур были депонированы в RCSB PDB [57].Имеется ограниченная информация о структурном моделировании с использованием инструментов моделирования для белков запаса зерна альбумина.
5.2. Глобулины
Практически все отложения в PDB RCSB на растительных глобулинах основаны на рентгеновской дифракции. Тот факт, что доступны модели на основе дифракции рентгеновских лучей, позволяет проводить верификацию структур белков на основе моделирования и упрощает дальнейшее компьютерное моделирование. Глобулины из семян бобовых были первым запасным белком, который был кристаллизован и оценен с помощью дифракции рентгеновских лучей [93,94,95,96].Кристаллическая структура оказалась компактной с солевыми мостиками и гидрофобными кластерами, в результате чего слои упакованных молекул образуют агрегаты [94]. С тех пор моделирование гомологии использовалось для моделирования других белков глобулинов, например, вицилина в какао, на основе кристаллических структур глобулинов бобовых культур, таких как канавалин из бобов джек и фазеолин из французских бобов [97] (). Эти исследования показывают, что гидрофобные аминокислоты скрываются внутри белковой молекулы при образовании тримеров, в то время как остатки гистидина находятся на границе раздела с другими глобулинами [97].В более поздних исследованиях использовалось моделирование гомологии Arabidopsis thaliana для определения структуры запасного белка масличных семян круциферина [98] (). Влияние структуры на функцию круциферина оценивалось с использованием различных изоформ белка [98]. Недавние исследования с использованием трехмерных молекулярных моделей и компьютерного моделирования продемонстрировали способность вицилин-подобных белков из бобовых растений связываться с хитином или хитиновыми структурами через три сайта связывания хитина на каждом тримере вицилина [106].Примеры структурных особенностей запасного белка 7S-глобулина в сое и 11S-глобулина в горохе, полученные путем моделирования на основе аминокислотных последовательностей [39,107,108] отдельных субъединиц и их полимеров, показаны на рис.
5.3. Проламины
Проламины и глютелины менее изучены путем моделирования и моделирования, чем глобулины и большинство других типов белков. Основная причина отсутствия моделей белков проламина заключается в том, что их структура внутренне неупорядочена [99].Исследования растворимости с использованием различных растворителей показали, что проламины являются мономерами в их естественной стадии [4,10] (). Однако было показано, что во время обработки проламины образуют дисульфидные связи с другими запасными белками семян, тем самым способствуя образованию полимеров [10,109]. Ранние исследования, оценивающие структурные особенности проламинов в пшенице (глиадины), с использованием инфракрасной спектроскопии с преобразованием Фурье (FT-IR), обнаружили равное количество α-спирали, линейной β-структуры, β-витков и неупорядоченной структуры [110] .Структуры глиадинов были оценены при pH 3,0 с помощью динамического рассеяния света, криопропускающей электронной микроскопии и малоуглового рассеяния рентгеновских лучей с последующим предсказанием ab initio и моделированием MD [105] (). Эти исследования указывают на присутствие димеров с гидродинамическим радиусом 5,72 нм, агрегированных кластеров 30 нм и олигомеров 68 и 103 нм [105]. Сообщалось также о важности концентрации глиадинов в дистиллированной воде для их агрегатного состояния [103].При 0,5 мас.% Глиадина может наблюдаться отталкивание глиадиновых ансамблей, в результате чего белок в основном присутствует в своей мономерной форме с ограниченными количествами димеров и олигомеров, а при 15 мас.% Глиадина — гелеобразной гидратированной формы. solid образуется в результате образования агрегатов [103]. Было также показано, что под действием тепла и давления глиадины образуют гексагональные структуры с параметром решетки 65 Å [27,33,38]. Ab initio моделирование было использовано для исследования причин образования гексагональных структур глиадинами и частично приписано глицерину, действующему как химический шаперон, помогающий в упаковке белковых молекул [38].Проламины кукурузы (зеины) были смоделированы с помощью МД-моделирования в большей степени, чем глиадины пшеницы. Структурной особенностью зеинов является α-спираль с четырьмя аминокислотными остатками на виток и гидрофобная поверхность внутри спирали, образованная неполярными остатками с каротиноидным лютеином, помогая стабилизировать структуру [111]. Во время испарения растворителя зеины способны самоорганизовываться в белки различной формы, включая стержни, сферы и пленки разных размеров, отчасти из-за так называемого связывания белков «голова к хвосту» [112].Ранние исследования пшеницы предполагали связывание глиадинов голова-хвост [113,114] при агрегации, что также было показано в подтвержденных исследованиях [103,105].
5.4. Глутелины
Глютелины представляют собой даже более крупные и сложные молекулы, чем проламины [104] (), а глютелины пшеницы (глютенины), как известно, образуют самые крупные полимеры в природе [115] (). Это одна из причин ограниченного моделирования этих белков. Подавляющее большинство предыдущих исследований было сосредоточено на изучении того, как образуются эти большие полимеры, и на основе их образования [10,31].Известно, что деполимеризация и повторная полимеризация глютенового полимера происходят во время технологических операций, таких как замес теста [116]. Таким образом, теоретические модели механизмов полимеризации были одним из способов использования инструментов моделирования для прогнозирования структуры полимера глютенина [117]. С помощью этих моделей можно оценить направленность образования полимеров (голова к хвосту, голова к голове, хвост к хвосту или хвост к голове). В недавнем исследовании с использованием ВЭЖХ и малоуглового рассеяния рентгеновских лучей было сообщено о сильно присущей и неупорядоченной структуре в нативном белке глютенина пшеницы, в то время как структуры неизвестного типа были сформированы во время обработки белков в пленки [34].Молекулярное моделирование, моделирование гомологии и моделирование MD также использовались на N -концевом домене глютенинов для изучения полимеризации белков в гигантские олигомеры посредством образования дисульфидных связей [118,119].
5.5. Будущие возможности моделирования белков-хранилищ семян злаков
Основные причины отсутствия исследований с использованием инструментов моделирования и моделирования MC / MD для исследования белков проламина и глутелина заключаются в том, что (i) белки являются крупными и являются одними из крупнейших белков в мире. природа [120]; (ii) белки в их нативной форме по своей природе неупорядочены и не растворимы в воде [99]; (iii) структуры белков изменяются при разбавлении [99] или обработке [31], т.е.например, на нижние уровни структур в разбавленном состоянии [103], иерархические структуры в концентрированных режимах [99] и гексагональные [27,31] и другие типы структур [34], развивающиеся при определенных условиях обработки; и iv) указанные структуры всегда связаны с агрегацией белков в полимеры [10]. Таким образом, моделирование этих белков чрезвычайно сложно и требует большой мощности компьютера. Однако запасные белки злаков очень полезны и важны: (i) в качестве запасного ресурса для регенерации растений [7]; и (ii) для пищевых продуктов и кормов для людей [7] и животных [121]; и потенциально полезны в (iii) непищевых применениях, таких как замена пластмасс на нефтяной основе [10,122].Была продемонстрирована четкая взаимосвязь структура-функция между образованием белковых структур во время обработки и функциональностью продуктов, полученных из запасных белков зерновых [123,124]. Следовательно, лучшее понимание структурных особенностей растительных запасных белков, особенно малоизученных проламинов и глютелинов, а также возможности точной настройки их структурных характеристик внесут значительный вклад в их полезность в различных приложениях. Более того, такое понимание помогает выявить физиологические и эволюционные причины различий в запасных белках среди растений.Новые инструменты моделирования, вместе с более быстрыми / мощными компьютерами и инструментами компьютерного кластера для расширения возможностей алгоритмов моделирования, имеют первостепенное значение в такой работе и откроют возможности для идентификации даже самых крупных и сложных белковых структур. Новые инструменты моделирования и недавно разработанные алгоритмы будут доступны для исследователей и других лиц в ближайшем будущем, вместе с более мощными компьютерами и компьютерными кластерами, которые проложат путь для моделирования даже самых крупных и изначально неупорядоченных белков, таких как глютелин, хранящий семена. белки.В будущем исследования глиадинов и глютенинов могут также выиграть от аналогичного подхода к подходам, используемым для эластомерных белков, с использованием моделей низкой сложности (не крупнозернистых) и / или работы с пептидными фрагментами для выявления поведения белков [125]. Такое моделирование откроет новые возможности для оценки биологических свойств растений и для точной настройки свойств продуктов питания и материалов, производимых из этих белков.
6. Выводы
Сочетание инноваций в компьютерных технологиях, повышенной скорости и мощности компьютеров, а также новых инструментов моделирования / симуляции расширит возможности, которые определяют структуры белков и выявляют взаимосвязи между структурой и функцией.До недавнего времени инструменты моделирования и симуляции редко использовались для оценки структур растительных белков и взаимосвязей между структурой и функцией. Таким образом, менее 9% текущих депозитов в Исследовательском сотрудничестве в банке данных по структурной биоинформатике связаны с растениями, а возраст одной трети этих депозитов составляет менее пяти лет. Для двух наиболее распространенных типов растительных белков, RuBisCO и запасных белков, моделирование использовалось в разной степени. Для RuBisCO и фотосинтетического аппарата моделирование использовалось довольно часто для описания процесса и структурных воздействий изменений в белке.Структурные особенности запасных белков были в меньшей степени описаны моделированием, особенно для проламина и глютелина. Текущее состояние моделирования в отношении структурных особенностей запасных белков проиллюстрировано на примерах белков глобулина (соя, горох), проламина (α-глиадин пшеницы) и глютелина (глютенин пшеницы), соответственно.
Вклад авторов
Идея проекта и этой статьи E.J. и M.H .; концептуализация данной статьи была выполнена совместно Ф.R., J.M. and E.J .; планирование и определение подразделов было выполнено совместно F.R., J.M. и E.J .; подготовка таблиц производилась Ф.Р .; подготовка и моделирование были выполнены J.M .; написание отдельных подразделов, F.R, J.M. и E.J. письмо — подготовка оригинального проекта, E.J .; написание — просмотр и редактирование, M.H .; визуализация, E.J .; надзор, E.J., M.H., F.R .; администрация проекта, E.J .; привлечение финансирования, E.J., M.H. Все авторы прочитали и согласились с опубликованной версией рукописи.
Моделирование для понимания взаимосвязей между структурой и функцией растительного белка — значение для белков-хранилищ семян
Abstract
Белки являются одними из самых важных молекул на Земле. Их структура и агрегационное поведение являются ключом к их функциональности в живых организмах и в продуктах, богатых белком. Инновации, такие как увеличенный размер и мощность компьютера, вместе с новыми инструментами моделирования, улучшили наше понимание взаимосвязей между структурой белка и функцией.В этом обзоре рассматриваются различные белки, присутствующие в растениях, и инструменты моделирования, которые можно применять для лучшего понимания белковых структур и их взаимосвязи с функциональностью, с особым акцентом на запасных белках растений. Моделирование растительных белков расширяется, но менее 9% депозитов в Исследовательском коллаборации структурной биоинформатики белковых данных поступают из растительных белков. Хотя применяются те же инструменты, что и для других белков, моделирование растительных белков отстает, а инновационные методы используются редко.Молекулярная динамика и молекулярный докинг обычно используются для оценки различий в формах или мутантах и их влияния на функциональность. Инструменты моделирования также использовались для описания фотосинтетического механизма и его реакций переноса электронов. Запасные белки, особенно в больших и изначально неупорядоченных проламинах и глютелинах, были значительно менее хорошо описаны с помощью моделирования. Эти белки агрегируются во время обработки и образуют большие полимеры, которые соотносятся с функциональностью.Полученные в результате взаимосвязи структура-функция важны для обработанных запасных белков, поэтому моделирование и имитационные исследования с использованием современных моделей, алгоритмов и компьютерных инструментов необходимы для лучшего понимания этих взаимосвязей.
Ключевые слова: альбумин, глобулин, глютелин, моделирование Монте-Карло, моделирование молекулярной динамики, проламин
1. Введение — Растительные белки: типы, характеристики и наличие
1.1. Разнообразие растительных белков и их функции
Белки — это биологические макромолекулы, которые отвечают за большинство биологических ролей (иногда вместе с другими биомолекулами) в клетке.Таким образом, белки можно рассматривать как биомолекулярные устройства с естественными структурными и функциональными свойствами, которые часто сложно воссоздать в лаборатории. Некоторыми классическими примерами белков с исключительными функциями являются белки шелка паука, сочетающие в себе очень высокую прочность с превосходной эластичностью [1], и бактериальные жгутики, которые представляют собой микроскопические пропеллеры [2]. Белки в форме ферментов катализируют реакции с большой скоростью и высокой селективностью.
Подобно белкам в целом, растительные белки играют различные ферментативные, структурные и функциональные роли (фотосинтез, биосинтез, транспорт, иммунитет и т. Д.).Они также действуют как среда для хранения, чтобы удовлетворить потребности развивающихся сеянцев в росте и питании. Белки выполняют эти функции в своем составе и определенных структурных формах, например, посредством складывания, которое может варьироваться от компактного и хорошо упорядоченного до развернутого и внутренне неупорядоченного.
1.2. Классификация растительных белков — взаимосвязь с запасными белками семян
Первые попытки классифицировать растительные белки были основаны на экстрагируемости и растворимости этих белков, при этом первое систематическое исследование, проведенное T.Б. Осборн, применив классификационную схему, предложенную Американским комитетом по номенклатуре белков [3]. Эта номенклатура в основном классифицирует белки на три типа; простые, сопряженные и производные. Белки во всех тканях растений классифицируются как простые белки, которые делятся на четыре типа [4] (). Эти четыре типа растительных белков в основном связаны с запасными белками семян и известны как альбумины, глобулины, проламины и глютелины, разделенные на основе фракционирования Осборна водой, солью, спиртом и щелочью соответственно ().Позднее были предприняты попытки более сложных классификаций растительных белков, основанных, например, на их химической структуре, механизме / механизмах действия, биологической функции или местонахождении внутри растения. Несмотря на эти попытки использовать более современные системы классификации, классификация Осборна по-прежнему остается наиболее широко используемой системой, особенно используемой для процедур экстракции и очистки белков [5]. Однако на практике классификация Осборна использовалась только для запасных белков семян, тогда как классификация других растительных белков обычно более сложна и иногда неясна.
Таблица 1
Типы, характеристики (на основе фракционирования по Осборну [3,4]) и наличие растительных белков.
| Тип протеина | Растворимость | Характеристики | Примеры в растениях | Ссылки (примеры) |
|---|---|---|---|---|
| Альбумины | Вода | Шаровидный тип 2, коагулянт | например, Лейцин, Легумалин, Фазелин, Рицин | [4,5,6] |
| Глобулины | Солевой раствор | Шаровидный, с более высокой молекулярной массой, чем альбумины | 7S вицилинового типа (горох, соя и т. д.)) 11S бобового типа (капуста, овес, рис) | [4,7] |
| Проламины | Смеси спирт / вода (например, 70% этанол) | Внутримолекулярные дисульфидные связи, высокая доля пролина и глутамин, повторяющиеся мотивы в центральных доменах | Глиадины, зеин, гордеин, секалин | [4,7,8,9,10] |
| Глютелины | Щелочные растворы | Межмолекулярные дисульфидные связи, высокая доля пролин и глутамин, повторяющиеся мотивы в центральных доменах | Глютенины в пшенице | [4,7,8,9,10,11] |
1.3. Характеристика и наличие белков, классифицированных по осборну.
Альбумины определяются как водорастворимые глобулярные белки, коагулирующие при нагревании (). Наиболее известные альбумины — это сывороточный альбумин, основной белок в крови человека, и яичный белок. В растениях альбумин присутствует в семенах в виде запасного белка 2S-альбумина, например, в виде лейцина в ячмене, пшенице и ржи, в виде бобумелина в горохе, сое и вигне, в виде фазелина в фасоли и в виде рицина в клещевине [6 ] (). Многие белки в тканях зеленых растений, в том числе рибулозо-1,5-бисфосфаткарбоксилаза оксигеназа (RuBisCO), фермент, катализирующий первую стадию фиксации углерода и самый распространенный белок на Земле, не определяются как альбумины, несмотря на то, что они водорастворимы. .RuBisCO растворим в воде и коагулирует под действием тепла [12], что, по определению Осборна, должно сделать его белком альбумина. Точно так же большинство ферментативных белков в растениях растворимы в воде и коагулируются под действием тепла, но, кроме того, что они были охарактеризованы как ферменты, они не были далее определены в тип белка.
Глобулины также являются глобулярными белками, которые имеют более высокий молекулярный вес, чем альбумины, и растворимы в разбавленном солевом растворе, но не растворимы в воде (). Самый известный глобулин — это главный белок крови человека (сывороточный гамма-глобулин) [13].У растений глобулины присутствуют в качестве запасных белков как у двудольных, так и у однодольных, что делает их наиболее распространенной группой запасных белков [7]. Основываясь на коэффициенте седиментации, глобулины-накопители растений в основном делятся на две группы: 7S-вицилиновый тип, который был обнаружен и широко изучен в горохе, сое и т. Д., И 11S-бобовый тип, который, например, является основным хранилищем. белок в большинстве бобовых и двудольных растений, таких как капуста, овес и рис [7] (). Некоторые белки листьев растений явно не растворимы в воде и могут быть классифицированы как глобулины в некоторых характеристиках белков листьев [14].Однако причина того, что эти белки листа не растворимы в воде, может заключаться в том, что они связаны с клеточной стенкой, взаимодействуют с пектином или являются гидрофобными [15], и поэтому их, очевидно, нелегко отнести к категории глобулинов или альбуминов.
Два дополнительных типа протеина, проламины и глютелины, обнаруживаются, в частности, в качестве запасных протеинов в семенах семейства злаковых (Triticeae), где они являются доминирующими протеинами, составляющими до 85% от общего протеина [7] (). Проламины, содержащиеся в пшенице, называются глиадинами, тогда как номенклатура проламинов в других злаках основана на их латинских названиях; зеин в кукурузе, гордеин в ячмене, секалин в ржи и т. д.[8] (). Чаще всего глютелин содержится в пшенице (глютенин), хотя глютелин также присутствует в ячмене и ржи [11] (). Проламины и глютелины имеют несколько общих черт, включая высокую долю пролина и глутамина и высокую долю повторяющихся мотивов или последовательностей с неповторяющимися доменами на их N- и C-концах [8]. Хотя эти белки различаются по молярной массе, основное различие между двумя типами белков заключается в образовании внутри- и межмолекулярных дисульфидных связей в нативном состоянии проламинов и глутелинов соответственно [9], что объясняет различия в их экстрагируемости. .
1,4. Запасные белки семян — типы и характеристики
Из предыдущих разделов ясно, что запасные белки семян присутствуют в семенах в различных типах, включая альбумин, глобулин, проламин и глютелин [6,7,8]. Эти белки могут иметь разные характеристики в растительной клетке, а также во время обработки и для различных применений, где запасные белки вносят вклад в функциональность. Однако на сегодняшний день запасные белки семян в основном охарактеризованы на основе их химических свойств во время фракционирования, осаждения и т. Д.[4,6,7,8]
2. Функциональные возможности растительных белков — в растениях, а также в пищевых продуктах и промышленности
2.1. Функция растительных белков в растении
Растительные белки удовлетворяют потребности проростков в питании и росте благодаря своим ферментативным, структурным, функциональным и запасающим функциям [16]. Растения содержат ряд определенных типов белков, которых нет в других живых организмах, и они выполняют определенные функции (). Например, у большинства растений есть какой-либо запасной орган (семена, клубни и т. Д.).) для размножения, где хранятся различные источники питательных веществ, чтобы у нового растения были ресурсы для роста в предстоящий сезон. Белки, углеводы и масла — это различные типы источников питательных веществ, которые накапливаются в органах хранения растений. Такие белки обычно называют запасными белками (). Их основная функция — расщепляться на аминокислоты, чтобы сформировать необходимые строительные блоки для появляющихся белков в растении следующего поколения [17]. Клетка растения содержит ряд органелл, в том числе хлоропласт, ответственных за фотосинтез ().У растений также есть специфический белок, фермент RuBisCO (), который катализирует передачу солнечной энергии в химическую энергию, которая может быть использована растением, посредством фиксации CO 2 [18].
Таблица 2
Примеры растительных белков с их уникальными функциями в растениях, пищевых и непищевых продуктах
| Использование | Тип белка (Примеры) | Возникновение (Примеры) | Функция (Примеры) | Ссылки (Примеры) |
|---|---|---|---|---|
| Живые растения | Запасные белки | Семена, клубни | Рост и питание рассады и проростков | [16,17] |
| Фотосинтез | ||||
| Белки плазматической мембраны e.g., поверхностные белки, глобулярные белки | Клеточная мембрана, Белковые каналы | Транспорт, структурная поддержка, ионная регуляция | [16,18] | |
| Пищевые продукты | Вицилин | Горох | Эмульгирование гелеобразования при нагревании свойства | [19,20,21,22] |
| Биологические материалы | Глютенины | Пшеница | Когезивная матрица, газовый барьер, прочность | [10,23,24,25,26,27, 28,29,30,31,32,33,34] |
| Глиадины | Пшеница | Связная матрица, газовый барьер, гибкость |
2.2. Функции растительных белков в пищевых продуктах
В пищевых продуктах белки часто являются основным функциональным компонентом, особенно в обработанных пищевых продуктах с высоким содержанием белка [19]. В таких продуктах белки вносят свой вклад в питание, а также в качество, текстуру, аромат, вкус, чувство сытости и простоту обработки [20] (). Большинство растительных белков обладают характеристиками, которые делают их интересными при переработке пищевых продуктов, хотя их конкретные характеристики могут отличаться. Например, было показано, что вицилин горохового белка обладает лучшими свойствами гелеобразования и эмульгирования, вызванными нагреванием, чем бобовые гороха, которые, как было обнаружено, более питательны для человека [21].Эффективность различных растительных белков для пищевых продуктов сильно зависит от их структурных особенностей и их способности образовывать определенные трехмерные (3D) конфигурации / конформации, а также их способности к сшиванию [10,22].
2.3. Функции растительных белков в промышленных приложениях
Растительные белки также обладают свойствами, которые делают их интересными для использования в качестве материалов (). Ряд растительных белков, включая в основном запасные белки, например, из пшеницы, сои, картофеля и масличных культур, обладают интересными свойствами для таких применений, как упаковка, огнестойкие и абсорбирующие материалы [23,24,25,26,27,28,29 , 30] ().Способность белков к сшиванию и агрегации важна для хороших свойств материала на основе белка [10,31,32,33].
2.4. Влияние запасных белков семян на функциональность
Приведенные выше описания ясно показывают первостепенное значение запасных белков в растениях как источника аминокислот, которые будут использоваться в качестве строительных блоков для развивающихся молодых проростков при появлении всходов [17]. В пищевых продуктах и в промышленности запасные белки семян играют центральную роль в обеспечении функциональности [19,20,21,22,23,24,25,26,27,28,29,30], поэтому важно понимать, как функционирует подвержены влиянию и могут быть настроены [35,36,37].
3. Моделирование — современное состояние растительных белков
3.1. Основа для моделирования структур белков
Как описано выше, трехмерная (3D) -конформация нативных белков вместе с их способностью сшивать, изменять форму и формировать определенные структурные особенности вносят существенный вклад в функциональные свойства конкретных белков. в растении и в растительных продуктах [31,34,38]. По сути, методы определения структуры белков можно разделить на три типа:е., основанные на различных типах методов микроскопии, основанные на рассеянии / дифракции и спектроскопии (например, методы рентгеновского и ядерного магнитного резонанса (ЯМР)), и основанные на моделировании [39] (). В этом обзоре мы сосредоточимся на возможностях и недостатках использования моделирования для определения структур растительных белков, уделяя особое внимание запасным белкам растений.
Таблица 3
Методы, используемые для определения структур белков и взаимосвязей между структурой и функцией.
| Тип метода | Метод (Примеры) | Используется для / приложений (Примеры) | Ссылки (Примеры) |
|---|---|---|---|
| Микроскопия | Трансмиссионная электронная микроскопия (TEM119) | (3D) структура белков из 2D изображений частиц | [39,48] |
| Крио-электронная микроскопия (Cryo-EM) | 3D-структура биомакромолекул в нативном состоянии | [39,49] | |
| Томография | 3D-изображения высокого разрешения | [50] | |
| Визуализация | Изображения отдельных белков с помощью низкоэлектронной голографии | [50,51] | |
| Рассеяние / дифракция, ядерная магнитная спектроскопия | резонансная спектроскопия (ЯМР)Химические сдвиги, отражающие конформации белков | [52] | |
| Малоугловые рентгеновские лучи рассеяние | Форма, конформация и сборка белков | [53] | |
| Широкоугольное рентгеновское рассеяние | Характеристика структурных моделей, сходства и изменений в атомной упаковке | [54] | |
| Фурье Инфракрасная спектроскопия с преобразованием (FT-IR) | Конформация белка путем подбора пика амидных полос | [39,55] | |
| Рентгеновская кристаллография | Атомное разрешение трехмерных структур белка | [56] | |
| Моделирование-имитация | На основе шаблона | Моделирование на основе гомологии | [34] |
| Ab initio | Моделирование основано только на информации о последовательности | [40,41] | |
| Монте-Карло (MC) | Статистический метод оценки движений белка | [42,43] | |
| Молекулярная динамика (MD) | Решение уравнения Ньютона уравнение движения | [43] | |
| Машинное обучение (AlphaFold) | Искусственная нейронная сеть | [45,46,47] |
3.2. Моделирование на основе шаблонов и Ab Initio
Методы, применяемые для моделирования структур растительных белков, аналогичны тем, которые используются для любого типа белка (). Моделирование на основе шаблонов — это наиболее упрощенный метод моделирования белков. Модели на основе шаблонов построены на сравнении аминокислотных последовательностей белков с известными белковыми структурами (часто идентифицируемыми с помощью кристаллографии) и предположении, что аналогичные последовательности приводят к одинаковым структурам белков [40]. Однако многие белки не имеют сходства последовательностей с другими белками, уже присутствующими в базах данных, и с известными структурами.Для таких белков (не показывающих взаимосвязи с известными белками) моделирование только на основе информации о последовательности, то есть предсказание структуры белка ab initio, является единственным вариантом. В предсказаниях ab initio термодинамические принципы применяются к случаю конформации белка посредством поиска общего минимума энергии [40].
3.3. Монте-Карло, молекулярная динамика и методы машинного обучения
Два более продвинутых / современных метода, Монте-Карло (MC) и молекулярная динамика (MD), были разработаны в последние годы для предсказания и моделирования структуры белков.Оба метода напоминают подход ab initio, поскольку моделирование основано только на информации о последовательности. (). Оба метода можно применять в разных масштабах с разной степенью детализации; от полностью атома и объединенного атома к крупнозернистым моделям [41]. Преимущество вычислений MC состоит в том, что их выполнять быстрее и проще, чем вычисления MD, из-за того, что они свободны от ограничений, связанных с решением уравнения движения Ньютона [42] (). Однако это также влияет на результаты, поскольку из прогона MC не собирается «динамическая» информация [42,43].Таким образом, в нескольких моделированиях белков MC была объединена с MD [44]. Более того, современные методы машинного обучения, такие как алгоритм AlphaFold, позволили значительно продвинуться в предсказании структуры белка на основе информации о последовательностях [45]. В последних экспериментах по критической оценке предсказания структуры белка (CASP) 3D-модели белков AlphaFold были помещены на первое место в категории «Бесплатное моделирование» с точки зрения точности [46]. Алгоритм AlphaFold использует искусственные нейронные сети для создания библиотеки специфичных для белков фрагментов [47].Однако алгоритмы, такие как AlphaFold, еще не применялись для прогнозирования структуры запасных белков семян, вероятно, потому, что эти алгоритмы обычно предсказывают белковые структуры на основе сворачивания, в то время как некоторые из наиболее полезных запасных белков изначально неупорядочены.
3.4. Моделирование растительных белков с особым акцентом на запасных белках семян
Область исследований по моделированию растительных белков сравнительно небольшая и относительно новая, с ограниченным количеством связанных с растениями депозитов в Исследовательском сотрудничестве по структурной биоинформатике банка данных белков (RCSB PDB).Поиск месторождений растений в настоящее время дает 2300 результатов, четверть из которых — от Arabidopsis. Сортировка, основанная на наиболее распространенных организмах, показывает 1382 попадания на Arabidopsis и 15000 попаданий на другие (другие = организмы растительного происхождения, но также и дополнительные организмы) в общей сложности более 160 000 общих отложений (большинство поступает от людей и микроорганизмов) [57]. Одна треть залежей в текущем поиске растений относится к 2015 году и позже. Для запасных белков семян доступно только 47 отложений, большинство из которых составляют глобулины, а остальные — альбумины.Эти отложения указывают на то, что моделирование растительных белков было сосредоточено на определенных областях. Это также отражено в информации в PDB RCSB, где доступно большое количество отложений, например, в белках, связанных с механизмом фотосинтеза, белках, связанных с рибосомами, ферментами, стрессом и защитой, а также для аллергенов и сладких на вкус. белки [57]. Моделирование растительных белков в этих различных областях кратко изложено в Разделе 4.1, Разделе 4.2, Разделе 4.3, Разделе 4.4, Разделе 4.5 и раздел 4.6, чтобы определить возможности, актуальные для моделирования запасных белков семян.
4. Основные области моделирования растительных белков и влияние на моделирование запасных белков семян
Подходы к моделированию шести наиболее распространенных растительных белков в RCSB PDF описаны ниже. Запасные белки семян не входят в их число, хотя знания, полученные из других областей исследований, могут иметь отношение к моделированию запасных белков семян.
4.1. Фотосинтетическое оборудование
Фотосинтетическое оборудование отвечает за передачу солнечной энергии в химическую энергию посредством фиксации CO 2 [18].Таким образом, это одна из наиболее важных и специфических черт растений, которая давно привлекает интерес научного сообщества. Моделирование методом МД, дополненное квантово-механическими описаниями, применялось уже в начале 1990-х годов для описания того, как перенос электронов контролируется движением белка в фотосинтетических реакционных центрах [58]. С тех пор моделирование молекулярной динамики способствовало пониманию того, что движение белка в реакционных центрах является ключом к кинетике первичной реакции переноса электрона [59].Чтобы понять все механизмы фотосинтетического аппарата, был принят ряд как аналитических, так и имитационных методов, как недавно сделал обзор Блумберже [60,61]. Инструменты для оценки перемещений белков в реакционных центрах могут быть полезны для исследования перемещений запасных белков семян во время обработки и передачи динамики / энергии для этих перемещений. Структура RuBisCO, а также дивергентных, мутантных и гибридных форм этого фермента охарактеризована с помощью рентгеновской кристаллографии [62].Моделирование молекулярной динамики также использовалось для объяснения вариаций в функциональности мутантов RuBisCO, где было обнаружено использование структурных контрольных точек, позволяющих точно настроить динамику фермента [63]. Точно так же динамику запасных белков семян, уже охарактеризованную экспериментальными методами, такими как рентгеновская кристаллография, можно понять с помощью методов компьютерного моделирования.
4.2. Белки, ассоциированные с рибосомами
Крио-ЭМ-исследования в сочетании с рентгеновской кристаллографией были применены для определения структуры рибосом, создания статических моделей для различных состояний рибосом.Недавно компьютерные исследования, включающие моделирование, оказались успешными в проливании света на структурные флуктуации и переходы между различными рибосомными конфигурациями [64]. Успехи в моделировании МД, включая крупномасштабное МД, являются одним из объяснений успешного моделирования больших макромолекулярных комплексов, таких как рибосомы [65]. Размер некоторых запасных белков семян создает проблемы при их моделировании, что приводит к сходству с моделированием рибосом. Таким образом, использование крупномасштабных МД может быть альтернативой для моделирования запасных белков семян.
4.3. Ферменты
Подходы к математическому моделированию долгое время были полезным инструментом для исследования сложности метаболических сетей и их ферментативной регуляции, в то время как более современные модели внесли большой вклад в растущую область системной биологии [66]. Чаще всего для изучения регуляции ферментов применялись ферментно-кинетические модели [66], хотя в последнее время для аналогичных целей использовались методы MD и моделирование молекулярной стыковки [67]. Ферментно-кинетическое моделирование метаболических путей существенно отличается от моделирования структур и функций запасных белков семян.
4.4. Стресс и защита
Что касается белков стресса и защитных механизмов, моделирование было использовано для лучшего понимания задействованных механизмов [68,69,70,71]. Опять же, недавнее использование МД-моделирования улучшило наше понимание этих белков. Как моделирование гомологии, так и моделирование методом МД использовались для изучения фона устойчивости растений к гербицидам [72]. Гомологическое моделирование, молекулярная стыковка и моделирование МД использовались для оценки различий в конформациях белков, вносящих вклад в устойчивость, по сравнению с реакциями восприимчивости растений к различным заболеваниям [73].Наибольшее значение для моделирования запасных белков семян имеет методология, описывающая различия в конформации белков, связанные с различными функциями и функциональными возможностями.
4.5. Аллергены
Аллергенами часто являются белки [74], а растения содержат множество аллергенов, на которые чувствительные люди проявляют аллергические реакции [75]. Белки растений, ответственные за аллергические реакции, были структурно смоделированы с использованием кристаллографии, рассеяния рентгеновских лучей и ЯМР, а также стыковочного моделирования моделей белков с аналогичной последовательностью [76,77].Кроме того, была определена трехмерная кристаллическая структура различных белков аллергии растительного происхождения, а моделирование МД было использовано для обнаружения молекулярных конформаций белков, участвующих в аллергических реакциях [78,79,80]. Некоторые аллергены растительного происхождения также являются запасными белками семян в растениях, поэтому моделирование, проведенное на аллергенах, можно напрямую перенести на исследования запасных белков семян и взаимосвязей между структурой и функцией.
4.6. Белки сладкого вкуса
Белки сладкого вкуса — это специфические растительные белки, представляющие большой интерес, поскольку они обладают характеристиками, делающими их в сотни или тысячи раз слаще по вкусу, чем сахар [81,82].Несколько исследований были сосредоточены на изучении этого свойства с использованием таких методов, как кристаллизация белков и определение их структуры с помощью ЯМР и рентгеновской кристаллографии [81,83]. Сравнительное / гомологическое моделирование и методы молекулярного стыковки использовались для предсказания трехмерных структур димерных и тетрамерных форм некоторых сладких белков, в то время как влияние pH на конформацию белков оценивалось с использованием МД-моделирования [82]. МД-моделирование также использовалось в качестве инструмента структурно-ориентированной белковой инженерии для разработки улучшенных низкокалорийных подсластителей на растительной основе для фармацевтического и пищевого применения [84].Методы, применяемые для понимания структурно-функционального поведения, и методы, используемые для структурно-ориентированной инженерии, могут представлять интерес для исследований и приложений семян запасных белков.
5. Понимание взаимосвязи между структурой и функцией запасных белков семян
Запасные белки растений, вероятно, являются второй по распространенности группой белков в растениях (после RuBisCO). У всех растений, содержащих запасные органы, такие как зерна и семена, функция запасных белков заключается в хранении аминокислот, необходимых для роста и развития проростков [85].С этими белками было проведено немного исследований с помощью инструментов моделирования, несмотря на обилие запасных белков растений, их важность как источника питания для формирующегося молодого ростка [85] и их влияние на функциональность продуктов из растительных зерен [10, 22,23,86,87,88,89]. Однако методы биоинформатики все чаще используются для классификации различных белков растений, при этом нейронные сети демонстрируют точность 95,3% при классификации белков риса по различным классам (альбумины, глобулины, проламины, глютелины) [90].Кроме того, алгоритмы машинного обучения успешно использовались для классификации запасных белков семян риса, пшеницы, кукурузы, клещевины и кресс-салата на их классы [91]. Структурно различные классы запасных белков семян можно разделить на два типа: альбумины / глобулины и проламины / глютелины (). Альбумины и глобулины, как правило, сильно структурированы и поэтому способны кристаллизоваться, и их сворачивание можно моделировать с помощью ряда методов, включая машинное обучение и моделирование ab initio [92,93,94,95,96,97,98] ().Большинство проламинов и глютелинов вместо этого по своей природе неупорядочены [99] и, таким образом, создают больше проблем при моделировании. Им потребуются алгоритмы на основе MC и MD для моделирования их структур, хотя методы малоуглового рассеяния в сочетании с инфракрасной спектроскопией (ИК) и высокоэффективной жидкостной хроматографией (ВЭЖХ) также применялись для изучения структурных изменений во время обработки [100,101,102,103,104] .
Отдельные субъединицы и полимеры, полученные из них (слева направо): запасные белки 7S-глобулин в сое, 11S-глобулин в горохе, α-глиадин в пшенице и субъединицы низкомолекулярного глютенина (LMW-GS) в пшенице.Аминокислотные последовательности и инструменты моделирования, применяемые для определения структур, описаны в Yoshizawa et al. [107] и Исследовательское объединение банка данных по структурной биоинформатике (RCSB PDB) (3AUP) [39] для 7S глобулина, а также в Tandang-Silvas et al. [108] и RSCB PDB (3KSC) [39] для 11S глобулина. Последовательности аминокислот для a-глиадина и LMW-GS можно найти по номерам доступа Uniprot {«type»: «entrez-protein», «attrs»: {«text»: «Q9ZP09», «term_id»: «75267695», «term_text»: «Q9ZP09»}} Q9ZP09 и {«type»: «entrez-protein», «attrs»: {«text»: «P10386», «term_id»: «121457», «term_text»: «P10386» }} P10386 и моделирование проводилось с использованием полностью атомной модели с алгоритмами Монте-Карло в программе Profasi [126].Все модели были визуализированы с помощью Visual Molecular Dynamics [127].
Таблица 4
Структурные характеристики некоторых смоделированных запасных белков семян.
| Тип белка | Метод прогнозирования структуры | Экспериментальная форма | Характеристики структуры | Ссылки (примеры) | |
|---|---|---|---|---|---|
| Глобулин | Кристаллическая структура Canavalin 90119 | Кристаллическая дифракция19 с солевыми мостиками и гидрофобными кластерами | [93,94,95,96] | ||
| Вицилин | Гомологическое моделирование | Аминокислотная последовательность | Тример | [97] | |
| Круциферин Аминокислотная последовательность | Гексамер через межпротомерные (IE) дисульфидные связи между двумя тримерами | [98] | |||
| Проламин | Глиадины | Динамическое рассеяние света, криопропускающая электронная микроскопия, малоугловое рассеяние рентгеновских лучей , МД моделирования | Раствор глиадина при pH 3.0 | Димеры 5,72 нм, агрегированные кластеры 30 нм, олигомеры 68 и 103 нм | [103,105] |
| Глютелин | Глютенины | Малоугловое рассеяние рентгеновских лучей | Родное / извлеченное из пшеницы семя | Собственно неупорядоченная структура | [34,104] |
5.1. Альбумины
Кристаллические структуры некоторых запасных белков альбумина были идентифицированы с помощью ЯМР и рентгеновской кристаллографии [92], и две из этих белковых структур были депонированы в RCSB PDB [57].Имеется ограниченная информация о структурном моделировании с использованием инструментов моделирования для белков запаса зерна альбумина.
5.2. Глобулины
Практически все отложения в PDB RCSB на растительных глобулинах основаны на рентгеновской дифракции. Тот факт, что доступны модели на основе дифракции рентгеновских лучей, позволяет проводить верификацию структур белков на основе моделирования и упрощает дальнейшее компьютерное моделирование. Глобулины из семян бобовых были первым запасным белком, который был кристаллизован и оценен с помощью дифракции рентгеновских лучей [93,94,95,96].Кристаллическая структура оказалась компактной с солевыми мостиками и гидрофобными кластерами, в результате чего слои упакованных молекул образуют агрегаты [94]. С тех пор моделирование гомологии использовалось для моделирования других белков глобулинов, например, вицилина в какао, на основе кристаллических структур глобулинов бобовых культур, таких как канавалин из бобов джек и фазеолин из французских бобов [97] (). Эти исследования показывают, что гидрофобные аминокислоты скрываются внутри белковой молекулы при образовании тримеров, в то время как остатки гистидина находятся на границе раздела с другими глобулинами [97].В более поздних исследованиях использовалось моделирование гомологии Arabidopsis thaliana для определения структуры запасного белка масличных семян круциферина [98] (). Влияние структуры на функцию круциферина оценивалось с использованием различных изоформ белка [98]. Недавние исследования с использованием трехмерных молекулярных моделей и компьютерного моделирования продемонстрировали способность вицилин-подобных белков из бобовых растений связываться с хитином или хитиновыми структурами через три сайта связывания хитина на каждом тримере вицилина [106].Примеры структурных особенностей запасного белка 7S-глобулина в сое и 11S-глобулина в горохе, полученные путем моделирования на основе аминокислотных последовательностей [39,107,108] отдельных субъединиц и их полимеров, показаны на рис.
5.3. Проламины
Проламины и глютелины менее изучены путем моделирования и моделирования, чем глобулины и большинство других типов белков. Основная причина отсутствия моделей белков проламина заключается в том, что их структура внутренне неупорядочена [99].Исследования растворимости с использованием различных растворителей показали, что проламины являются мономерами в их естественной стадии [4,10] (). Однако было показано, что во время обработки проламины образуют дисульфидные связи с другими запасными белками семян, тем самым способствуя образованию полимеров [10,109]. Ранние исследования, оценивающие структурные особенности проламинов в пшенице (глиадины), с использованием инфракрасной спектроскопии с преобразованием Фурье (FT-IR), обнаружили равное количество α-спирали, линейной β-структуры, β-витков и неупорядоченной структуры [110] .Структуры глиадинов были оценены при pH 3,0 с помощью динамического рассеяния света, криопропускающей электронной микроскопии и малоуглового рассеяния рентгеновских лучей с последующим предсказанием ab initio и моделированием MD [105] (). Эти исследования указывают на присутствие димеров с гидродинамическим радиусом 5,72 нм, агрегированных кластеров 30 нм и олигомеров 68 и 103 нм [105]. Сообщалось также о важности концентрации глиадинов в дистиллированной воде для их агрегатного состояния [103].При 0,5 мас.% Глиадина может наблюдаться отталкивание глиадиновых ансамблей, в результате чего белок в основном присутствует в своей мономерной форме с ограниченными количествами димеров и олигомеров, а при 15 мас.% Глиадина — гелеобразной гидратированной формы. solid образуется в результате образования агрегатов [103]. Было также показано, что под действием тепла и давления глиадины образуют гексагональные структуры с параметром решетки 65 Å [27,33,38]. Ab initio моделирование было использовано для исследования причин образования гексагональных структур глиадинами и частично приписано глицерину, действующему как химический шаперон, помогающий в упаковке белковых молекул [38].Проламины кукурузы (зеины) были смоделированы с помощью МД-моделирования в большей степени, чем глиадины пшеницы. Структурной особенностью зеинов является α-спираль с четырьмя аминокислотными остатками на виток и гидрофобная поверхность внутри спирали, образованная неполярными остатками с каротиноидным лютеином, помогая стабилизировать структуру [111]. Во время испарения растворителя зеины способны самоорганизовываться в белки различной формы, включая стержни, сферы и пленки разных размеров, отчасти из-за так называемого связывания белков «голова к хвосту» [112].Ранние исследования пшеницы предполагали связывание глиадинов голова-хвост [113,114] при агрегации, что также было показано в подтвержденных исследованиях [103,105].
5.4. Глутелины
Глютелины представляют собой даже более крупные и сложные молекулы, чем проламины [104] (), а глютелины пшеницы (глютенины), как известно, образуют самые крупные полимеры в природе [115] (). Это одна из причин ограниченного моделирования этих белков. Подавляющее большинство предыдущих исследований было сосредоточено на изучении того, как образуются эти большие полимеры, и на основе их образования [10,31].Известно, что деполимеризация и повторная полимеризация глютенового полимера происходят во время технологических операций, таких как замес теста [116]. Таким образом, теоретические модели механизмов полимеризации были одним из способов использования инструментов моделирования для прогнозирования структуры полимера глютенина [117]. С помощью этих моделей можно оценить направленность образования полимеров (голова к хвосту, голова к голове, хвост к хвосту или хвост к голове). В недавнем исследовании с использованием ВЭЖХ и малоуглового рассеяния рентгеновских лучей было сообщено о сильно присущей и неупорядоченной структуре в нативном белке глютенина пшеницы, в то время как структуры неизвестного типа были сформированы во время обработки белков в пленки [34].Молекулярное моделирование, моделирование гомологии и моделирование MD также использовались на N -концевом домене глютенинов для изучения полимеризации белков в гигантские олигомеры посредством образования дисульфидных связей [118,119].
5.5. Будущие возможности моделирования белков-хранилищ семян злаков
Основные причины отсутствия исследований с использованием инструментов моделирования и моделирования MC / MD для исследования белков проламина и глутелина заключаются в том, что (i) белки являются крупными и являются одними из крупнейших белков в мире. природа [120]; (ii) белки в их нативной форме по своей природе неупорядочены и не растворимы в воде [99]; (iii) структуры белков изменяются при разбавлении [99] или обработке [31], т.е.например, на нижние уровни структур в разбавленном состоянии [103], иерархические структуры в концентрированных режимах [99] и гексагональные [27,31] и другие типы структур [34], развивающиеся при определенных условиях обработки; и iv) указанные структуры всегда связаны с агрегацией белков в полимеры [10]. Таким образом, моделирование этих белков чрезвычайно сложно и требует большой мощности компьютера. Однако запасные белки злаков очень полезны и важны: (i) в качестве запасного ресурса для регенерации растений [7]; и (ii) для пищевых продуктов и кормов для людей [7] и животных [121]; и потенциально полезны в (iii) непищевых применениях, таких как замена пластмасс на нефтяной основе [10,122].Была продемонстрирована четкая взаимосвязь структура-функция между образованием белковых структур во время обработки и функциональностью продуктов, полученных из запасных белков зерновых [123,124]. Следовательно, лучшее понимание структурных особенностей растительных запасных белков, особенно малоизученных проламинов и глютелинов, а также возможности точной настройки их структурных характеристик внесут значительный вклад в их полезность в различных приложениях. Более того, такое понимание помогает выявить физиологические и эволюционные причины различий в запасных белках среди растений.Новые инструменты моделирования, вместе с более быстрыми / мощными компьютерами и инструментами компьютерного кластера для расширения возможностей алгоритмов моделирования, имеют первостепенное значение в такой работе и откроют возможности для идентификации даже самых крупных и сложных белковых структур. Новые инструменты моделирования и недавно разработанные алгоритмы будут доступны для исследователей и других лиц в ближайшем будущем, вместе с более мощными компьютерами и компьютерными кластерами, которые проложат путь для моделирования даже самых крупных и изначально неупорядоченных белков, таких как глютелин, хранящий семена. белки.В будущем исследования глиадинов и глютенинов могут также выиграть от аналогичного подхода к подходам, используемым для эластомерных белков, с использованием моделей низкой сложности (не крупнозернистых) и / или работы с пептидными фрагментами для выявления поведения белков [125]. Такое моделирование откроет новые возможности для оценки биологических свойств растений и для точной настройки свойств продуктов питания и материалов, производимых из этих белков.
6. Выводы
Сочетание инноваций в компьютерных технологиях, повышенной скорости и мощности компьютеров, а также новых инструментов моделирования / симуляции расширит возможности, которые определяют структуры белков и выявляют взаимосвязи между структурой и функцией.До недавнего времени инструменты моделирования и симуляции редко использовались для оценки структур растительных белков и взаимосвязей между структурой и функцией. Таким образом, менее 9% текущих депозитов в Исследовательском сотрудничестве в банке данных по структурной биоинформатике связаны с растениями, а возраст одной трети этих депозитов составляет менее пяти лет. Для двух наиболее распространенных типов растительных белков, RuBisCO и запасных белков, моделирование использовалось в разной степени. Для RuBisCO и фотосинтетического аппарата моделирование использовалось довольно часто для описания процесса и структурных воздействий изменений в белке.Структурные особенности запасных белков были в меньшей степени описаны моделированием, особенно для проламина и глютелина. Текущее состояние моделирования в отношении структурных особенностей запасных белков проиллюстрировано на примерах белков глобулина (соя, горох), проламина (α-глиадин пшеницы) и глютелина (глютенин пшеницы), соответственно.
Вклад авторов
Идея проекта и этой статьи E.J. и M.H .; концептуализация данной статьи была выполнена совместно Ф.R., J.M. and E.J .; планирование и определение подразделов было выполнено совместно F.R., J.M. и E.J .; подготовка таблиц производилась Ф.Р .; подготовка и моделирование были выполнены J.M .; написание отдельных подразделов, F.R, J.M. и E.J. письмо — подготовка оригинального проекта, E.J .; написание — просмотр и редактирование, M.H .; визуализация, E.J .; надзор, E.J., M.H., F.R .; администрация проекта, E.J .; привлечение финансирования, E.J., M.H. Все авторы прочитали и согласились с опубликованной версией рукописи.
Какие источники растительного белка являются лучшими?
Возможно, вы слышали об отчете комиссии EAT-Lancet, в котором излагается схема питания здоровых людей и здоровой планеты. В этом отчете, который был разработан 37 учеными и выпущен ранее в этом году, было обнаружено, что лучшая диета для людей и планеты включает в себя разнообразные продукты растительного происхождения, с низким содержанием животных белков, предпочтение ненасыщенных жиров по сравнению с насыщенными и ограничивает количество рафинированных зерновые, продукты с высокой степенью обработки и добавленный сахар.
Данные свидетельствуют о том, что такой режим питания связан с большей продолжительностью жизни и, что не менее важно, с качеством жизни, включающим более здоровое тело и разум.
Употребление большего количества растительной пищи может принести пользу вашему организму (и планете). Предыдущие исследования показывают, что такой режим питания может снизить риск сердечных заболеваний и диабета 2 типа; способствовать более тонкой талии и более здоровой массе тела; обеспечивают более высокий уровень важных питательных веществ, таких как магний, калий, железо, фолиевая кислота и клетчатка; уменьшить воспаление и окислительный стресс, которые могут способствовать повреждению клеток (что ускоряет старение и может привести к хроническим заболеваниям), а также способствует более острому мышлению и меньшему количеству проблем с памятью с течением времени.
Связанные
Если идея сократить потребление мяса и молочных продуктов кажется сложной, это руководство для начинающих по растительному белку может помочь вам постепенно перейти на более растительную диету, которая лучше для вас и мира, в котором вы живете.
И независимо от того. Независимо от того, хотите ли вы прыгнуть обеими ногами или просто перекусить одним пальцем на растительной основе, вы получите выгоду от протеина, клетчатки и других защитных витаминов, минералов, антиоксидантов и растительных соединений, предлагаемых этими продуктами.
Можно ли получить достаточно белка, если не ешьте мясо?
«Совершенно возможно удовлетворить потребности в белке и других питательных веществах без мяса», — говорит Синтия Сасс, врач-диетолог, специализирующаяся на растительном питании.«С юных лет нас учат, что нашему телу нужно мясо. На самом деле наш организм нуждается в ключевых питательных веществах, содержащихся в мясе, но мы можем получить достаточное количество из продуктов растительного происхождения », — объясняет она.
Есть ли что-нибудь в сочетании растительных белков?
Все белки, растительные или животные, состоят из цепочки аминокислот. Белки животного происхождения считаются полноценными белками, потому что они содержат все девять незаменимых аминокислот, которые необходимы вашему организму для поддержания белковых тканей в организме.Большинству растительных белков не хватает одного или нескольких из этих девяти строительных блоков.
«Старая теория заключалась в том, что для эффективного использования растительного белка необходимо одновременно есть дополнительные белки. Например, рис и бобы дополняют друг друга, потому что ключевые аминокислоты, отсутствующие в бобах, содержатся в рисе, и наоборот », — говорит Сасс. Она объясняет, что больше не нужно беспокоиться об объединении растительных белков, если вы потребляете достаточно калорий и широкий спектр растительных продуктов.«Достаточное количество незаменимых аминокислот можно получить в течение 24 часов. Печень помогает, накапливая в течение дня различные незаменимые аминокислоты для последующего использования », — говорит она.
Тем не менее, она подчеркивает важность полноценной и разнообразной диеты (а не веганской нездоровой пищи!). «Чтобы лучше обеспечить ваше тело широким спектром аминокислот, а также витаминов, минералов и антиоксидантов, смешивайте свои блюда и закуски. Включите овощи и фрукты, а также цельнозерновые, бобовые (фасоль, чечевицу, горох, нут), орехи и семена », — говорит она.
Согласно Sass, когда вы едите здоровую пищу, большая часть ваших блюд в любом случае должна быть на растительной основе: овощи, растительные жиры, такие как оливковое масло первого отжима, авокадо или тахини, а также цельнозерновые или крахмалистые овощи. , например, киноа, коричневый рис, сладкий картофель или спагетти из тыквы.
«Это означает, что единственное, что вам нужно сделать, — это обменять мясо на растительную альтернативу, что проще, чем вы думаете», — говорит она. «Многие люди, когда думают, что приготовить на ужин, в первую очередь сосредотачиваются на мясе.Измените эту схему, добавив в свой список белков зернобобовые (общий термин для обозначения фасоли, чечевицы, гороха и нута) и заменители мяса на основе горохового белка », — предлагает она.
Чтобы более комфортно употреблять растительные белки, Джеки Ньюджент, RDN и автор «The All-Natural Diabetes Cookbook», рекомендует начинать с ингредиентов, богатых растительным белком, таких как арахисовое масло или хумус, с которыми вы уже знакомы, и затем забирая это оттуда. «Например, если вы уже наслаждаетесь хумусом (на основе нута) в качестве соуса, используйте его как пасту для сэндвичей или топпер для тостов», — говорит она.
Смузи с высоким содержанием белка и ванильюAmy Gorin NutritionЭми Горин, RDN, владелица Amy Gorin Nutrition, предлагает аналогичный подход — в данном случае для любителей смузи: «Смешайте растительные белки, такие как эдамаме, тофу или консервированный нут, в течение протеиновый пунш. Эти смеси передают ароматы других ингредиентов, поэтому они не будут такими сильными, как если бы вы съели их в одиночку ».
Попробуйте этот рецепт: Ванильный смузи с высоким содержанием белка
Еще одна идея начального уровня — это своп на основе белка.«Подумайте о том, чтобы использовать хумус вместо сыра в кесадилье, попробуйте темпе или тофу вместо мяса в жарком и наслаждайтесь фасолью или чечевицей вместо мяса в начинке с чили или тако», — говорит Ньюджент. Энджи Аш, доктор медицинских наук и владелец компании Eleat Sports Nutrition, LLC, говорит, что ее спортсмены предпочитают растительные блюда — схватку с тофу. «При измельчении и приготовлении с пищевыми дрожжами, порошком чили, перцем и некоторыми другими специями он приобретает текстуру, напоминающую яичницу, которая имеет восхитительный вкус с картофельными оладьями, перцем и луком», — говорит Аше.
Попробуйте этот рецепт: Тако для веганских завтраков
Тако для веганских завтраков Eleat Sports NutritionКак готовить с растительными белками
«При использовании растительных белков учтите, что их кулинарные свойства могут различаться. от белка животного происхождения. Например, если вы используете консервированную фасоль в чили вместо сырого говяжьего фарша, вам не нужно обжаривать фасоль. И вкус тоже будет отличаться. Вы можете получить меньше умами — этого пикантного вкуса.Так что, помимо растительного белка, подумайте о том, чтобы улучшить вкус другими способами, например, добавив грибы, соевый соус или другие ингредиенты, богатые умами », — говорит Ньюджент.
Asche разделяет аналогичный совет. «Растительные белки, такие как тофу и темпе, невероятно легко приготовить, но их нужно заправлять или мариновать. Если вы попытаетесь просто нарезать тофу и зажарить его на сковороде, скорее всего, он вам не понравится », — говорит она.
Количество белка, которое вы можете получить из растительных источников, может варьироваться.Ниже мы рассмотрим белок из распространенных источников, а также несколько простых рецептов, которые помогут вам упростить свой путь к употреблению большего количества белка из растений.
1. Бобовые
Эти продукты содержат большое количество полезных минералов, таких как калий, магний, фолиевая кислота и железо, которых часто не хватает в нашем рационе. Хотя вы можете купить их сушеными (и ускорить приготовление в Instant Pot), консервированные бобы значительно упрощают употребление этих продуктов. «Одно из преимуществ растительных белков, таких как консервированные бобы, заключается в том, что вам не нужно много готовиться.Приготовить обед или ужин на растительной основе часто бывает намного быстрее, чем ждать прибытия еды на вынос », — говорит Горин.
Хумус на гриле «Кесадилья» Джеки Ньюджент, RDNОдна чашка консервированного нута содержит около 11 граммов белка, а чашка чечевицы — около 18 граммов; чашка черной фасоли содержит 14 граммов белка. Есть так много способов насладиться этими блюдами, но некоторые из самых простых:
- Сверху салаты или миски с овощами
- Сложенные в тако или кесадильи (см. Ниже)
- В качестве основы вегетарианских гамбургеров
- Смешанные с энергетические шарики размером с закуску или обжаренные в закуски (как показано ниже)
Попробуйте эти рецепты:
Сладкие и соленые закуски из нута с кунжутом Jackie Newgent, RDN2.Орехи
Содержание белка в орехах варьируется от 4 граммов (грецкие орехи) до 7 граммов (фисташки) на четверть стакана. Количество может показаться небольшим, но оно довольно близко к вареному яйцу, в котором около 6 граммов. Кроме того, если учесть тот факт, что орехи часто сочетаются с другими источниками растительного белка, легко увидеть, что они могут дать вам хороший импульс. Есть бесконечное количество способов насладиться орехами и их маслом (как вы, вероятно, знаете!), Но вот еще несколько:
- Нарезанные и поданные с теплыми фруктами
- Добавлены к жареному столу
- Нарезанные на соусы и пасты (см. Ниже )
- В качестве «мучной» основы для выпечки
Попробуйте этот рецепт: Заправка для ранчо из кешью
Заправка для ранчо из кешьюЭми Кац, Veggies Save the Day.СеменаВ порции семян конопли из 3 столовых ложек содержится 10 граммов растительного белка. В таком же количестве семян чиа более 5 граммов. Порция тахини, состоящая из 2 столовых ложек молотого масла из семян кунжута, содержит 5 граммов этого питательного вещества.
Для таких ингредиентов, как орехи и семена, Newgent предлагает посыпать ими блюда, которые вам уже нравятся. «Это может быть так же просто, как добавить семена чиа или конопли в ваш любимый смузи», — говорит она. Помимо протеина, семена чиа поглощают в 10 раз больше своего веса в жидкости, поэтому при использовании их в смузи и пудингах вы получите более густую кремообразную консистенцию.
Семена очень разносторонние. Среди способов их использования:
- В качестве начинки тоста с авокадо
- Посыпать тушеными овощами
- В качестве основного ингредиента пудинга с чиа (как в рецепте ниже)
Попробуйте этот рецепт: Зеленый пудинг с чиа
Зеленый пудинг с чиаЭми Кац, «Овощи спасут день»4. Зерновые
Квиноа, вероятно, является наиболее примечательным зерном, богатым белком (что парадоксально, поскольку на самом деле это семена), но другие цельнозерновые продукты поставляют белок также.Вы найдете около 6 граммов белка в чашке вареного пшена или булгура и около 7 граммов в таком же количестве дикого риса; для справки: в лебеде 8 граммов на чашку. Опять же, эти цифры могут вас не удивить, но в сочетании с другими источниками растительного белка они могут составлять значимые суммы. Вот некоторые богатые белком способы включения цельного зерна:
- В виде горячих хлопьев, перемешанных с измельченными орехами и фруктами
- В плове или запеканке с бобовыми и другими яркими овощами (см. Ниже)
- Добавляют бобовые в салаты и Миски с овощным зерном
Попробуйте этот рецепт: Запеканка из киноа из черной фасоли
Запеканка из киноа из черной фасоли Эми Кац, овощи спасают день5.Соя
Как и животные источники белка, цельная соя является полноценным источником девяти незаменимых аминокислот, необходимых вашему организму. Цельные соевые продукты включают тофу, эдамаме, соевые орехи, соевое молоко и темпе. Порция тофу в 3 унции содержит почти 9 граммов белка — столько же, сколько полстакана очищенного от скорлупы эдамаме.
Связанные
Раньше существовали опасения по поводу того, могут ли соевые продукты, содержащие растительные эстрогены, имитирующие действие гормона, повышать риск гормонозависимого рака (например, рака груди и простаты).Однако, глядя на все существующие доказательства, Американский институт исследований рака говорит, что это не так, и что в некоторых популяциях цельные соевые продукты могут даже защищать от рака. Тем не менее, безопасность изолята соевого белка — широко потребляемой обработанной формы сои, содержащейся в постных бургерах, имитациях мяса, коктейлях и батончиках — все еще неизвестна, поэтому рекомендуется употреблять цельные формы сои.
Southwestern Vegan BowlEleat Sports NutritionПри выборе тофу Горин рекомендует обращать внимание на форму, которую вы используете.«Если вы хотите смешать его с смузи или использовать в качестве основы для приготовления шоколадного мусса, я бы порекомендовал мягкий тофу. Я предпочитаю твердый тофу для жарки или запекания — этот сорт лучше всего подходит, если вам нужна более мясная текстура. Многие люди не поклонники тофу просто потому, что не осознают, насколько универсален этот ингредиент! » Вот несколько простых способов съесть эти продукты целиком:
- Используйте очищенный эдамам вместо гороха в запеканках и блюдах из пасты (включая макароны и сыр)
- Попробуйте заменить очень твердый тофу на курицу (см. Рецепт тофу с пармезаном ниже)
- Сделайте крошки тофу, чтобы использовать их вместо говяжьего фарша или индейки в блюдах для тако и зерновых тарелках (как в рецепте ниже)
Попробуйте эти рецепты:
СОВЕТЫ ПО ЗДОРОВОМУ ПИТАНИЮ
Хотите больше советов, как эти? NBC News BETTER одержимы поиском более простых, здоровых и разумных способов жизни.Подпишитесь на нашу рассылку и следите за нами в Facebook, Twitter и Instagram.
Растительная жизнь: белки и аминокислоты
Белки находятся во всех клетках и выполняют множество важных клеточных функций. Внутри любой клетки могут быть тысячи различных белков, имеющих различные размеры, структуры и функции. Белки также являются важными структурными компонентами клеточной стенки.
Белки являются наиболее сложными и многочисленными макромолекулами. Внутри клетки многие белки функционируют как ферменты в катализе метаболических реакций, в то время как другие служат транспортными молекулами, запасными белками, переносчиками электронов и структурными компонентами клетки.
Они особенно важны для семян, где они составляют до 40 процентов веса семян и служат для хранения аминокислот для развивающегося зародыша.
Белки также являются важными структурными компонентами клеточной стенки. Поскольку белки и их строительные блоки, аминокислоты, составляют такой крупный компонент жизни растений, растения служат важным пищевым источником восьми-десяти незаменимых аминокислот для людей и других животных.
Аминокислоты
Аминокислоты — это молекулярные строительные блоки белков.Все аминокислоты имеют общую структуру с центральным атомом углерода, альфа-углеродом, ковалентно связанным с атомом водорода, аминогруппой, группой карбоновой кислоты и группой, обозначенной как R-группа, структура которой варьируется от аминокислоты до аминокислота.
Именно разнообразная природа группы R обеспечивает белку многие его структурные и функциональные характеристики. Некоторые группы R являются полярными или электрически заряженными при физиологическом pH, что делает группы R гидрофильными (водолюбивыми).Другие группы R неполярны и гидрофобны (избегают воды).
Двадцать стандартных аминокислот, которые клетка использует для синтеза своих белков, — это аланин, аргинин, аспартат (аспарагиновая кислота), аспарагин, цистеин, глутамат (глутаминовая кислота), глутамин, глицин, гистидин, изолейцин, лейцин, лизин, метионин, фенилаланин. , пролин, серин, треонин, триптофан, тирозин и валин.
Каждая из двадцати аминокислот отличается от других девятнадцати структурой своей R-группы.После включения в белок стандартная аминокислота может подвергаться модификации, чтобы создать нестандартные аминокислоты и еще большее разнообразие белковых структур.
Одной из наиболее распространенных нестандартных аминокислот, содержащихся в белках, является гидроксипролин, который обычно содержится в белках клеточной стенки растений. В дополнение к двадцати аминокислотам, из которых строятся белки, многие нестандартные аминокислоты свободно встречаются в клетке и не обнаруживаются в белках. Канаванин, например, содержится в семенах многих бобовых.
Основываясь на информации о клеточной дезоксирибонуклеиновой кислоте (ДНК), клетка соединяет двадцать стандартных аминокислот пептидными связями в определенных последовательностях, в результате чего образуются цепи от двух до многих тысяч. Более короткие цепи аминокислот называются пептидами или олигопептидами, а более длинные цепи называются полипептидами.
Термин «белок» обычно зарезервирован для тех олигопептидов и полипептидов, которые выполняют биологические функции, поскольку отдельные полипептиды часто не выполняют биологических функций, если они не связаны с другими полипептидами.
Первичная структура
Белки отличаются друг от друга последовательностями аминокислот. Последовательность аминокислот белка называется его первичной структурой. Было показано, что мутации приводят к изменению всего лишь одной аминокислоты в белке. Поскольку ДНК определяет первичную структуру белка, информация о последовательности белка часто используется для изучения эволюционных взаимоотношений между организмами.
Белки часто образуют комплексы с другими соединениями в их биологически активном состоянии.Эти белки называются конъюгированными белками. Белки в комплексе с металлами, липидами, сахарами и рибофлавином называются металлопротеинами, липопротеинами, гликопротеинами и флавопротеинами соответственно.
Гликопротеины (буквально «сахарные белки») являются важными составляющими плазматической мембраны. Эти молекулы сахара могут встречаться по отдельности или в виде коротких простых разветвленных цепей.
| От аммониевых кислот к белкам |
Белковая цепь может быть свернута в различные трехмерные формы.Трехмерная форма, которую принимает белок, называется его конформацией и определяется его аминокислотной последовательностью.
Чтобы белок был активным, он должен принять определенную конформацию. Любое изменение его строения может привести к снижению активности. Денатурирующие агенты изменяют структуру белка, так что он теряет свою конформацию, биологическую функцию и активность.
Вторичная структура
Вторичная структура относится к локальному складыванию или конформации полипептидной цепи на относительно коротких (около пятидесяти аминокислот) участках.
Две общие вторичные структуры, альфа-спираль и бета-лист, регулярно встречаются в белках. В среднем только около половины полипептидной цепи принимает альфа- или бета-конформацию, тогда как остальная часть существует в виде чередований и случайных структур.
Некоторые белки показывают только альфа-структуру, другие — только бета-структуру, в то время как третьи демонстрируют либо смесь двух структур, либо ни одну вторичную структуру. Как альфа-, так и бета-структуры повышают структурную стабильность белка.Аминокислотная последовательность определяет, будет ли конкретная последовательность аминокислот в белке иметь альфа- или бета-структуру.
Третичная структура
Общая пространственная ориентация всей полипептидной цепи в пространстве называется ее третичной структурой. Обычно различают две третичные структуры. Волокнистые или нитчатые белки расположены в виде волокон или листов, в то время как глобулярные белки расположены примерно в виде сферических или глобулярных структур.
Аминокислотная последовательность определяет общий фолдинг третичной структуры белка.Волокнистые белки в основном участвуют в структурных функциях, тогда как глобулярные белки действуют как ферменты, транспортные молекулы, переносчики электронов и регуляторные белки.
Четвертичная структура
Некоторые белки состоят из более чем одной полипептидной цепи. Белок, состоящий только из одного полипептида, называется мономером, в то время как белки, состоящие из двух, трех, четырех и так далее, называются димерами, тримерами, тетрамерами и так далее, соответственно.
Как растения получают белок?
Все начинается с корней.Растения получают питательные вещества из двух разных систем — одна начинается в листьях и отвечает за фотосинтез. Другой начинается у корней и перемещает воду, наполненную растворенными ионами, вверх по растению. Белок — одно из питательных веществ, которые начинаются с корней и продвигаются вверх.
Растения — автотрофы
Растения — автотрофы. В отличие от животных, которые должны получать пищу из внешних источников, таких как растения и другие животные, растения могут производить сами.Растения берут основные элементы из внешнего мира и приносят их в свои тела, где они превращаются в крахмал и белки, которые могут использоваться растением или животным, которое их ест.
Азот и бактерии
Белок производится из нитрата, формы азота, фиксируемой микроорганизмами. Растения не могут использовать азот напрямую, поэтому они полагаются на бактерии, чтобы преобразовать азот в форму, которую они могут использовать. Эти бактерии обитают возле корней растений или в специальных структурах на корнях, называемых клубеньками.Бактерии в клубеньках сформировали симбиотические отношения с растениями, где они обменивают пригодный для использования азот растений сахар.
Нитраты и аминокислоты
Нитраты, попадающие в растение через корни, поступают в растение, где они превращаются в 20 различных видов аминокислот. Эти аминокислоты превращаются в белки в специальных структурах клеток, называемых рибосомами. Эти конструкции находятся в четырех местах на заводе. Некоторые свободно плавают в цитоплазме клеток, а другие прикрепляются к поверхности эндоплазматического ретикулума, митохондрий и хлоропластов.
Транспорт белков
Из рибосом, содержащихся в эндоплазматическом ретикулуме, белки направляются в аппарат Гольджи. Аппарат Гольджи сортирует эти белки для распределения по растению, где они будут использоваться для формирования новых структур для дальнейшего транспорта питательных веществ, а также для основных метаболических процессов.

 , Marshall B., Lienard D., Faye L. (2009). From Neanderthal to nanobiotech: from plant potions to pharming with plant factories. Methods Mol. Biol. 483, 1–23;
, Marshall B., Lienard D., Faye L. (2009). From Neanderthal to nanobiotech: from plant potions to pharming with plant factories. Methods Mol. Biol. 483, 1–23; Biotechnol. Appl. Biochem. 58, 58–67;
Biotechnol. Appl. Biochem. 58, 58–67; J., Borca M.V. (1999). Protection of mice against challenge with foot and mouth disease virus (FMDV) by immunization with foliar extracts from plants infected with recombinant tobacco mosaic virus expressing the FMDV structural protein. Virology. 264, 85–91;
J., Borca M.V. (1999). Protection of mice against challenge with foot and mouth disease virus (FMDV) by immunization with foliar extracts from plants infected with recombinant tobacco mosaic virus expressing the FMDV structural protein. Virology. 264, 85–91; , Vojdani F. et al. (2008). Plant-produced idiotype vaccines for the treatment of non-Hodgkin’s lymphoma: safety and immunogenicity in a Phase I clinical study. Proc. Natl. Acad. Sci. USA. 105, 10131–10136;
, Vojdani F. et al. (2008). Plant-produced idiotype vaccines for the treatment of non-Hodgkin’s lymphoma: safety and immunogenicity in a Phase I clinical study. Proc. Natl. Acad. Sci. USA. 105, 10131–10136; 5
5 5
5 Если потребление калорий является низким, поскольку Вы сидите на диете или по любой другой причине, Вам, возможно, потребуется добавить несколько дополнительных богатых белком продуктов питания в ваше меню.
Если потребление калорий является низким, поскольку Вы сидите на диете или по любой другой причине, Вам, возможно, потребуется добавить несколько дополнительных богатых белком продуктов питания в ваше меню. R. Young and P. L. Pellett, “Plant Proteins in Relation to Human Protein and Amino Acid Nutrition,” American Journal of Clinical Nutrition 59, suppl. no. 5 (1994): S1203–S1212.
R. Young and P. L. Pellett, “Plant Proteins in Relation to Human Protein and Amino Acid Nutrition,” American Journal of Clinical Nutrition 59, suppl. no. 5 (1994): S1203–S1212.